Clear Sky Science · es
Embigin participa en la regulación del desarrollo renal temprano en ratón
Por qué importan los riñones pequeños
Antes de que nazca un bebé, sus órganos atraviesan un proceso de construcción complejo en el que las células deben dividirse, moverse y conectarse de manera precisa. Los riñones, que filtran la sangre y mantienen el equilibrio de sal y agua en el cuerpo, se ensamblan a partir de tubos ramificados que crecen como las ramas de un árbol. Este estudio explora una proteína de superficie poco conocida llamada embigin y muestra que contribuye discretamente a guiar la configuración temprana del riñón de ratón —especialmente la formación de las primeras ramas—, ofreciendo pistas sobre cómo se coordina el crecimiento de los órganos y qué puede fallar en enfermedades.
Un ayudante en la superficie celular
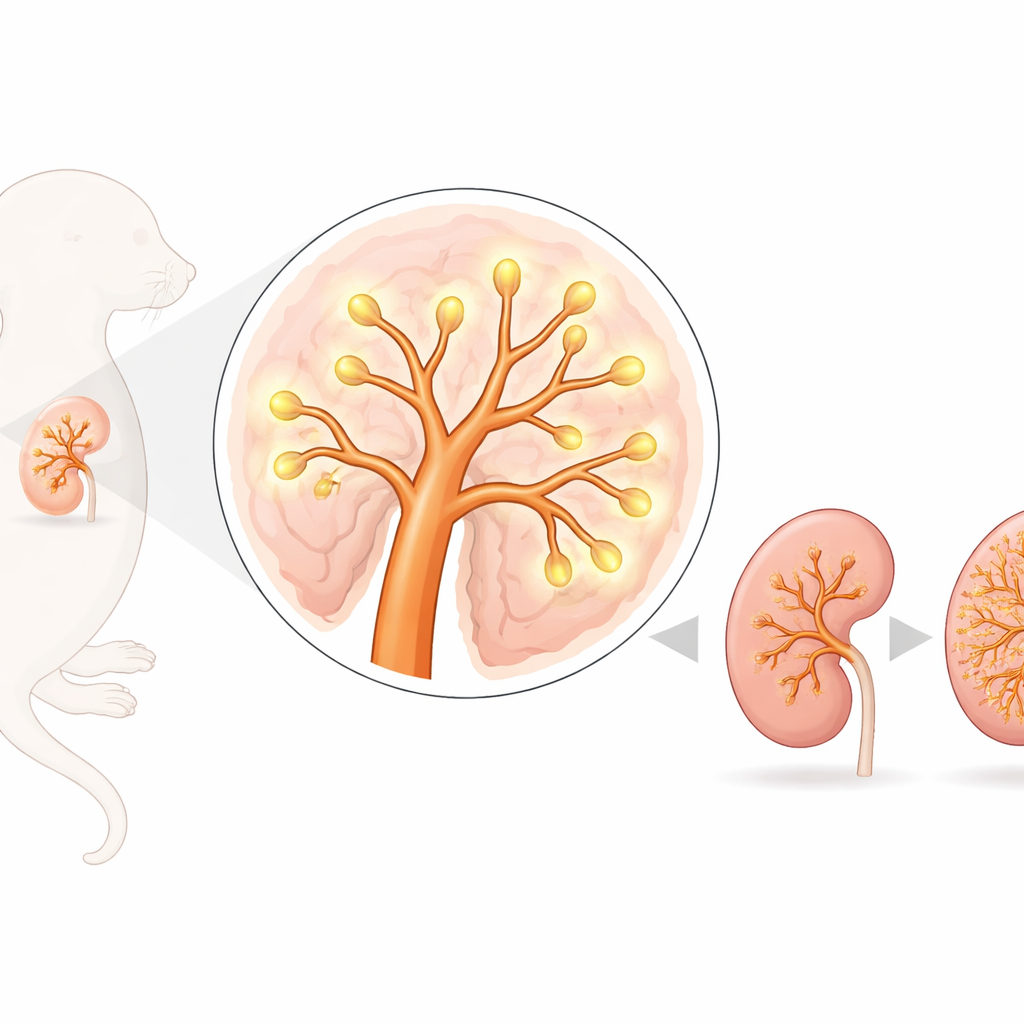
Embigin se encuentra en la membrana externa de las células y se sabe que ayuda a ciertas proteínas transportadoras que mueven pequeñas moléculas metabólicas dentro y fuera de las células. También puede unirse a componentes del andamiaje tisular que rodea a las células. Trabajos anteriores mostraron que los ratones que carecen de embigin tienen dificultades en el desarrollo pulmonar y a menudo mueren poco después del nacimiento, lo que sugiere que esta proteína es importante para construir órganos. Aquí, los investigadores preguntaron si embigin desempeña un papel similar en el riñón, donde el desarrollo comienza con un simple brote que se divide repetidamente para formar el futuro sistema colector de orina y desencadena la formación de unidades filtrantes llamadas nefronas.
Guiando la ramificación renal temprana
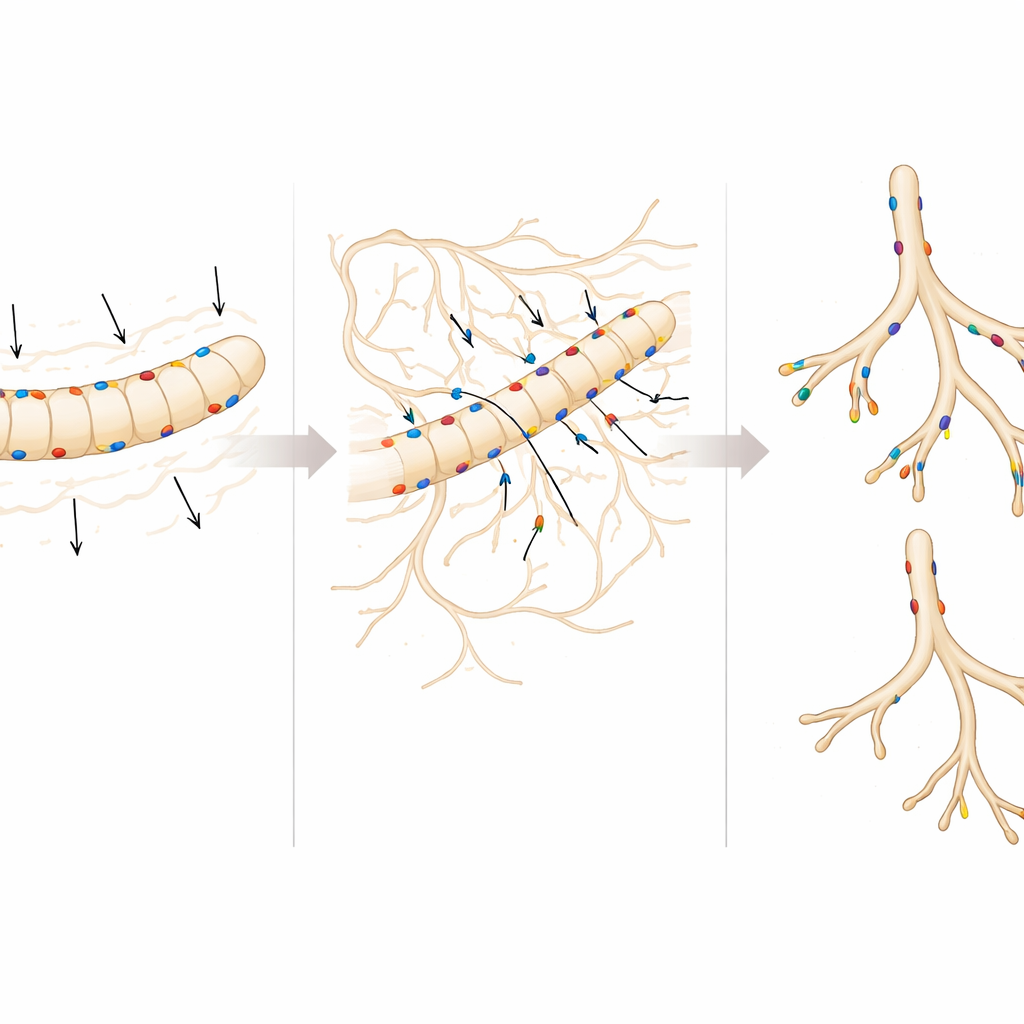
Mediante microscopía fluorescente, el equipo encontró que embigin está presente de forma intensa en los tubos ramificados del riñón temprano —conocidos como brote ureteral— y en células que comienzan a convertirse en nefronas, pero no en las células madre renales más primitivas que cubren las puntas en crecimiento. Cuando cultivaron riñones embrionarios de ratones normales y de ratones deficientes en embigin en una etapa temprana, la diferencia fue notable: los riñones sin embigin produjeron muchas menos puntas ramificadas y, en conjunto, los riñones eran más pequeños en etapas posteriores de la gestación. Sin embargo, al comparar el tamaño renal con el tamaño corporal total, las proporciones fueron similares, lo que sugiere que embigin contribuye tanto al crecimiento general como al modelado específico del riñón.
Desarrollo retrasado, no destruido
Para ver qué ocurría a nivel molecular, los investigadores midieron la actividad génica en riñones en desarrollo. En un punto de la mitad de la gestación, los riñones sin embigin mostraron una reducción en la actividad de docenas de genes vinculados a la construcción de nefronas, al modelado de los tubos, al control de la presión sanguínea y al manejo de los fluidos corporales. Varios de los genes más afectados son cruciales para células especializadas llamadas podocitos, que forman parte de la barrera de filtración renal. Sin embargo, en una etapa posterior, estas diferencias en la expresión génica habían desaparecido en gran medida y la estructura renal parecía normal al microscopio. Los ratones adultos que sobrevivieron sin embigin no presentaron pérdida de proteína en la orina ni defectos estructurales renales evidentes, lo que apunta a un retraso temporal en el desarrollo más que a un daño permanente.
Señales compartidas entre tejidos
El equipo recurrió entonces a una línea celular epitelial de ratón, silenciando embigin para ver qué genes cambiaban. Aunque estas células no procedían del riñón, la pérdida de embigin volvió a alterar numerosos genes implicados en la formación de órganos, en la conformación de tubos y en vías relacionadas con el riñón. La comparación de los datos de la línea celular con los del riñón temprano resaltó tres genes —Pappa2, Acta2 y Tagln— que se redujeron de manera consistente cuando faltaba embigin. Estos genes se han relacionado con el desarrollo renal, el tono vascular y el movimiento celular, procesos que dependen de cómo las células perciben y se adhieren a su matriz circundante. El reanálisis de conjuntos de datos de secuenciación de ARN unicelular de embriones muy tempranos mostró que embigin ya está activo en los precursores renales más primitivos, reforzando la idea de que apoya decisiones clave al inicio de la formación de órganos.
Qué implica para la construcción de órganos
En conjunto, los hallazgos presentan a embigin como un organizador sutil pero importante del crecimiento renal temprano. No parece ser absolutamente imprescindible para tener un riñón funcional —otras proteínas pueden compensar con el tiempo—, pero ayuda a asegurar la ramificación oportuna del árbol tubular temprano y la activación adecuada de redes génicas que moldean nefronas y estructuras filtrantes sanguíneas. Para un lector general, el mensaje es que proteínas de superficie celular aparentemente oscuras pueden tener efectos amplios en la morfología de los órganos, y que comprender a estos ayudantes ocultos podría algún día mejorar nuestra comprensión de problemas renales congénitos y guiar estrategias para crecer o reparar tejido renal.
Cita: Talvi, S., Jokinen, J., Rappu, P. et al. Embigin is involved in the regulation of early mouse kidney development. Sci Rep 16, 8403 (2026). https://doi.org/10.1038/s41598-026-39966-7
Palabras clave: desarrollo renal, embigin, morfogénesis por ramificación, células madre, formación de órganos