Clear Sky Science · es
La dinámica de la actina mediada por caldesmón‑1 es esencial para la diferenciación osteogénica de las células intersticiales de la válvula aórtica
Por qué importa el endurecimiento de la válvula cardíaca
A medida que las personas envejecen, una de las puertas principales del corazón —la válvula aórtica— puede volverse gradualmente rígida y prácticamente como una piedra. Esta afección, llamada estenosis aórtica, obliga al corazón a bombear con más esfuerzo y puede conducir a insuficiencia cardíaca. Hoy por hoy, los únicos tratamientos fiables son el reemplazo valvular quirúrgico o por catéter. El estudio resumido aquí plantea una pregunta básica pero crucial: ¿qué hace que el tejido blando y flexible de la válvula se transforme poco a poco en material similar al óseo? Al descubrir un actor molecular clave en este proceso, la investigación apunta a futuros fármacos que podrían ralentizar o incluso prevenir la calcificación valvular en lugar de limitarse a sustituir la válvula dañada.
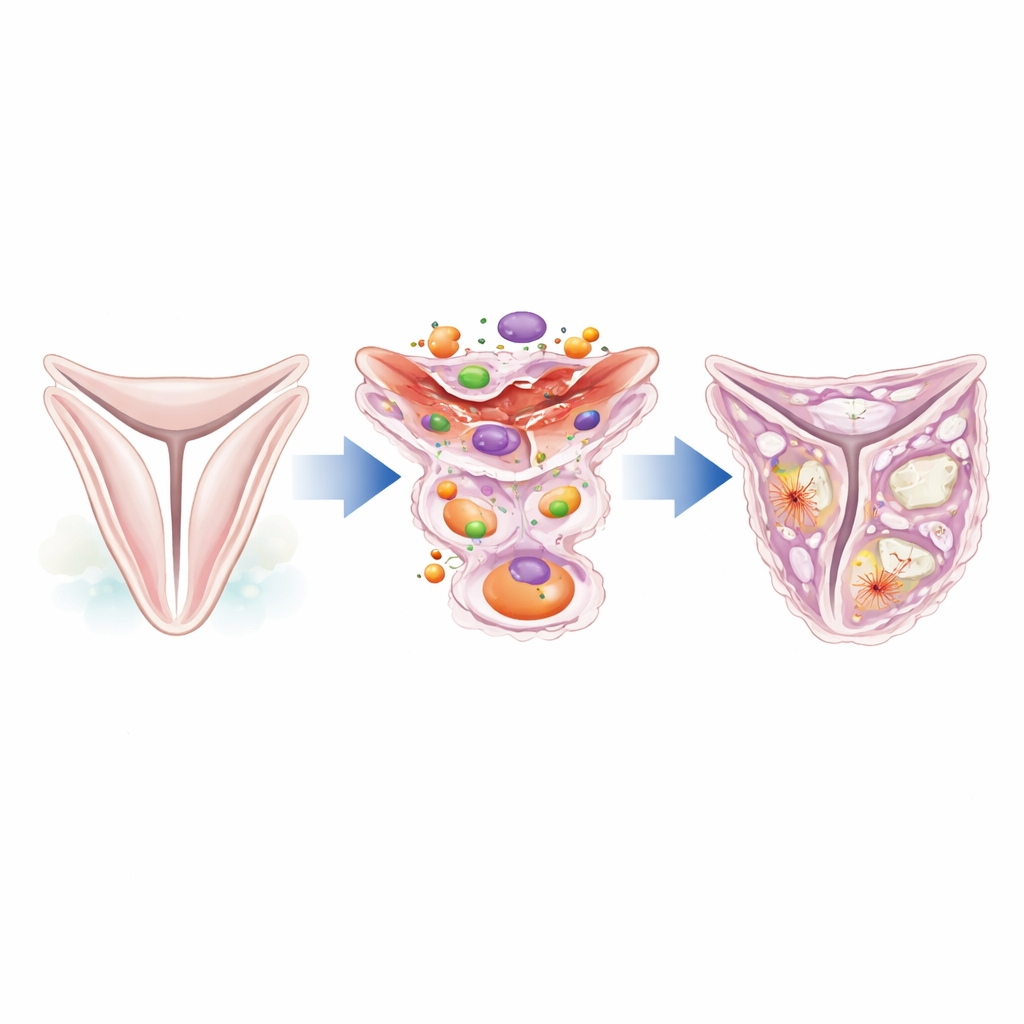
Una mirada más cercana a los trabajadores ocultos de la válvula
Las valvas de la válvula aórtica están sostenidas por una delgada capa de células de soporte especializadas conocidas como células intersticiales valvulares. En una válvula sana, estas células permanecen en estado de reposo y ayudan a mantener la estructura del tejido. Sin embargo, bajo estrés o lesión pueden cambiar de identidad y empezar a comportarse como células formadoras de cicatrices o incluso como células formadoras de hueso. Los autores se centraron en una proteína llamada caldesmón‑1, que ayuda a controlar el andamiaje interno de la célula compuesto por filamentos de actina. Al analizar datos de secuenciación de ARN unicelular ya existentes de válvulas humanas, encontraron que caldesmón‑1 está fuertemente incrementada en válvulas de pacientes con estenosis aórtica en comparación con válvulas normales, especialmente en células intersticiales presentes en regiones engrosadas y fibróticas.
Del tejido flexible a parches fibróticos y similares al hueso
Estudios al microscopio de muestras humanas de válvulas revelaron que la proteína caldesmón‑1 es abundante en las valvas enfermas y se alinea con marcadores de células activadas y contráctiles y de células tipo fibroblasto que producen colágeno. Estas células ricas en caldesmón‑1 se agrupan alrededor de áreas de fibrosis y calcificación temprana, lo que sugiere que contribuyen a construir la matriz extra que engrosa la válvula. Un análisis más profundo mostró que estas células expresan genes típicos de tipos celulares similares a músculo liso y proclives a formar hueso, y son grandes productoras de proteínas estructurales como el colágeno tipo I. En otras palabras, allí donde la válvula se vuelve rígida y cicatriza, las células intersticiales positivas para caldesmón‑1 están presentes.
Cómo una proteína que controla la forma empuja a las células hacia el hueso
Para entender causa y efecto, el equipo aisló células intersticiales de válvulas humanas y utilizó ARN de interferencia para reducir los niveles de caldesmón‑1. Sin esta proteína, las células perdieron su forma alargada y fusiforme y se volvieron más redondeadas. Sus filamentos de actina internos se hicieron más delgados y disminuyeron su capacidad de dividirse y moverse de forma dirigida. Cuando los investigadores expusieron estas células a un medio de cultivo osteogénico, es decir, que estimula la formación ósea, las células normales formaron depósitos de calcio con facilidad, pero las células con caldesmón‑1 reducido mostraron mucha menos mineralización. La secuenciación masiva de ARN confirmó que muchos genes implicados en la formación ósea y en la remodelación tisular, incluidos impulsores osteogénicos conocidos como RUNX2 y la fosfatasa alcalina, se activaban fuertemente bajo condiciones osteogénicas pero no aumentaban cuando se había silenciado caldesmón‑1.
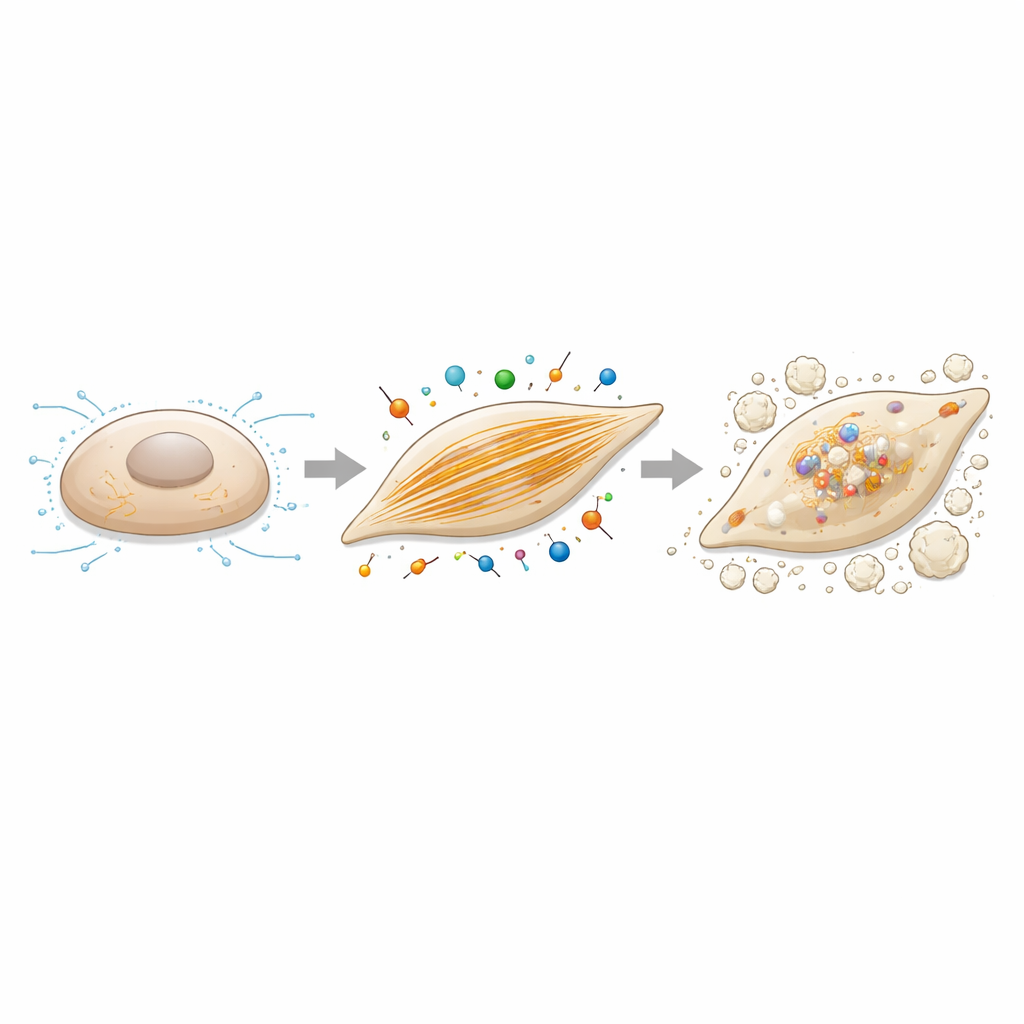
Los filamentos de actina como palanca de control para la calcificación
Dado que caldesmón‑1 regula la actina, los autores preguntaron si alterar la ensambladura de la actina en sí cambiaría la tendencia de las células a calcificarse. Trataron las células intersticiales valvulares con cictochalasin B, un compuesto que perturba suavemente el crecimiento de los filamentos de actina, mientras aplicaban las mismas condiciones de cultivo promotoras de hueso. A dosis que no comprometieron seriamente la supervivencia celular, este tratamiento redujo drásticamente la deposición de calcio y disminuyó la expresión de genes relacionados con la ossificación, incluido caldesmón‑1 y RUNX2. Junto con los experimentos de silenciamiento, estos hallazgos dibujan un panorama coherente: las redes robustas de filamentos de actina y las fuerzas contráctiles que sostienen no son meros espectadores, sino que impulsan activamente el cambio de células de soporte en reposo a células formadoras de hueso en la válvula.
Qué significa esto para futuros tratamientos
Para un público no especializado, el mensaje principal es que el endurecimiento de la válvula aórtica es un proceso activo y regulado, y no simplemente un “desgaste”. Este estudio identifica a caldesmón‑1 como un coordinador central que enlaza el esqueleto interno de la célula con el programa genético para producir tejido similar al óseo. Al ayudar a que las células intersticiales valvulares adopten una identidad contráctil, fibrótica y, en última instancia, osteogénica, caldesmón‑1 contribuye directamente a la acumulación de depósitos duros que estrechan la válvula. Aunque cualquier terapia que apunte a esta proteína o a la dinámica de la actina requerirá pruebas cuidadosas para evitar efectos indeseados en otros tejidos, las vías mediadas por caldesmón‑1 emergen ahora como candidatas prometedoras para fármacos destinados a ralentizar o detener la calcificación valvular antes de que sea necesario recurrir a cirugía.
Cita: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Palabras clave: calcificación de la válvula aórtica, caldesmón‑1, células intersticiales valvulares, citoesqueleto de actina, diferenciación osteogénica