Clear Sky Science · es
RBP4 interfiere en la progresión del carcinoma de células escamosas de la lengua al inhibir la vía de señalización PI3K/AKT y promover la polarización M1 de los macrófagos
Por qué el cáncer de lengua necesita nuevas ideas
El cáncer de lengua puede privar a las personas de la capacidad de hablar, comer y saborear, y aun con cirugía, quimioterapia y radioterapia, la supervivencia a largo plazo suele ser decepcionante. Este estudio explora a un aliado inesperado en nuestra sangre, una proteína transportadora de vitamina A llamada RBP4, y muestra cómo puede tanto frenar el crecimiento de los tumores de la lengua como movilizar a los defensores inmunitarios del propio organismo. Al desentrañar cómo funciona esta molécula dentro de las células cancerosas y en las células inmunitarias circundantes, la investigación apunta a estrategias nuevas que podrían algún día hacer los tratamientos más eficaces y menos dañinos.
Una proteína oculta en los tumores de la lengua
Los investigadores empezaron examinando grandes bases de datos genéticos de cáncer para ver qué genes relacionados con la inmunidad podrían predecir cómo evolucionan los pacientes con carcinoma de células escamosas de la lengua. Entre cientos de candidatos, RBP4, una proteína conocida por transportar vitamina A en el torrente sanguíneo, emergió como especialmente interesante. Al comparar muestras tumorales con tejido lingual sano adyacente, observaron que los niveles de RBP4 eran sistemáticamente mucho más bajos en el cáncer. Este patrón se confirmó en varios conjuntos de datos independientes y en muestras de tejido de 20 pacientes, lo que sugiere que la pérdida de RBP4 es una característica común de esta enfermedad.
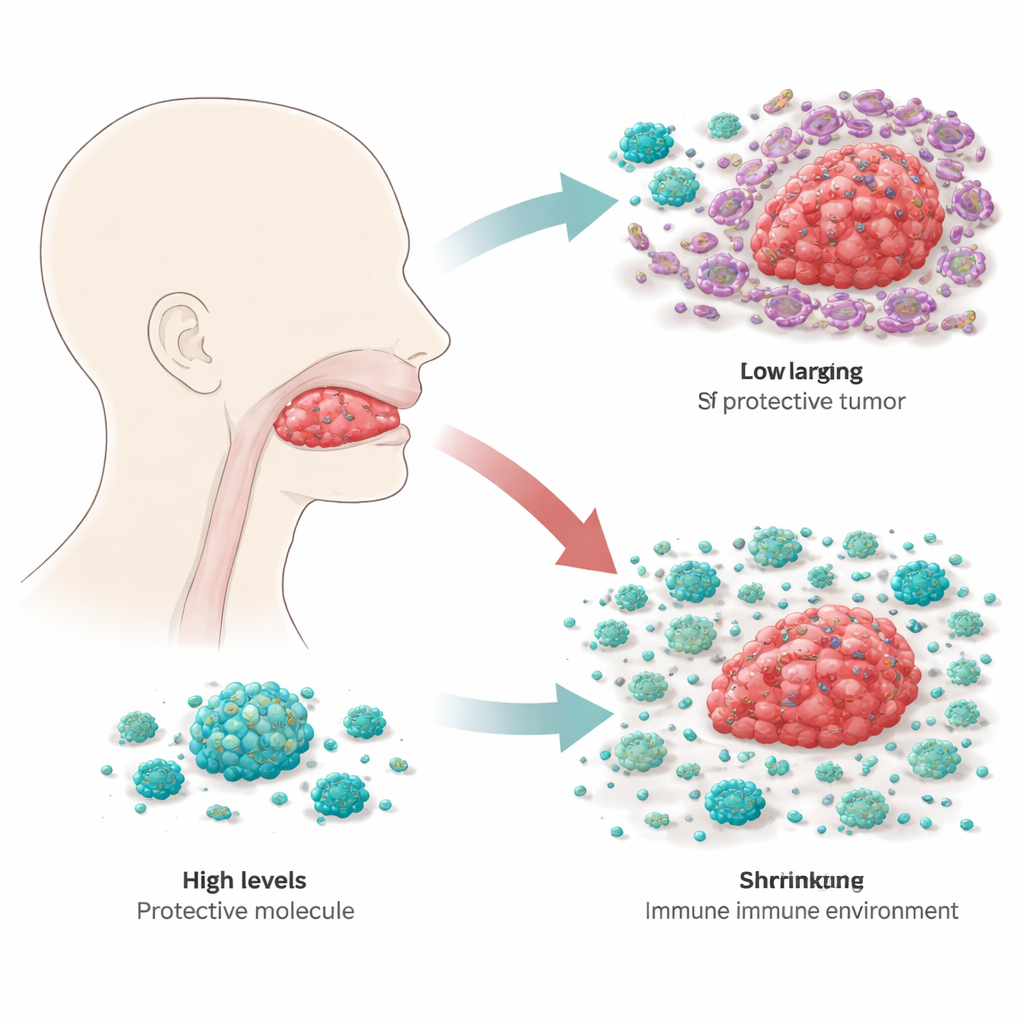
Frenar el crecimiento tumoral desde el interior
Para averiguar qué hace realmente RBP4 en las células del cáncer de lengua, los científicos diseñaron líneas celulares tumorales que producían o bien RBP4 extra o bien cantidades muy reducidas. En cultivo, las células con niveles altos de RBP4 crecieron más despacio, mientras que las que tenían RBP4 reducido se multiplicaron más rápido y mostraron mayor capacidad de movimiento e invasión a través de membranas artificiales, comportamientos asociados a la diseminación y la recaída. Cuando estas células modificadas se trasplantaron en ratones, los tumores con RBP4 extra permanecieron más pequeños, en tanto que los tumores con RBP4 reducido crecieron de forma más agresiva. Al seguir interruptores clave del control del crecimiento dentro de las células, el equipo demostró que RBP4 atenúa una vía de crecimiento mayor conocida como PI3K–AKT–mTOR, de la que muchos cánceres dependen como acelerador interno. Con niveles altos de RBP4, esta vía está más calmada y las células tumorales son menos capaces de adoptar el estado flexible y móvil que favorece la migración.
Convertir células inmunitarias en combatientes contra el tumor
El cáncer no crece en aislamiento; vive dentro de un vecindario de células inmunitarias, vasos sanguíneos y células de soporte llamado microambiente tumoral. Aquí, los macrófagos—grandes células inmunitarias que pueden atacar o ayudar a los tumores—desempeñan un papel central. Los investigadores observaron que los tumores con más RBP4 tendían también a contener más macrófagos de tipo “M1”, asociados a inflamación y destrucción tumoral, en lugar del tipo “M2”, que a menudo apoya el crecimiento tumoral. En cultivo celular, cuando los macrófagos se expusieron a RBP4 purificado o a células de cáncer de lengua modificadas para secretar más RBP4, se desplazaron hacia este estado M1, de lucha contra el tumor. Cuando RBP4 se redujo en las células cancerosas, los macrófagos tendieron a orientarse hacia el perfil más favorable al tumor.
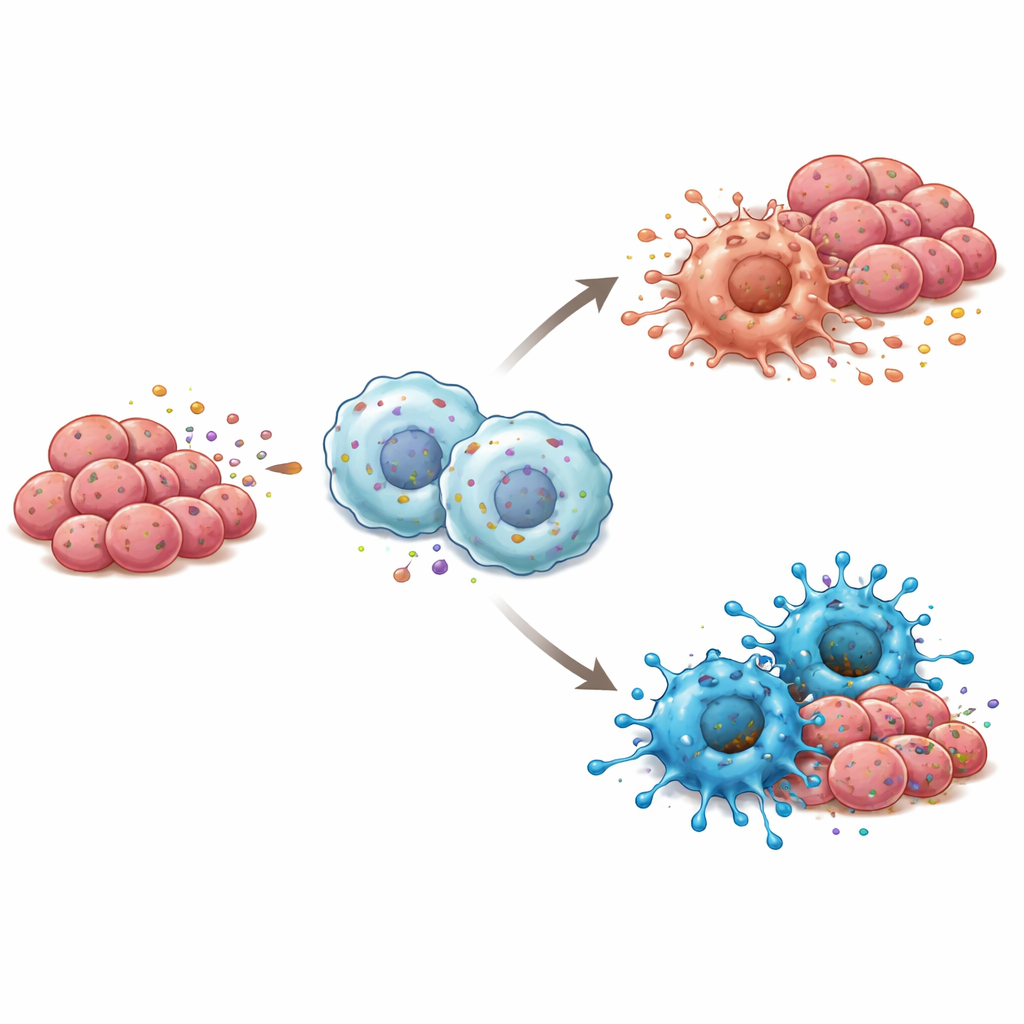
Vías de señalización tras el cambio inmunitario
Para entender cómo RBP4 induce a los macrófagos a adoptar una postura más hostil hacia los tumores, los investigadores examinaron qué sistemas de alarma internos se activaban en estas células inmunitarias. Encontraron que RBP4 estimulaba un sensor llamado TLR4 en la superficie del macrófago y, a su vez, activaba NF-κB, un interruptor maestro que impulsa respuestas inflamatorias. Bloquear TLR4 con un inhibidor químico detuvo esta reacción en cadena e impidió que los macrófagos adoptaran el estado M1, incluso en presencia de RBP4. En ratones, los tumores formados por células de cáncer de lengua ricas en RBP4 y mezcladas con macrófagos crecieron más despacio y contenían más células de tipo M1, junto con una mayor actividad de TLR4 y NF-κB, reforzando la idea de que esta vía es clave para los efectos inmunitarios de RBP4.
Qué podría significar esto para la atención futura
En conjunto, el trabajo presenta a RBP4 como un freno de doble acción sobre el cáncer de lengua: dentro de las células tumorales, atenúa un circuito de crecimiento hiperactivo, y en el entorno tumoral, ayuda a convertir a los macrófagos en defensores más vigilantes. Aunque quedan muchas preguntas—como exactamente cómo interactúa RBP4 con sus dianas y cómo aumentarlo de forma segura—el estudio sugiere que restaurar o imitar las acciones de RBP4 podría tanto ralentizar la expansión tumoral como fortalecer la presión inmunitaria del propio organismo sobre el cáncer. Para los pacientes, eso abre la posibilidad de terapias futuras que no solo extirpen los tumores, sino que también reconfiguren su cableado interno y su “ecosistema” local para evitar que regresen.
Cita: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Palabras clave: cáncer de lengua, RBP4, microambiente tumoral, macrófagos, vía PI3K AKT