Clear Sky Science · es
Impacto de la oxidación del ARN en G-cuádruplex sobre su dinámica conformacional e interacción con la proteína TDP-43 asociada a la ELA
Por qué esto importa para la salud neuronal
La esclerosis lateral amiotrófica (ELA) es una enfermedad letal en la que las células nerviosas que controlan el movimiento mueren lentamente, pero las causas precisas de este daño selectivo siguen siendo misteriosas. Este estudio planteó una pregunta simple pero importante: al envejecer y sufrir las células un mayor daño químico similar al “óxido”, ¿este desgaste del ARN —la copia de trabajo de nuestros genes— interrumpe señales vitales que mantienen vivas a las motoneuronas? Al examinar de cerca una forma de ARN plegada especial y una proteína clave vinculada a la ELA llamada TDP-43, el trabajo revela cómo pequeñas cicatrices químicas pueden contribuir a crear las condiciones para la enfermedad. 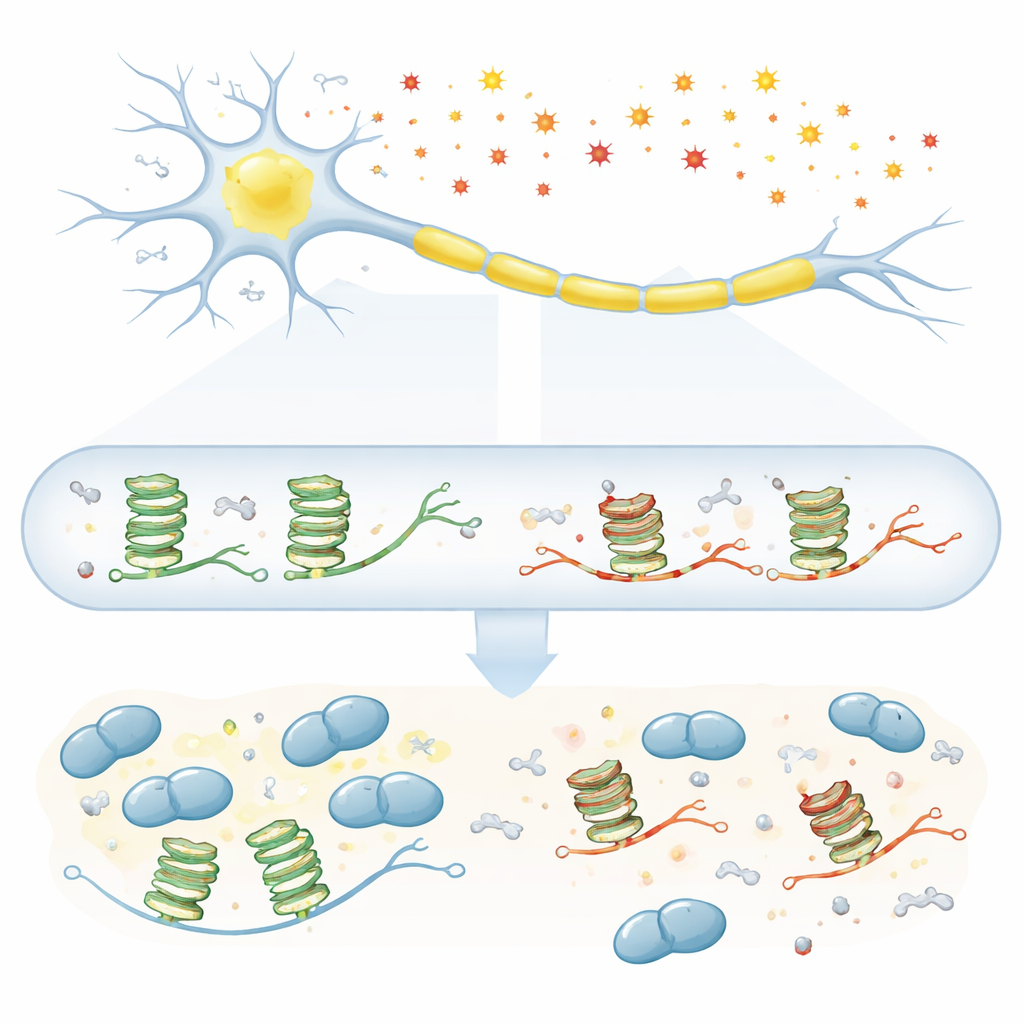
Un nudo de ARN frágil en el corazón de las motoneuronas
Las motoneuronas dependen del envío de mensajes de ARN a larga distancia a lo largo de sus axones para que las proteínas se sinteticen in situ, cerca de las conexiones con el músculo. Muchos de estos mensajes contienen un “nudo” estructural especial llamado G-cuádruplex, formado por tramos de la base guanina. Proteínas como TDP-43 reconocen este nudo y enganchan el ARN a gránulos de transporte que se desplazan por el axón. El problema es que la guanina también es la base más fácil de oxidarse cuando las células sufren estrés por especies reactivas de oxígeno, que se acumulan con la edad. Pistas previas sugerían que los G-cuádruplex y TDP-43 son centrales en la ELA, pero no estaba claro cómo la oxidación de estos nudos de ARN podría interferir con su asociación.
Observando cómo el estrés oxidativo deforma las formas del ARN
Los investigadores expusieron primero células de neuroblastoma humano a peróxido de hidrógeno, un agente oxidante común, y luego examinaron el estado de las estructuras en G-cuádruplex. Las señales de una sonda sensible a G-cuádruplex disminuyeron a medida que aumentó el estrés oxidativo, lo que indica que estos compactos nudos de ARN estaban perdiendo su forma normal. Para precisar la química, el equipo construyó ARN sintéticos que forman G-cuádruplex y deliberadamente incorporó cantidades variables de 8-oxoguanina, una forma oxidada conocida de la guanina encontrada en neuronas envejecidas y en tejidos de ELA. Usando un conjunto de herramientas biofísicas, mostraron que incluso niveles modestos de esta modificación aflojan el apilamiento ordenado del G-cuádruplex, aunque el resultado exacto depende de la secuencia de ARN circundante. 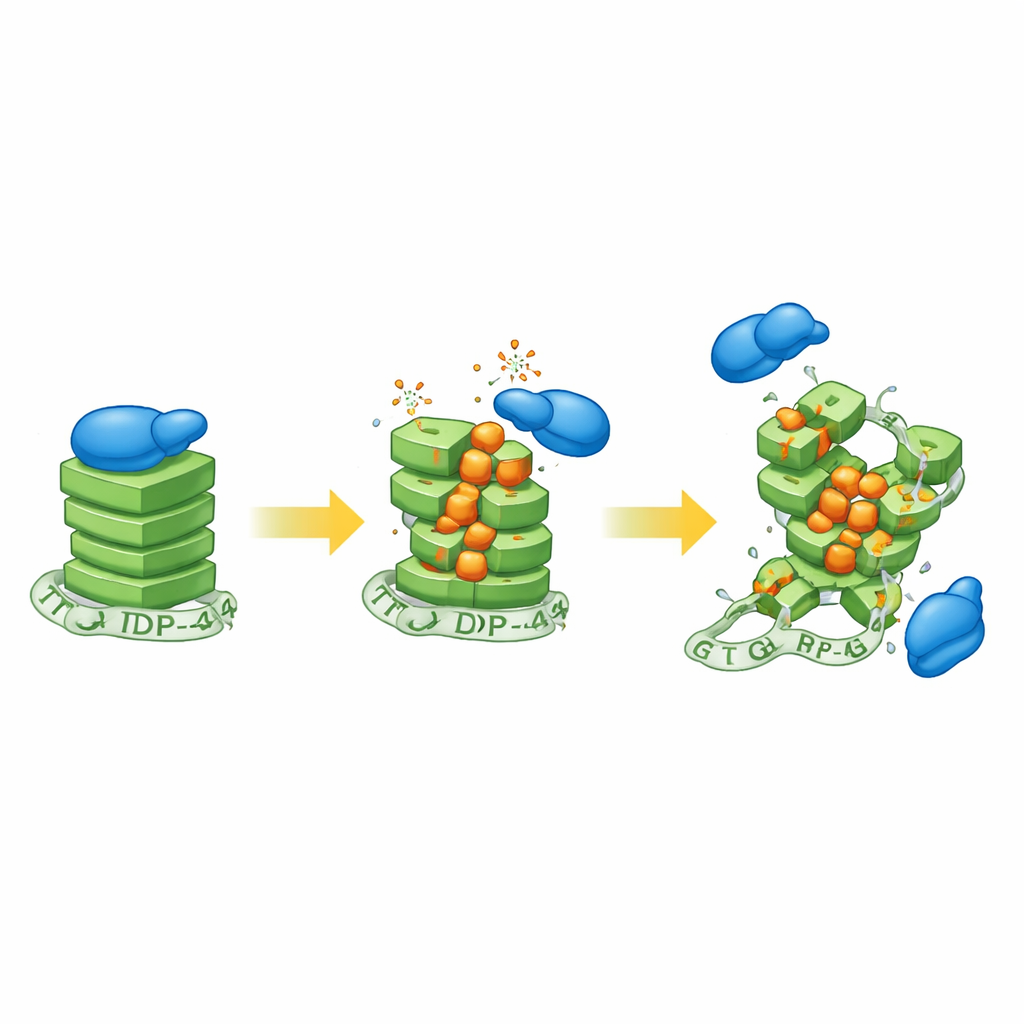
Nuevas fallas: bases desajustadas y cadenas mal apareadas
Un análisis más detallado reveló dos tipos distintos de problemas estructurales. En un G-cuádruplex derivado del mensajero PSD-95, las guaninas oxidadas tendían a aparearse de forma inapropiada con adeninas cercanas, formando “desajustes” que deforman sutilmente el pliegue. Estos desajustes aparecían más fácilmente en niveles intermedios de oxidación, cuando el ARN aún podía ensamblarse de forma transitoria en un G-cuádruplex que ponía en contacto a los socios equivocados. En otro G-cuádruplex proveniente del mensajero CaMKIIα, la oxidación intensa desestabilizó el nudo intramolecular habitual con tal fuerza que las guaninas intactas restantes buscaron parejas en otras hebras de ARN, promoviendo G-cuádruplex intermoleculares anómalos. Tales estructuras mal conectadas podrían enredar distintos ARN entre sí e interferir con el tráfico normal de ARN dentro de las neuronas.
Cuando el ARN dañado pierde a su proteína compañera
El estudio preguntó entonces cómo interactúan estos nudos distorsionados con TDP-43. Usando ensayos de unión basados en geles, los investigadores mostraron que TDP-43 prefiere con fuerza los G-cuádruplex intactos y paralelos y que cada vez pierde capacidad de unión a medida que se introducen más bases oxidadas. La estructura de CaMKIIα, ya muy compacta, resultó especialmente sensible: incluso baja oxidación casi abolió la unión de TDP-43. Una segunda proteína, FUS —también vinculada a la ELA— mostró una pérdida de afinidad similar pero algo menos severa, lo que sugiere que la oxidación debilita en general la unión de las proteínas que reconocen G-cuádruplex. De forma intrigante, cuando TDP-43 se mezcló con ARN levemente oxidado, las evidencias indicaron que la proteína interactuaba con una forma intermedia inestable del G-cuádruplex más que con un nudo completamente plegado, lo que sugiere una lucha dinámica entre estabilización y descomposición.
Vulnerabilidad extra en proteínas mutantes vinculadas a la ELA
El trabajo examinó además diez variantes de TDP-43 encontradas en pacientes con ELA, la mayoría con cambios en una cola flexible rica en glicina que ajusta el reconocimiento del ARN. Todas estas variantes ya se unían a G-cuádruplex normales con menos fuerza que la proteína de tipo salvaje. Cuando se introdujeron ARN G-cuádruplex oxidados como competidores, las variantes fueron aún menos capaces que la proteína normal de reconocer y unirse a las estructuras dañadas. Algunas variantes localizadas en regiones particularmente propensas al desorden fueron las más afectadas. Esto sugiere un doble golpe en personas de edad avanzada portadoras de tales mutaciones: no solo su TDP-43 es intrínsecamente menos eficaz, sino que la oxidación del ARN relacionada con la edad erosiona aún más su capacidad para escoltar mensajes cruciales a lo largo de los axones de las motoneuronas.
Qué significa esto para entender la ELA
En términos sencillos, este estudio muestra que el daño químico impulsado por la edad remodela delicados nudos de ARN que guían el transporte de mensajes en las motoneuronas, y estos nudos deformados ya no cooperan bien con TDP-43 ni con proteínas relacionadas. El resultado es una mayor probabilidad de carga de ARN mal dirigida o atascada, precisamente en los axones largos y vulnerables que mantienen el control muscular. Para las personas que además heredan mutaciones en TDP-43, este debilitamiento de las interacciones ARN–proteína inducido por la oxidación puede empujar a neuronas ya estresadas más cerca del colapso. Al iluminar esta cadena de eventos sutil pero potente —del estrés oxidativo a la alteración de la arquitectura del ARN y al transporte perturbado— el trabajo destaca la oxidación de ARN en G-cuádruplex como un vínculo molecular prometedor entre el envejecimiento y la ELA, y como un posible objetivo para futuras terapias protectoras.
Cita: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Palabras clave: esclerosis lateral amiotrófica, oxidación del ARN, G-cuádruplex, TDP-43, degeneración de motoneuronas