Clear Sky Science · es
Identificación de biomarcadores relacionados con la lesión de la barrera hematoencefálica en el infarto cerebral mediante análisis transcriptómico
Por qué esto importa para el ictus y la salud cerebral
Cuando alguien sufre un ictus por la obstrucción de un vaso sanguíneo en el cerebro, los médicos pueden ver el daño en las pruebas por imagen pero aún les cuesta predecir quién desarrollará hinchazón creciente, hemorragia o discapacidad a largo plazo. Gran parte de ese daño ocurre en el guardián protector del cerebro, la barrera hematoencefálica, que normalmente impide que sustancias nocivas de la sangre se filtren al delicado tejido nervioso. Este estudio planteó una pregunta simple pero importante: ¿existen señales moleculares características que indiquen cuándo esta barrera se está deteriorando, y podrían esas señales en el futuro orientar un mejor diagnóstico y tratamiento para los pacientes con ictus?
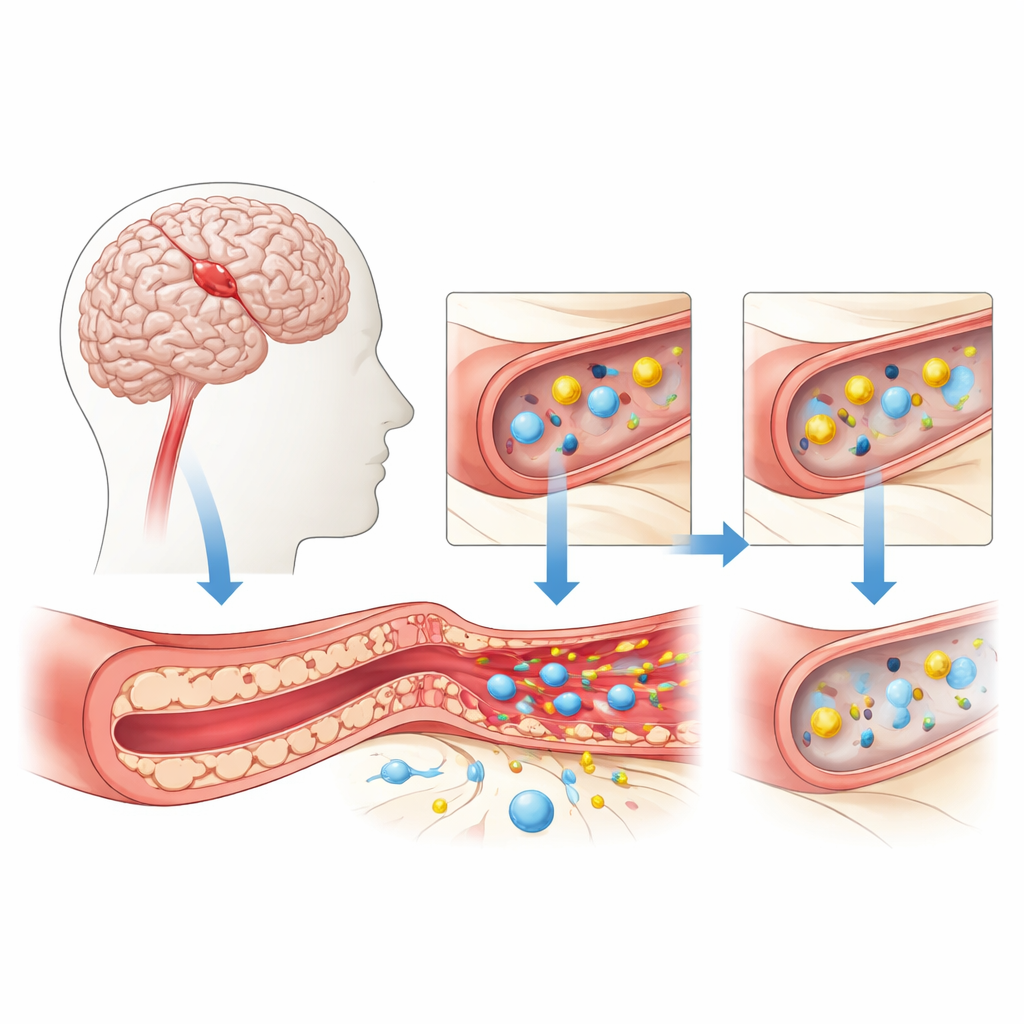
La puerta protectora del cerebro bajo estrés
La barrera hematoencefálica está formada por células muy juntas que recubren los pequeños vasos sanguíneos cerebrales. Estas células controlan con precisión lo que puede pasar de la sangre al cerebro, dejando entrar nutrientes vitales como oxígeno y glucosa y bloqueando toxinas y células inmunitarias que podrían causar daño. Durante un infarto cerebral, o ictus isquémico, el flujo sanguíneo cae de forma abrupta. Sin suficiente oxígeno y glucosa, las células que recubren los vasos se estresan y comienzan a perder su sello hermético. Se abren huecos entre ellas, el líquido se filtra al tejido circundante y mensajeros químicos de la inflamación inundan la zona, todo lo cual puede agravar la hinchazón y la lesión cerebral.
Recrear el daño por ictus en el laboratorio
Para estudiar lo que ocurre dentro de estas células de la barrera, los investigadores utilizaron una línea celular humana bien conocida que imita el revestimiento de los vasos cerebrales. Expusieron estas células a un ambiente con bajo oxígeno y sin glucosa —llamado privación de oxígeno y glucosa— para imitar las condiciones de un ictus, y luego restauraron las condiciones normales para simular el tratamiento y la recuperación. Midieron qué tan bien sobrevivían las células, cuánto se filtraba una enzima indicadora de daño celular y cuántas moléculas inflamatorias liberaban. Como era de esperar, el tratamiento estresante redujo la salud celular, aumentó señales inflamatorias como IL-1β, IL-6 y TNF-α, y elevó la filtración de un marcador de daño llamado LDH. Cuando se restauraron el oxígeno y los nutrientes, muchos de estos cambios perjudiciales se atenuaron y las células recuperaron parte de su capacidad para formar estructuras semejantes a vasos en una prueba de crecimiento.
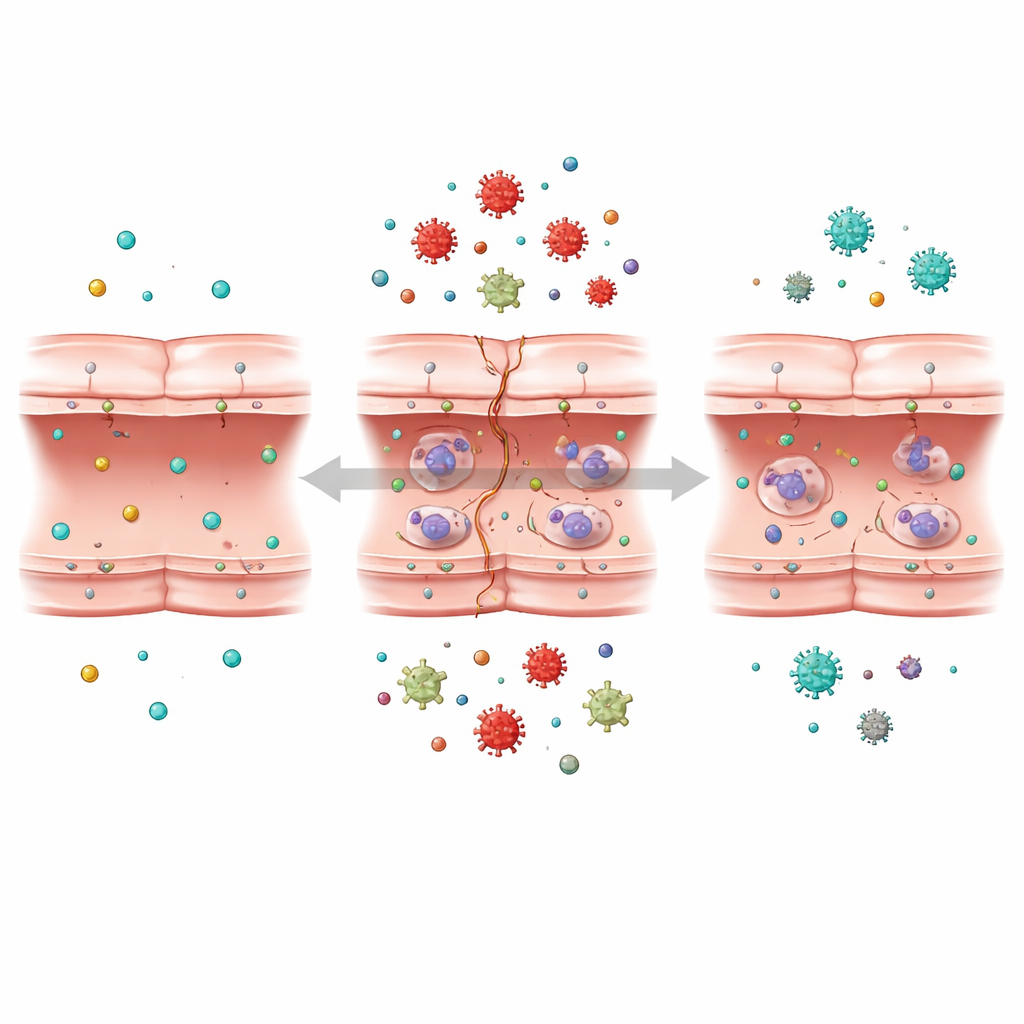
Escuchando la conversación molecular de la célula
El equipo recurrió entonces a una técnica potente conocida como transcriptómica, que registra los niveles de actividad de miles de genes a la vez. Comparando células normales, células sometidas a privación de oxígeno y glucosa y células permitidas a recuperarse, identificaron más de mil genes cuya actividad cambió en respuesta al estrés similar al ictus. Con herramientas de análisis avanzadas y aprendizaje automático, agruparon genes con comportamientos similares y buscaron aquellos más estrechamente asociados con la lesión de la barrera. Hallaron que muchos de los genes más afectados estaban vinculados a tres estructuras clave dentro de la célula: el ribosoma, que sintetiza proteínas; el retículo endoplásmico, que ayuda a plegarlas y procesarlas; y las mitocondrias, las pequeñas centrales energéticas que suministran energía.
Los ribosomas emergen como señales indicadoras
A partir de este gran conjunto de genes, los investigadores utilizaron un algoritmo de random forest —un tipo de aprendizaje automático basado en árboles de decisión— para reducir la lista a un pequeño grupo de genes especialmente informativos. Luego mapearon cómo interactúan las proteínas correspondientes entre sí. Este análisis destacó seis genes centrales, la mayoría relacionados con el ribosoma, la fábrica de proteínas de la célula. En la condición similar al ictus, estos genes vinculados al ribosoma mostraron una mayor activación, mientras que su actividad volvió hacia niveles normales cuando se restauraron el oxígeno y la glucosa. Este patrón sugiere que los cambios en la maquinaria de producción de proteínas de la célula pueden ser una señal temprana y sensible de daño y recuperación de la barrera hematoencefálica.
Qué podría significar esto para la atención futura
Para un lector no especializado, la conclusión es que este estudio señala una nueva clase de “luces de advertencia” moleculares que se encienden cuando la barrera protectora del cerebro resulta dañada durante un ictus. En lugar de centrarse únicamente en culpables bien conocidos, como enzimas que degradan la pared del vaso, el trabajo muestra que las propias fábricas de proteínas celulares responden fuertemente al daño y se calman cuando mejoran las condiciones. Si investigaciones futuras confirman que estos marcadores relacionados con los ribosomas pueden detectarse en muestras de pacientes, como la sangre, los médicos podrían algún día utilizarlos para valorar cuánto se ha dañado la barrera, para cronometrar tratamientos que reduzcan la inflamación y la hinchazón, y para probar nuevos fármacos destinados a preservar a este crucial guardián de la salud cerebral.
Cita: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Palabras clave: ictus isquémico, barrera hematoencefálica, biomarcadores, genes ribosómicos, células endoteliales