Clear Sky Science · es
La colonización bacteriana de los tumores impulsa la activación inmune y la eficacia del bloqueo de puntos de control
Por qué importan los pequeños inquilinos en los tumores
El tratamiento del cáncer se ha transformado con inmunoterapias que liberan a las células inmunitarias del propio organismo contra los tumores. Sin embargo, muchos pacientes siguen obteniendo pocos beneficios y ha sido difícil predecir quién responderá. Este estudio explora a un jugador inesperado que puede inclinar la balanza: las bacterias que viven dentro de los propios tumores. Al examinar modelos de cáncer en ratón, los investigadores muestran que estos inquilinos microscópicos pueden cambiar el comportamiento del sistema inmunitario dentro y alrededor de un tumor y, a su vez, ayudar a determinar si una inmunoterapia ampliamente usada llamada anti–PD-1 funciona bien o fracasa.
Bacterias ocultas dentro de los tumores
Durante años, la mayor atención se centró en los trillones de microbios en el intestino y en cómo moldean la inmunidad global. Más recientemente, los científicos han descubierto que muchos tumores humanos también albergan comunidades bacterianas pequeñas pero activas. El equipo detrás de este estudio planteó dos preguntas básicas: ¿los modelos tumorales de uso común en ratón también contienen bacterias y, de ser así, influyen realmente en el crecimiento del tumor y en la respuesta al tratamiento? Compararon dos modelos: MCA-205, un tipo de sarcoma, y MOC1, un modelo de cáncer de cabeza y cuello. Mediante pruebas basadas en ADN, secuenciación y métodos de cultivo, encontraron que los tumores MCA-205 llevaban consistentemente bacterias vivas, mientras que los tumores MOC1 no, incluso cuando se ubicaban en la boca, rica en bacterias. En MCA-205, los niveles bacterianos tendían a aumentar a medida que los tumores crecían, lo que sugiere que el tumor en expansión ofrecía un nicho favorable para los microbios.
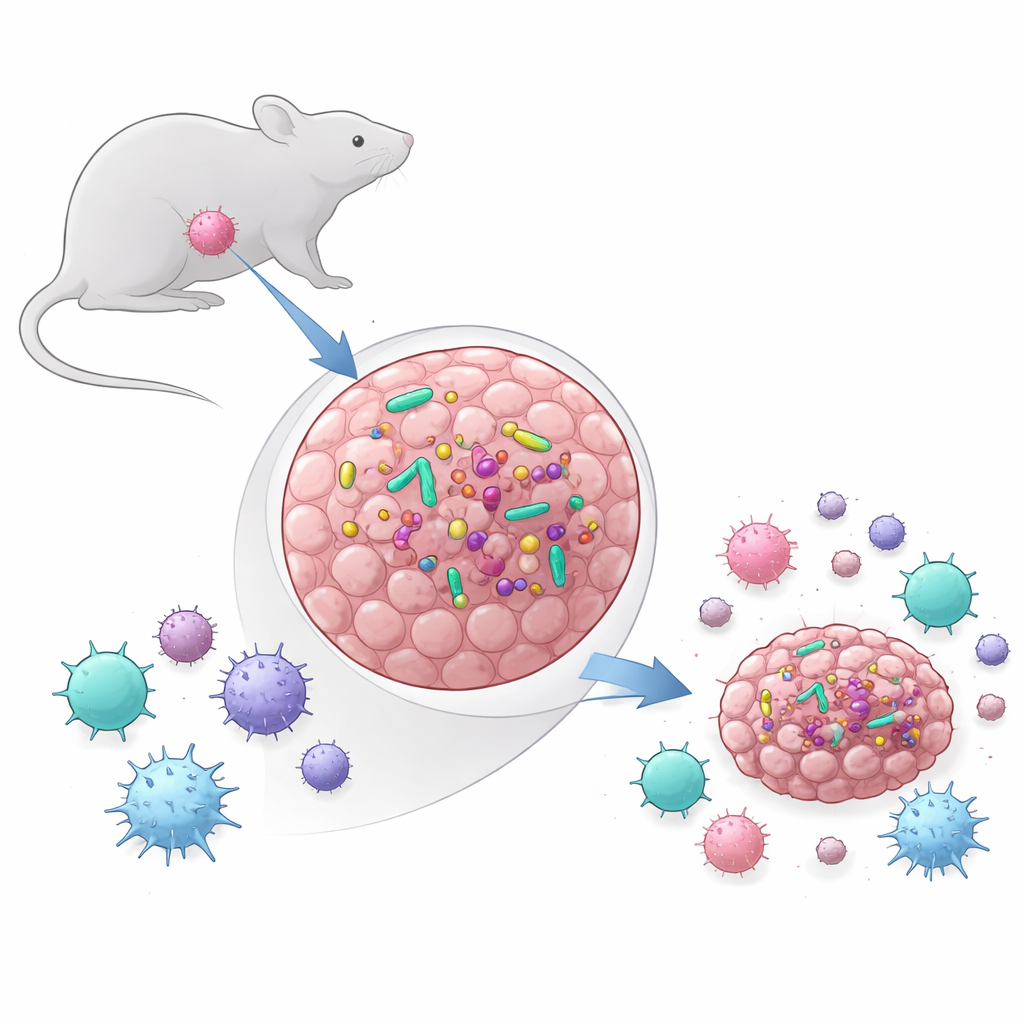
Rastreando el origen de los microbios
Encontrar bacterias dentro de los tumores planteó otra cuestión: ¿provienen estos invasores de la piel, de la boca o del intestino? Al comparar el ADN bacteriano de los tumores con muestras de heces, frotis cutáneos y frotis orales, los investigadores hallaron que la comunidad intratumoral era más simple y menos diversa que los ricos ecosistemas del intestino y la boca. La mayoría de los tipos bacterianos en los tumores coincidían con los observados en el tracto gastrointestinal, mientras que relativamente pocos coincidian con la piel. Esto sugiere que las bacterias pueden filtrarse desde el intestino o la cavidad oral hacia el torrente sanguíneo y luego sembrar el tumor, donde solo ciertas especies logran persistir. La mezcla de grupos bacterianos reflejaba la observada en varios cánceres humanos, reforzando la idea de que estos tumores de ratón pueden modelar las interacciones reales entre tumores y microbios.
Cómo las bacterias tumorales configuran el éxito de la inmunoterapia
El hallazgo central del estudio es que las bacterias que habitan el tumor pueden determinar el éxito o fracaso de la terapia anti–PD-1, un inhibidor de puntos de control diseñado para reactivar las células T citotóxicas agotadas. Cuando el equipo usó antibióticos capaces de penetrar el tumor y erradicar las bacterias locales mientras preservaban en gran medida la colonización intestinal, los tumores MCA-205 se volvieron mucho menos sensibles al anti–PD-1. Las respuestas cayeron aún más cuando la microbiota intestinal se vio ampliamente alterada. En contraste, en los tumores MOC1 que carecían de bacterias detectables desde el principio, los antibióticos tuvieron poco efecto ni sobre la carga bacteriana ni sobre el resultado del tratamiento. En MCA-205, los tumores que se redujeron en respuesta al anti–PD-1 tendían a contener más bacterias que los que resistieron la terapia, vinculando una alta carga bacteriana intratumoral con un mejor control del crecimiento.
Dentro del frente de batalla inmunitario
Para comprender cómo las bacterias inclinan el equilibrio inmunitario, los investigadores examinaron las células inmunes dentro y alrededor de los tumores. Cuando las bacterias intratumorales se eliminaron con antibióticos que penetraban el tumor, menos células T CD8 citotóxicas infiltraron el tumor, y la proporción de estas células frente a las células T reguladoras se desplazó hacia la supresión. Las células dendríticas, los centinelas que toman material tumoral y activan las células T, también disminuyeron en número y mostraron menores signos de activación cuando las bacterias estaban ausentes. Curiosamente, añadir simplemente una cepa extra de E. coli inofensiva en el tumor, o desactivar una vía principal de detección microbiana (MyD88) en células inmunes clave, no potenció la terapia. Esto implica que no basta con cualquier presencia bacteriana o con una señal de alarma simple; probablemente se requieren comunidades específicas y una comunicación más matizada con el sistema inmunitario.
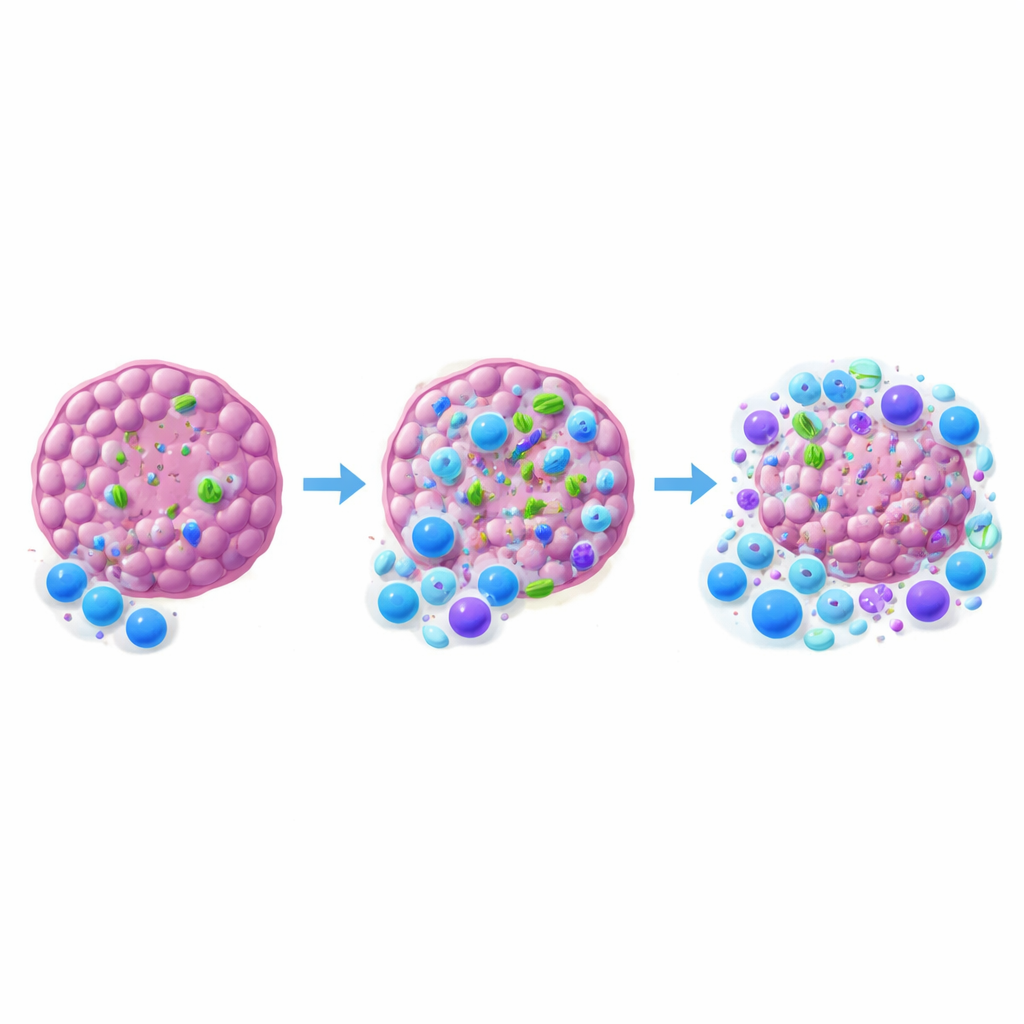
Qué significa esto para la atención del cáncer futura
Para un público no especialista, la conclusión es que las bacterias que viven dentro de los tumores no son meros espectadores. En al menos algunos tipos de cáncer, ayudan a reunir las células inmunitarias adecuadas en el tumor y a apoyar la acción de los fármacos anti–PD-1. Otros tumores pueden permanecer casi libres de bacterias y responder de manera muy diferente. A medida que los científicos diseñen y prueben nuevos tratamientos en ratones, saber si un modelo tumoral determinado alberga bacterias —y cuáles— puede ser esencial para interpretar resultados y elegir estrategias que se traduzcan en los pacientes. A largo plazo, ajustar con cuidado las pequeñas comunidades dentro de los tumores podría sumarse a los fármacos y a las células inmunitarias como una nueva herramienta para mejorar la inmunoterapia contra el cáncer.
Cita: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Palabras clave: microbiota intratumoral, inmunoterapia contra el cáncer, anti-PD-1, microambiente tumoral, bacterias y tumores