Clear Sky Science · es
Redundancia críptica entre PAR1b y PAR1a, dos miembros de la familia de quinasas PAR1, en la supervivencia de ratones con eliminación de PAR1b
Cómo las células encuentran planes de respaldo para el ADN dañado
Nuestras células afrontan constantemente daños en su ADN y, cuando los sistemas de reparación fallan, el resultado puede ser cáncer o la muerte durante el desarrollo. Este estudio explora un mecanismo de rescate sorprendente en ratones: cuando falta una proteína clave que ayuda al famoso gen relacionado con el cáncer BRCA1 a realizar su función, un pariente cercano interviene silenciosamente. El trabajo revela cómo los embriones tempranos pueden reconfigurar sus sistemas de control genético para sobrevivir, ofreciendo una nueva perspectiva sobre por qué algunos defectos genéticos son letales mientras que otros se toleran inesperadamente.
Una familia de organizadores celulares con un papel oculto
Los investigadores se centraron en una familia de enzimas llamadas quinasas PAR1, que ayudan a las células a mantener su organización interna. Un miembro de la familia, PAR1b, se había mostrado previamente como guía de BRCA1 hacia el núcleo celular, donde BRCA1 supervisa la reparación precisa del ADN y protege sitios de replicación frágiles. Eliminando BRCA1 por completo en ratones resulta letal en etapas tempranas del desarrollo embrionario, lo que subraya su importancia. Sin embargo, de manera enigmática, los ratones que carecen por completo de PAR1b sobreviven hasta la edad adulta, pese a que PAR1b actúa aguas arriba de BRCA1. Esta discrepancia sugirió que otra quinasa PAR1 podría sustituir silenciosamente a PAR1b en determinadas condiciones.
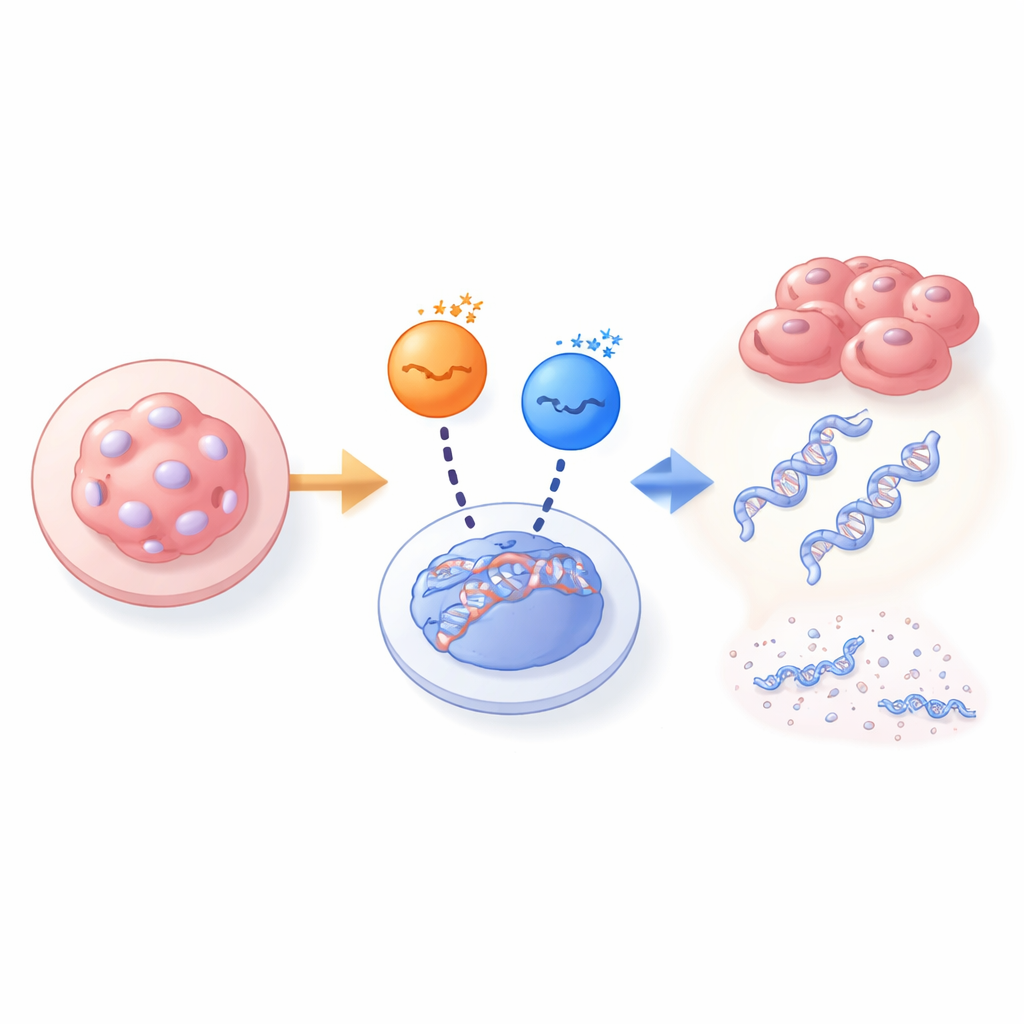
Cuando una quinasa falla, otra toma el relevo
Para indagar este misterio, el equipo comparó fibroblastos embrionarios de ratón procedentes de embriones normales con los de embriones que carecían completamente de PAR1b. En células normales, inhibir PAR1b reducía drásticamente BRCA1 dentro del núcleo y provocaba un aumento de marcadores de rotura del ADN, lo que a su vez bloqueaba el crecimiento celular. La reducción de otras quinasas PAR1 (PAR1a, PAR1c, PAR1d) tuvo poco efecto. Sin embargo, en células derivadas de embriones sin PAR1b, BRCA1 seguía presente en el núcleo y el ADN permanecía relativamente intacto, a pesar de la ausencia de PAR1b. En estas células nulas para PAR1b, eliminar PAR1a se volvió letal, mientras que eliminar PAR1c o PAR1d no lo fue. Este cambio en la dependencia mostró que PAR1a había asumido el papel de PAR1b para guiar a BRCA1, pero solo en embriones que habían carecido de PAR1b desde el principio.
Reconfiguración epigenética temprana como estrategia de supervivencia
Los investigadores sospecharon que este sistema de respaldo oculto estaba ligado a la epigenética: la forma en que el ADN se empaqueta y se marca químicamente para activar o silenciar genes sin cambiar el código genético. Usando una técnica genómica para explorar la accesibilidad de la cromatina, encontraron miles de regiones donde la accesibilidad del ADN difería entre las células normales y las nulas para PAR1b. Muchos cambios afectaban a genes que controlan cómo se envuelven y modifican los cromosomas, lo que sugiere una reprogramación amplia de la red de control génico. Un efecto destacado afectó al gen 53BP1, una proteína que normalmente empuja a las células hacia una forma rápida y aproximada de reparación del ADN que se opone al método más preciso de BRCA1. En las células nulas para PAR1b, el cuerpo del gen 53BP1 estaba más compactado y sus niveles de ARN y proteína eran mucho más bajos.
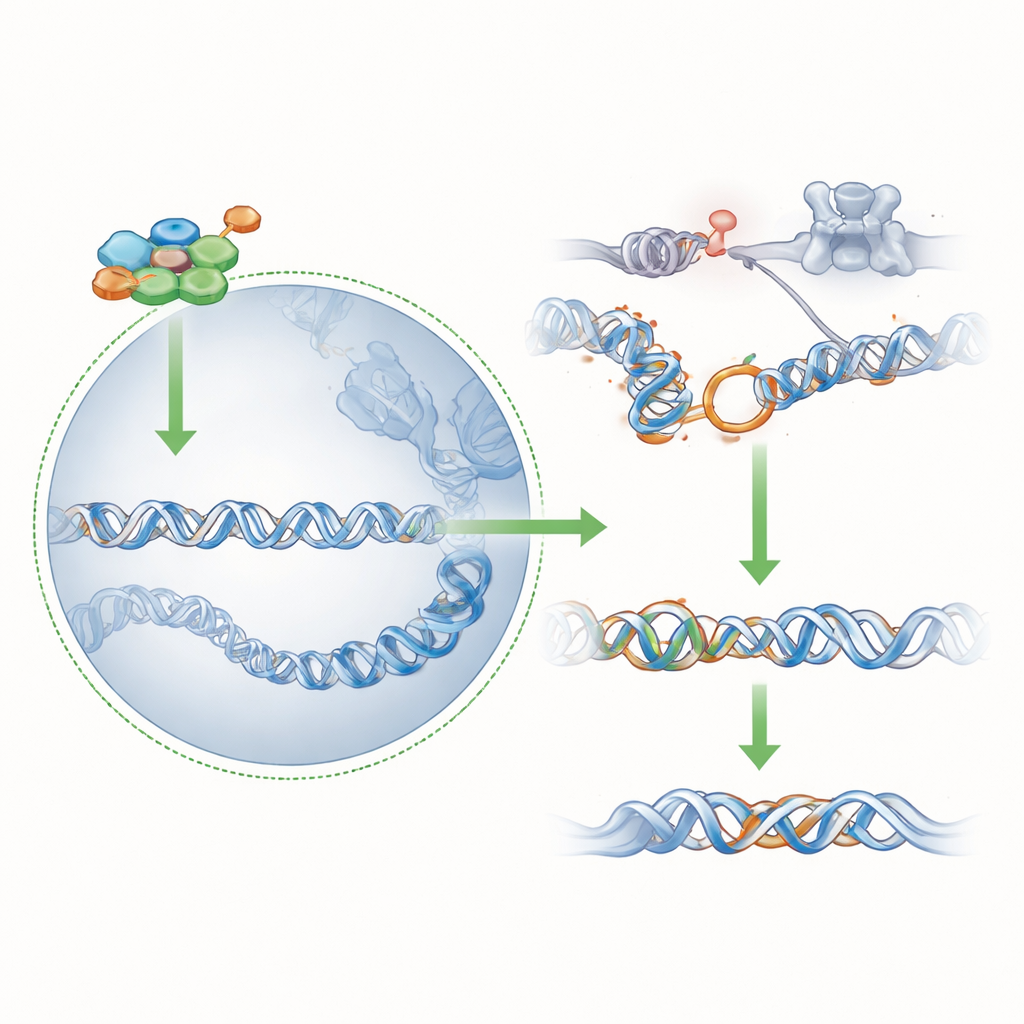
Inclinar la balanza entre vías de reparación
Al reducir 53BP1, el embrión reduce efectivamente su dependencia de la plena capacidad de BRCA1: incluso una cantidad modesta de BRCA1 nuclear, transportada por PAR1a en lugar de PAR1b, puede ahora sostener la reparación suficiente para mantener vivas a las células. Experimentos que emplearon una proteína bacteriana que apaga todas las quinasas PAR1 confirmaron que la presencia nuclear de BRCA1 en las células nulas para PAR1b sigue dependiendo de la actividad de la familia PAR1, concretamente de PAR1a. En conjunto, los resultados dibujan un panorama en el que la pérdida temprana de PAR1b desencadena un rápido remodelado de la cromatina y de las redes de reparación del ADN, silenciando a un oponente de BRCA1 (53BP1) y desenmascarando la capacidad de PAR1a para sustituir a PAR1b.
Qué significa esto para la enfermedad y el tratamiento
Este trabajo introduce la idea de la “redundancia críptica”: una función de respaldo que existe pero suele estar latente y solo se hace visible cuando un componente clave se pierde muy pronto en el desarrollo. En ratones, esto permite que los embriones sobrevivan a la pérdida de PAR1b, a diferencia de lo que ocurre con la pérdida de BRCA1. Los hallazgos también sugieren que algunas personas con variantes dañinas en PAR1b pueden sobrevivir porque mecanismos de respaldo similares se activan, aunque no sin posibles consecuencias para la función cerebral, el metabolismo o el riesgo de cáncer. A la larga, entender cómo los ajustes epigenéticos tempranos silencian 53BP1 y desplazan el control de BRCA1 de PAR1b a PAR1a podría inspirar estrategias para imitar deliberadamente estos cambios: bien para proteger células que han perdido PAR1b, bien para afinar las vías de reparación del ADN en la terapia contra el cáncer.
Cita: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Palabras clave: BRCA1, reparación del ADN, redundancia de quinasas, regulación epigenética, desarrollo embrionario