Clear Sky Science · es
La variante p.Arg676Cys de Sema5A asociada al trastorno del espectro autista activa señalización Arf6/FE65 y conduce a morfogénesis celular aberrante
Cómo un pequeño cambio puede alterar el cableado cerebral
El trastorno del espectro autista afecta la forma en que las personas se comunican, interactúan y responden al mundo que les rodea, pero los pasos biológicos que llevan de un cambio en el ADN a una función cerebral alterada suelen ser enigmáticos. Este estudio investiga uno de esos cambios genéticos en una proteína guía cerebral llamada Sema5A y muestra, con un detalle inusualmente fino, cómo un solo bloque de construcción intercambiado en esa proteína puede impulsar a las neuronas jóvenes a desarrollar ramas excesivamente largas y enredadas. Entender este error microscópico en el cableado podría ayudar a los científicos a diseñar tratamientos que orienten a las células cerebrales hacia una forma más saludable.
Células cerebrales que crecen demasiado
Durante el desarrollo cerebral, las neuronas jóvenes envían largas y delgadas extensiones que buscan los socios adecuados, formando los circuitos que sustentan el pensamiento y el comportamiento. Este crecimiento debe estar muy controlado: si hay pocas ramificaciones, las células no conectan; si hay demasiadas, los circuitos pueden volverse ruidosos o estar mal cableados. Trabajos previos habían mostrado que una versión de Sema5A ligada al autismo, en la que un aminoácido en la posición 676 cambia de arginina a cisteína, hace que las neuronas en cultivo desarrollen procesos inusualmente largos. El nuevo estudio se propuso descubrir qué interruptores y proteínas auxiliares internas usa esta Sema5A mutante para impulsar ese crecimiento descontrolado.
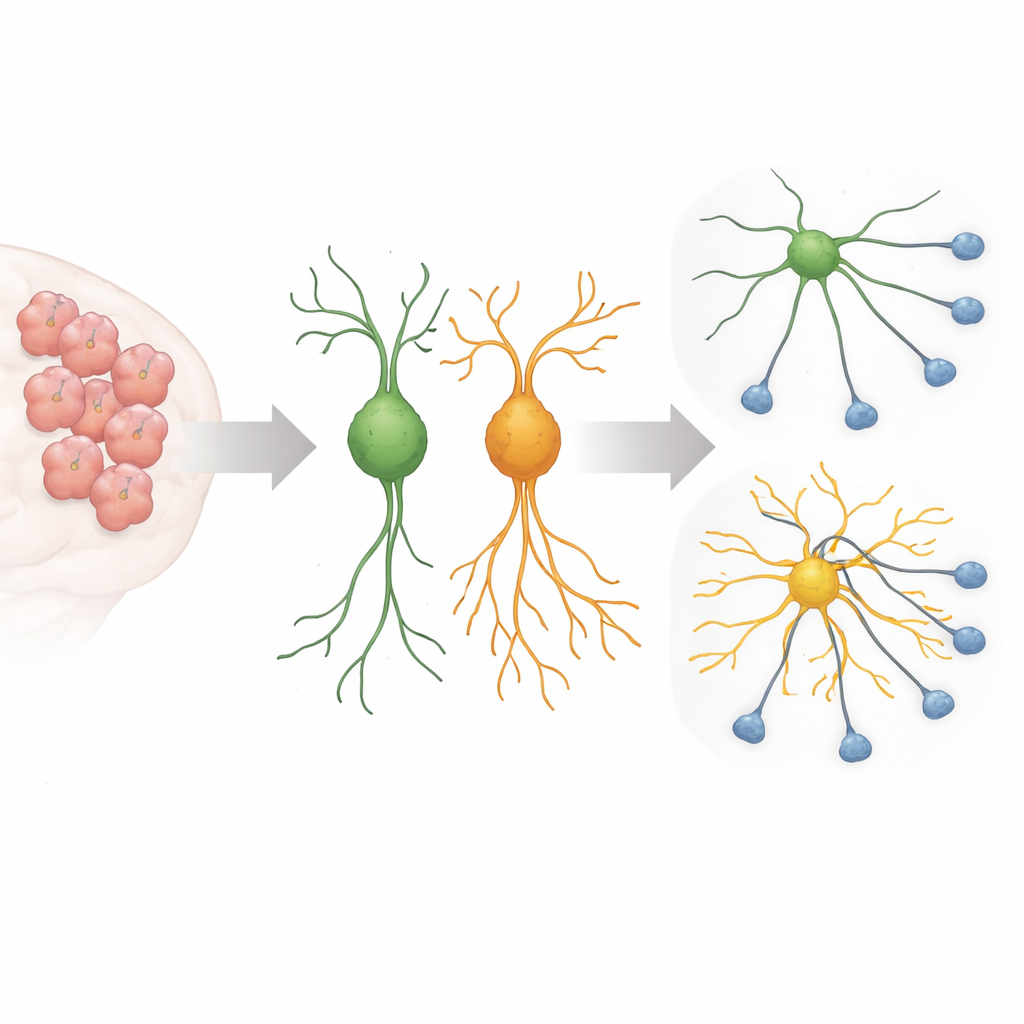
Una señal engañosa dentro de la célula
Los investigadores se centraron en un pequeño interruptor molecular llamado Arf6 y en una proteína andamiaje llamada FE65, ambos conocidos por ayudar a moldear las membranas celulares y el esqueleto interno que sostiene las extensiones celulares. Usando un sistema CRISPR–Cas13 para reducir selectivamente estas proteínas en células tipo neuronal de ratón y en células cerebrales primarias de ratón, encontraron que disminuir Arf6 o FE65 reducía drásticamente el crecimiento excesivo causado por la Sema5A mutante. Los procesos largos y arácnidos se acortaron hacia longitudes más típicas, y los marcadores de maduración neuronal bajaron, lo que sugiere que el efecto de la mutación depende en gran medida de esta vía de señalización en particular.
Conexión con el motor de la forma celular
Dentro de las neuronas, una familia de moléculas actúa como un "motor" de la forma controlando la actina, el filamento estructural principal en las ramas celulares. Un miembro clave de esta familia, Rac1, normalmente se activa para ayudar a extender los neuritos, pero una actividad excesiva puede impulsar un crecimiento descontrolado. El equipo mostró que en células con Sema5A normal, Arf6 es necesario para la activación ordinaria de Rac1 durante el crecimiento sano, mientras que FE65 no es esencial. Con la Sema5A mutante, sin embargo, tanto Arf6 como FE65 se volvieron críticos: reducir cualquiera de los dos, o saturar la célula con la región de FE65 que se une a su pareja ELMO2, redujo la actividad anormalmente alta de Rac1 hacia niveles normales. Esto implica que la versión dañina de Sema5A explota específicamente un complejo Arf6–FE65–ELMO2–DOCK5 para sobreestimular a Rac1 y forzar a los neuritos a crecer en exceso.
Un centro concurrido de socios de señalización
Para ver cómo encajan estas piezas, los científicos también examinaron los "señalosomas" basados en ELMO2: agrupaciones de proteínas que se ensamblan para transmitir señales de crecimiento. Cuando se redujo Arf6 o FE65, las células que expresaban la Sema5A mutante formaron menos de estos complejos ELMO2 en sus cuerpos y en las puntas en crecimiento, coherente con la idea de que Arf6 y FE65 ayudan a construir la maquinaria que convierte la mutación de Sema5A en un cambio físico en la forma celular. El trabajo encaja en una imagen más amplia en la que pequeños interruptores moleculares como Arf6 y Rac1, ayudados por andamios como FE65, actúan como centros neurálgicos que vinculan muchos genes asociados al autismo con la arquitectura final de los circuitos cerebrales.
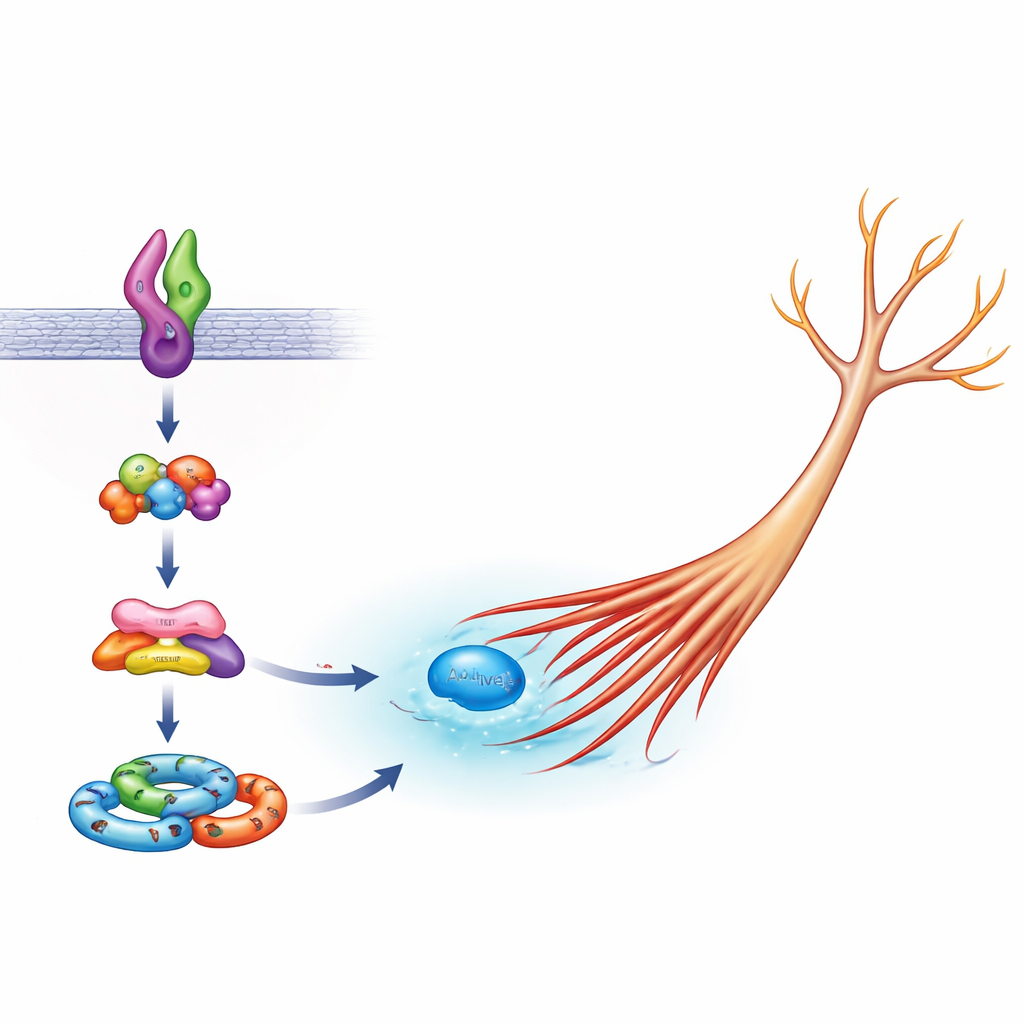
Por qué importa esta cadena microscópica
Para un no especialista, la sopa de letras de nombres de proteínas puede parecer alejada de la experiencia vivida del autismo. Sin embargo, este estudio ofrece un puente concreto: traza cómo un cambio genético preciso en Sema5A puede sobreactivar una cadena específica de moléculas auxiliares, causando que las neuronas extiendan sus ramas demasiado y, potencialmente, cableen el cerebro de maneras atípicas. Al identificar a Arf6, FE65 y el complejo señal ELMO2 como eslabones cruciales en esta cadena, el trabajo destaca posibles dianas farmacológicas futuras. En principio, fármacos que ajusten suavemente a la baja esta vía sobreactivada podrían algún día ayudar a corregir los cambios subyacentes en la forma celular asociados a formas de autismo relacionadas con Sema5A, aportando una pieza importante al rompecabezas más amplio de los trastornos del neurodesarrollo.
Cita: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Palabras clave: trastorno del espectro autista, mutación Sema5A, morfogénesis neuronal, señalización Rac1, vía Arf6 FE65