Clear Sky Science · es
Efectos letales de las estructuras de la ivermectina sobre los vectores de la malaria y análisis in silico de las interacciones con sus canales iónicos de cloruro regulados por glutamato
Convertir un fármaco antiparasitario en un asesino de mosquitos
La ivermectina es más conocida como un medicamento contra gusanos parásitos en humanos y ganado, pero tiene un efecto secundario sorprendente: los mosquitos que se alimentan de sangre tratada con el fármaco a menudo mueren. Eso plantea una idea intrigante para el control de la malaria: ¿podría administrar ivermectina a personas o animales reducir lo suficiente las poblaciones locales de mosquitos como para cortar la transmisión? Este estudio profundiza en cómo la ivermectina y moléculas relacionadas matan a los mosquitos Anopheles que transmiten la malaria, y qué cambios podrían, algún día, permitir a los mosquitos escapar de sus efectos.
Por qué importa matar mosquitos a través de la sangre
El control tradicional de la malaria se basa en mosquiteros y pulverizaciones de insecticidas, que atacan a los mosquitos desde el exterior. La ivermectina ofrece una estrategia diferente: cuando humanos o animales toman el fármaco, su sangre se vuelve letal para los mosquitos hematófagos. Los investigadores se centraron en dos importantes vectores de malaria del sudeste asiático, Anopheles dirus y Anopheles minimus, que difieren mucho en la facilidad con la que la ivermectina los mata. Al comparar estas especies, el equipo buscó entender por qué el fármaco es más letal en algunos mosquitos que en otros y cómo la estructura química influye en ese efecto letal.
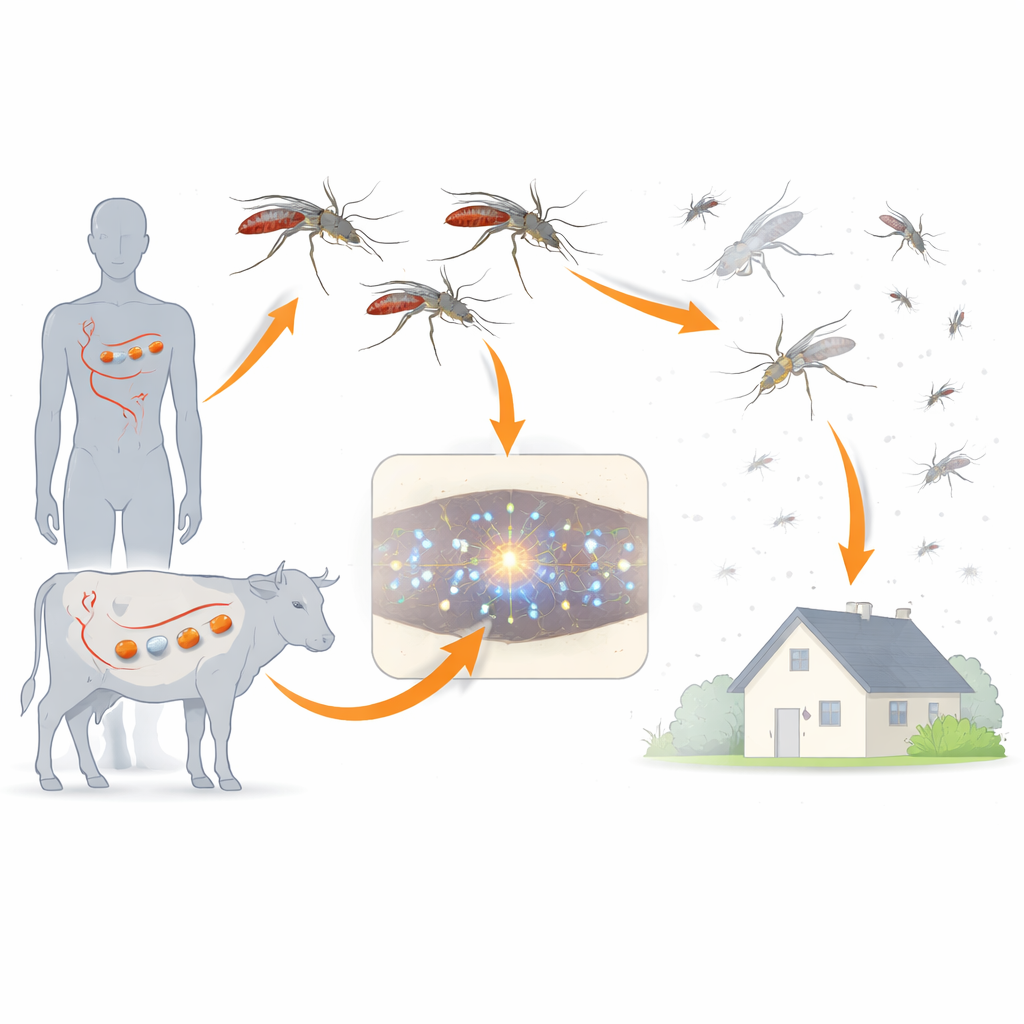
Probar qué partes del fármaco importan
La ivermectina es una molécula voluminosa construida alrededor de un anillo grande con dos anillos de azúcar unidos. El equipo comparó la ivermectina completa (con ambos azúcares) con una versión con un solo anillo de azúcar (llamada monosacárido) y con un núcleo despojado sin azúcares (aglicona). Alimentaron estos compuestos, a diferentes concentraciones, a miles de mosquitos en comidas sanguíneas y siguieron la supervivencia durante diez días. La ivermectina completa fue altamente letal, especialmente para An. minimus, mientras que el monosacárido fue mucho más débil y la aglicona tuvo casi ningún poder letal a dosis realistas. En otras palabras, retirar un anillo de azúcar convirtió un potente asesino de mosquitos en uno mucho más leve, y eliminar ambos borró casi por completo el efecto.
Echar un vistazo dentro de la puerta nerviosa del mosquito
La ivermectina actúa sobre una pequeña puerta en las células nerviosas y musculares llamada canal de cloruro regulado por glutamato (GluCl). Cuando esta puerta se fuerza a abrir, los iones de cloruro entran en masa, la actividad eléctrica colapsa y el mosquito queda paralizado y muere. Usando predicción avanzada de estructuras proteicas y acoplamiento por ordenador, los investigadores construyeron modelos tridimensionales del canal GluCl de Anopheles y simularon cómo la ivermectina y sus variantes encajan en el canal. Encontraron que, en los mosquitos, una parte específica del lazo proteico cerca del poro—que contiene un aminoácido llamado treonina en la posición 304—puede formar un enlace de hidrógeno con el segundo anillo de azúcar de la ivermectina. Este enlace, junto con atractivos débiles cercanos, parece estabilizar una conformación con el fármaco unido que mantiene el canal abierto.
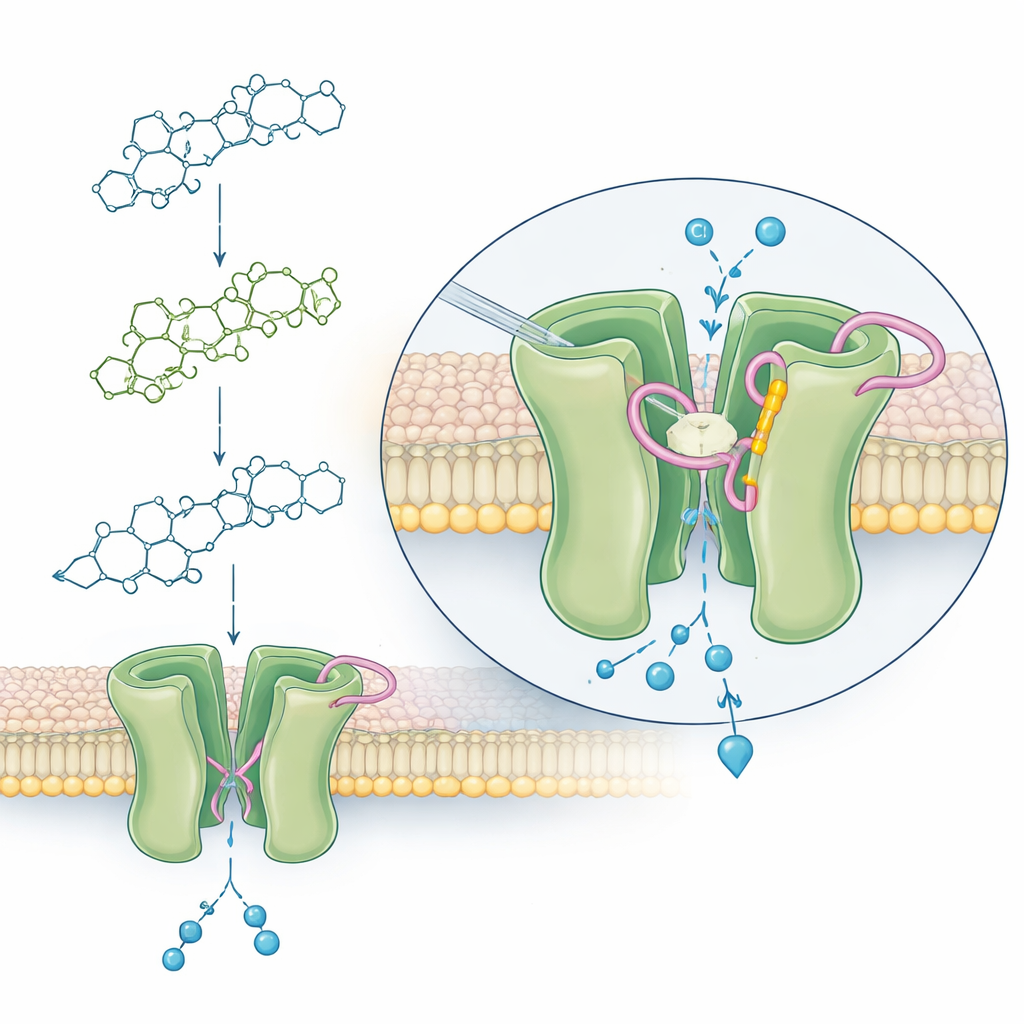
Por qué algunas versiones matan y otras no
Las simulaciones mostraron un patrón consistente: la ivermectina completa y tres productos principales de degradación de la ivermectina encontrados en humanos se introducen profundamente en el canal, permitiendo que su segundo anillo de azúcar interactúe estrechamente con el lazo clave. Estas formas generaron una unión predicha fuerte y, en trabajos anteriores, demostraron ser tan letales para los mosquitos como el fármaco original. El monosacárido, al carecer de ese segundo anillo, podía todavía tocar débilmente el lazo pero no podía formar el mismo enlace estabilizador, lo que coincide con su poder letal mucho menor. La aglicona no contactó el lazo en absoluto, alineándose con su incapacidad para matar mosquitos en las pruebas de alimentación. A través de todas las estructuras, surgió también como importante una interacción compartida con otra parte del canal (en la subunidad opuesta), lo que sugiere que varios puntos de contacto trabajan juntos para bloquear la puerta abierta.
Mirando hacia la resistencia y mejores herramientas
Los hallazgos sugieren que el segundo anillo de azúcar de la ivermectina—y su capacidad para unirse con un lazo específico del canal GluCl del mosquito—es fundamental para su efecto letal sobre los mosquitos. Esta imagen más detallada de cómo el fármaco encaja en el canal destaca puntos débiles potenciales donde futuras mutaciones podrían reducir la unión y conducir a la resistencia. También insinúa maneras en que los químicos podrían modificar moléculas similares a la ivermectina para mantener o mejorar su eficacia contra los mosquitos. Aunque el estudio se apoya en modelos por ordenador que aún requieren confirmación experimental, refuerza el caso de las estrategias basadas en ivermectina como parte de la caja de herramientas para el control de la malaria y señala características moleculares que será crucial vigilar conforme se implementen tales estrategias.
Cita: Nguyen, M.N., Jones, A.K., Hotwagner, D. et al. Lethal effects of ivermectin structures on malaria vectors and in silico analysis of interactions with their glutamate-gated chloride ion channels. Sci Rep 16, 8141 (2026). https://doi.org/10.1038/s41598-026-39698-8
Palabras clave: ivermectina, vectores de la malaria, mosquitos Anopheles, canales iónicos, resistencia a insecticidas