Clear Sky Science · es
Dirección de tipos neuronales específicos en el cerebro de primates no humanos mediante el uso de un inmunotoxina recombinante específica para CD25 murino
Por qué importa este estudio cerebral
Comprender cómo grupos específicos de células cerebrales controlan el movimiento, la emoción y el comportamiento es clave para tratar trastornos como la enfermedad de Parkinson y el autismo. Pero el cerebro es un denso bosque de células entrelazadas, y la mayoría de las herramientas derriban muchos árboles a la vez. Este estudio presenta una forma de eliminar solo un tipo concreto de neurona en el cerebro de un mono, con un daño colateral mínimo, abriendo la puerta a experimentos mucho más precisos sobre cómo circuitos particulares moldean el comportamiento y la enfermedad.
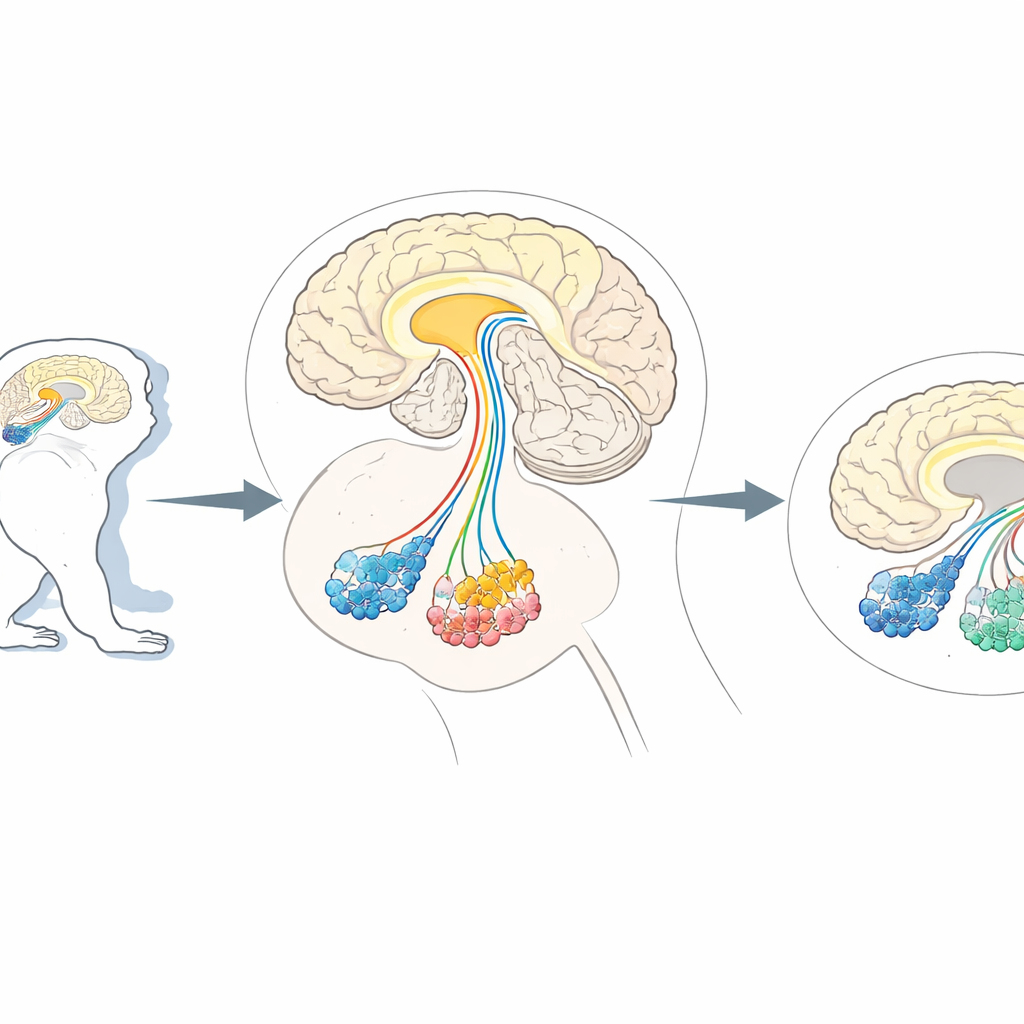
Necesidad de una "poda" celular cerebral precisa
Los investigadores a menudo recurren a primates no humanos, como marmosetos y macacos, porque sus cerebros están organizados de forma muy similar al nuestro. Estos animales son modelos invaluables para condiciones que afectan funciones cerebrales superiores, desde problemas de movimiento parkinsonianos hasta cambios en el comportamiento social similares al autismo. Los métodos existentes pueden silenciar o estimular vías específicas, pero realmente eliminar solo un tipo de neurona en estos cerebros complejos sin dañar a otras ha seguido siendo difícil. Trabajos anteriores en ratones usaron una táctica: neuronas seleccionadas se diseñaron para expresar un marcador de superficie celular humano llamado CD25, que puede ser reconocido por una toxina diseñada que mata únicamente a esas células marcadas. Sin embargo, ese mismo marcador aparece de forma natural en células inmunitarias de primates y posiblemente en células cerebrales, lo que aumentaba el riesgo de que la toxina atacara objetivos equivocados en monos.
Diseñando un escalpelo molecular más seguro
Los autores se propusieron construir un nuevo escalpelo molecular adaptado al uso en primates. En lugar de dirigirse a la versión humana de CD25, se centraron en la versión murina, que es mucho menos similar al CD25 natural de los monos. Primero inmunizaron a un conejo con la proteína CD25 de ratón y emplearon un método basado en microchips para seleccionar células individuales del conejo que producían anticuerpos que se unían fuertemente al CD25 murino pero no a la forma humana. A partir de estas, identificaron un anticuerpo destacado, llamado RMAb-52, con muy alta afinidad. Luego ensamblaron las partes clave de ese anticuerpo con un fragmento tóxico de la bacteria Pseudomonas para crear una única proteína inmunotoxina diseñada, denominada anti-mCD25-PE38.
Probando la herramienta
En experimentos en tubo de ensayo, la nueva inmunotoxina se unió al CD25 murino mucho más fuertemente que al CD25 humano, confirmando su selectividad. Cuando se aplicó a células en cultivo engendradas para portar CD25 murino, la toxina redujo drásticamente su supervivencia a dosis muy bajas, mientras que las células con CD25 humano permanecieron indemnes. A continuación, el equipo pasó a marmosetos vivos. Usando un vector viral especial que viaja de forma retrógrada a lo largo de las fibras nerviosas, introdujeron el gen de CD25 murino en las neuronas productoras de dopamina que envían señales desde una región profunda del cerebro llamada sustancia negra hasta el estriado, una vía crucial para el control del movimiento. Tras esperar a que el virus activara el marcador en estas neuronas, inyectaron la proteína anti-mCD25-PE38 directamente en la zona media del cerebro objetivo.
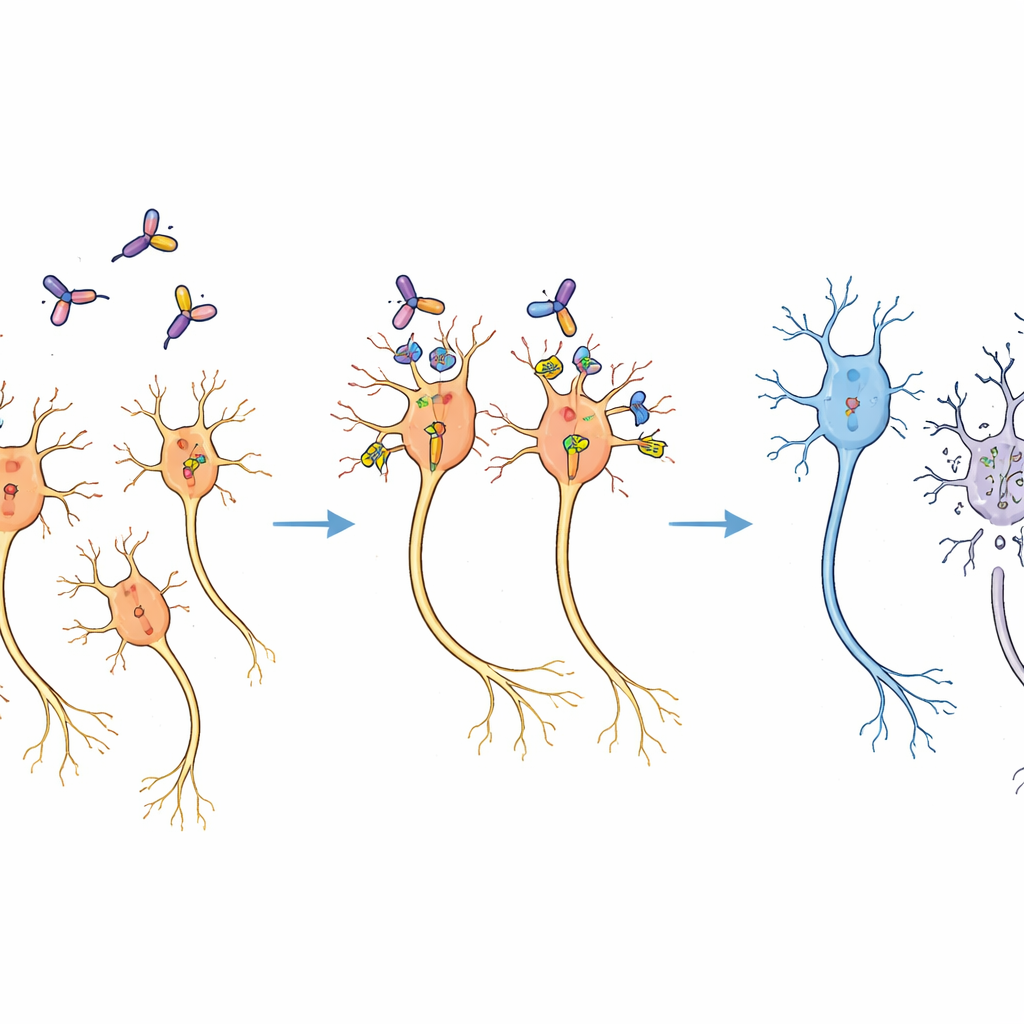
Pérdida selectiva sin daño generalizado
Dos semanas después del tratamiento, las secciones cerebrales de los marmosetos contaron una historia clara. En el lado que recibió la inmunotoxina, el número de neuronas dopaminérgicas se redujo a aproximadamente dos tercios respecto al lado no tratado, como mostraron las tinciones para una enzima productora de dopamina. Aun así, el tejido cerebral circundante parecía normal al microscopio, y otras regiones cerebrales que también recibieron el vector viral no mostraron una pérdida evidente de células. Experimentos piloto ya habían establecido un rango de dosis que evitaba lesiones tisulares inespecíficas, y la dosis elegida quedó claramente dentro de esa ventana segura. El patrón de pérdida coincidió con la propagación esperada del virus y la toxina, lo que indica que las neuronas fueron eliminadas específicamente porque habían sido diseñadas para mostrar CD25 murino, no porque la toxina dañara células de forma indiscriminada.
Qué significa esto para la investigación cerebral futura
Para un lector no especializado, el mensaje clave es que los investigadores han construido un botón de borrado altamente selectivo para poblaciones neuronales elegidas en cerebros de primates. Al combinar un sistema de entrega viral retrógrado con una inmunotoxina específica para ratón, pueden eliminar vías definidas —por ejemplo, circuitos dopaminérgicos implicados en la enfermedad de Parkinson— mientras preservan las células vecinas. Esta estrategia evita reacciones cruzadas peligrosas con el CD25 propio del animal y debería ser especialmente útil cuando ese receptor natural está presente o elevado en la enfermedad. A largo plazo, este enfoque ayudará a los científicos a mapear cómo rutas individuales en el cableado cerebral contribuyen al movimiento, la toma de decisiones y los síntomas psiquiátricos, acercándonos a tratamientos dirigidos que ajusten circuitos defectuosos en lugar de afectar ampliamente a todo el cerebro.
Cita: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Palabras clave: neurociencia en primates no humanos, dirección con inmunotoxinas, neuronas dopaminérgicas, circuitos cerebrales de marmoseto, modelos de la enfermedad de Parkinson