Clear Sky Science · es
Acoplamiento molecular y dinámica revelan nuevos inhibidores de CDK6 para terapia dirigida del glioblastoma
Por qué importa este estudio sobre cáncer cerebral
El glioblastoma es una de las formas más agresivas de cáncer cerebral, y para muchos pacientes los tratamientos actuales siguen sin ser lo suficientemente eficaces o duraderos. Este estudio explora una nueva vía para atacar el glioblastoma centrando el tiro en un único interruptor de control hiperactivo dentro de las células tumorales, una proteína llamada CDK6. Empleando simulaciones informáticas avanzadas en lugar de animales de laboratorio o tubos de ensayo, los investigadores filtraron cientos de moléculas con propiedades farmacológicas e identificaron un candidato especialmente prometedor, denominado compuesto 21, que algún día podría ayudar a frenar o detener esta enfermedad letal.
Un tumor mortal que elude los tratamientos actuales
El glioblastoma crece rápidamente, invade el tejido cerebral circundante y casi siempre reaparece tras cirugía, radioterapia y quimioterapia. Los fármacos estándar como la temozolomida pueden reducir los tumores al principio, pero muchas células cancerosas se adaptan y se vuelven resistentes, lo que conduce a recaídas. Una razón es que su maquinaria interna de división celular permanece en modo “arranque”. Proteínas llamadas CDK actúan como engranajes temporales que dicen a las células cuándo copiar su ADN y dividirse. En el glioblastoma, la vía CDK4/6 está frecuentemente sobreactivada, empujando a las células a multiplicarse incluso frente a la radiación y los fármacos. Eso convierte a CDK6 en un objetivo atractivo: si los científicos pueden apagarlo selectivamente en las células tumorales, podrían ralentizar el crecimiento y hacer que los tratamientos existentes funcionen mejor.
Buscando en el ordenador un mejor inhibidor de CDK6
En lugar de comenzar en el laboratorio, el equipo realizó una búsqueda virtual a gran escala. Empezaron con una molécula conocida que se une a CDK6 y pidieron a un programa de cribado que encontrara cientos de estructuras similares en una base de datos de fármacos. De 400 candidatos iniciales, se seleccionaron 109 para un acoplamiento computacional detallado contra la estructura 3D de la CDK6 humana. El docking es como probar muchas llaves en una cerradura: el software predice qué moléculas encajan con mayor ajuste en el bolsillo activo de la proteína y con qué fuerza podrían unirse. Cuarenta y ocho candidatos parecían incluso mejores que la molécula de referencia original, pero uno, el compuesto 21, destacó por la mayor afinidad prevista y contactos especialmente favorables en puntos específicos de CDK6 que se sabe regulan la selectividad.
Comprobar si el “fármaco virtual” se comporta como una medicina real
Una fuerte unión es solo parte de la historia; un medicamento útil también debe llegar al cerebro, disolverse bien y evitar dañar el tejido sano. Los investigadores utilizaron programas adicionales para estimar cómo se absorbería cada compuesto principal, cómo se distribuiría por el cuerpo y cómo se eliminaría. El compuesto 21 superó las reglas estándar de “apariencia de fármaco”, mostró buena solubilidad predicha y, lo que es importante para los tumores cerebrales, se pronosticó que cruzaría la barrera hematoencefálica manteniéndose razonablemente seguro. Una herramienta separada de toxicidad sugirió que, salvo posibles problemas con dosis orales muy altas, el compuesto 21 tenía menos probabilidades que muchos otros de irritar la piel o los ojos o de causar daños agudos severos. Otro conjunto de cálculos examinó cómo se distribuyen los electrones dentro de la molécula, dando pistas sobre su estabilidad química y su tendencia a formar reacciones secundarias no deseadas; estas pruebas volvieron a favorecer al compuesto 21 frente al fármaco de referencia original.
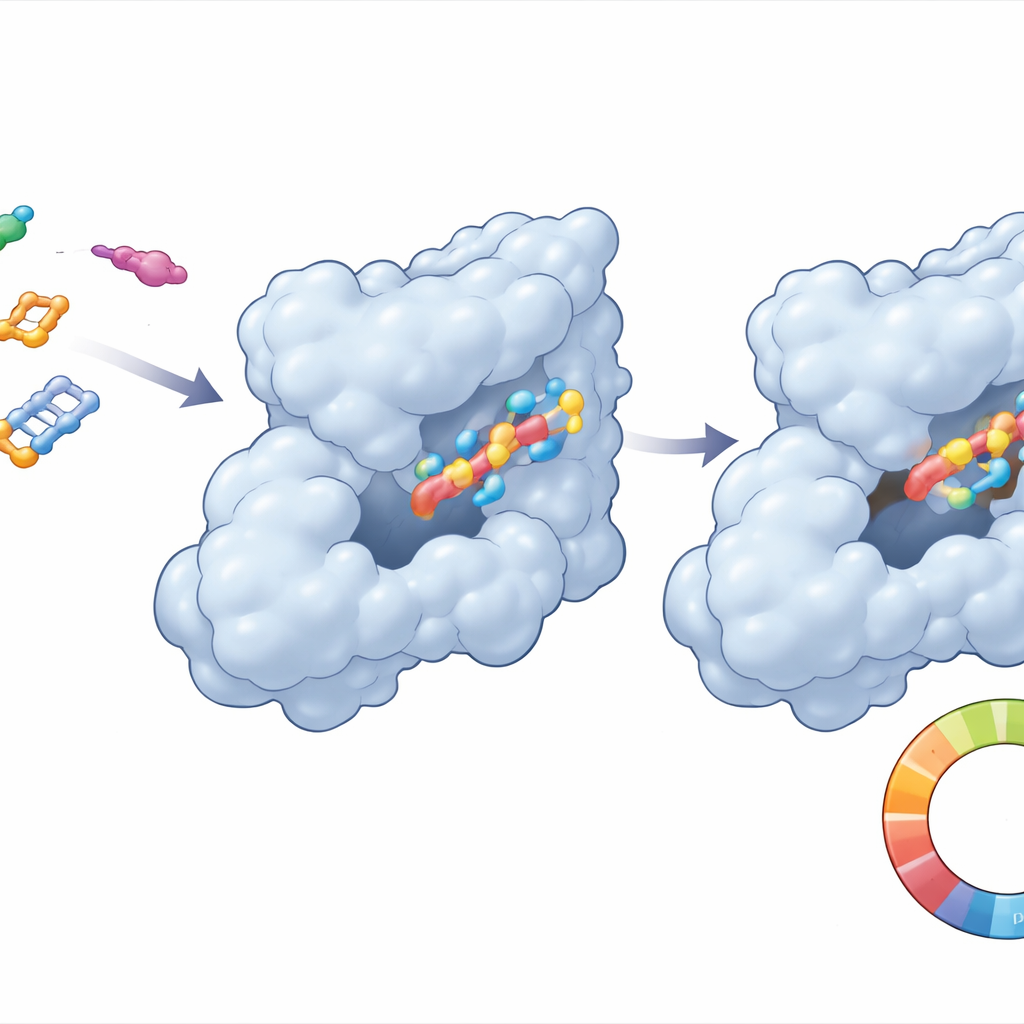
Observando cómo se mueven juntos el fármaco y su diana
Dado que las proteínas y las moléculas farmacológicas no son rígidas, el equipo lanzó “películas” informáticas largas de 250 milmillonésimas de segundo para ver cómo se comportan realmente CDK6 y cada compuesto en un entorno acuoso y similar al corporal. Para el compuesto 21, el complejo se asentó rápidamente en una disposición estable y osciló solo modestamente, una buena señal de que la molécula permanecería alojada en el bolsillo de CDK6. Se mantuvieron puntos de contacto clave entre el fármaco y la proteína, mientras que la forma global de CDK6 permaneció compacta. En contraste, el compuesto de referencia mostró fluctuaciones mayores y contactos más débiles e inconsistentes. Cálculos energéticos adicionales apoyaron la idea de que CDK6 prefiere unirse más firmemente al compuesto 21, principalmente mediante interacciones hidrofóbicas ajustadas (similares al aceite) y enlaces de hidrógeno bien posicionados.
Qué podría significar esto para la atención futura del cáncer cerebral
En conjunto, estas pruebas basadas en ordenador construyen un argumento sólido de que el compuesto 21 es un punto de partida de alta calidad para un nuevo fármaco contra el glioblastoma dirigido a CDK6. Parece más selectivo, más estable y mejor preparado para alcanzar el cerebro que la molécula de referencia, evitando al mismo tiempo muchos escollos comunes de toxicidad. Sin embargo, el trabajo aún está en una fase predictiva: en este estudio no se trataron células ni animales. Los siguientes pasos serán sintetizar el compuesto 21, comprobar si realmente ralentiza el crecimiento de células de glioblastoma en el laboratorio y ver cómo se comporta en modelos animales. Si esos estudios confirman las simulaciones, esta molécula —o versiones mejoradas de la misma— podría eventualmente contribuir a terapias más precisas y dirigidas que ofrezcan a los pacientes con glioblastoma mejores probabilidades y un control de la enfermedad más duradero.
Cita: Khan, M.U., Munir, M., Manzoor, H. et al. Molecular docking and dynamics reveal novel CDK6 inhibitors for targeted glioblastoma therapy. Sci Rep 16, 9000 (2026). https://doi.org/10.1038/s41598-026-39629-7
Palabras clave: glioblastoma, inhibidores de CDK6, terapia dirigida, cribado virtual de fármacos, cáncer cerebral