Clear Sky Science · es
Resolviendo la contradicción entre simulaciones y resultados experimentales del uso de nanopartículas de oro en la terapia con protones
Por qué importan las partículas diminutas de oro en el tratamiento del cáncer
La terapia con protones es una forma avanzada de radioterapia que puede dirigir con precisión los tumores al tiempo que preserva el tejido sano circundante. En los últimos años, los científicos han intentado combinar la terapia con protones con pequeñas partículas de oro, llamadas nanopartículas de oro, para hacer el tratamiento aún más letal para las células cancerosas. Los experimentos muestran que esta combinación a menudo destruye más células tumorales que los protones solos, pero las simulaciones por ordenador han tenido dificultades para explicar por qué. Este artículo aborda ese misterio de larga data y apunta a un protagonista distinto del que muchos investigadores esperaban.
Historia antigua: culpando a los electrones rápidos
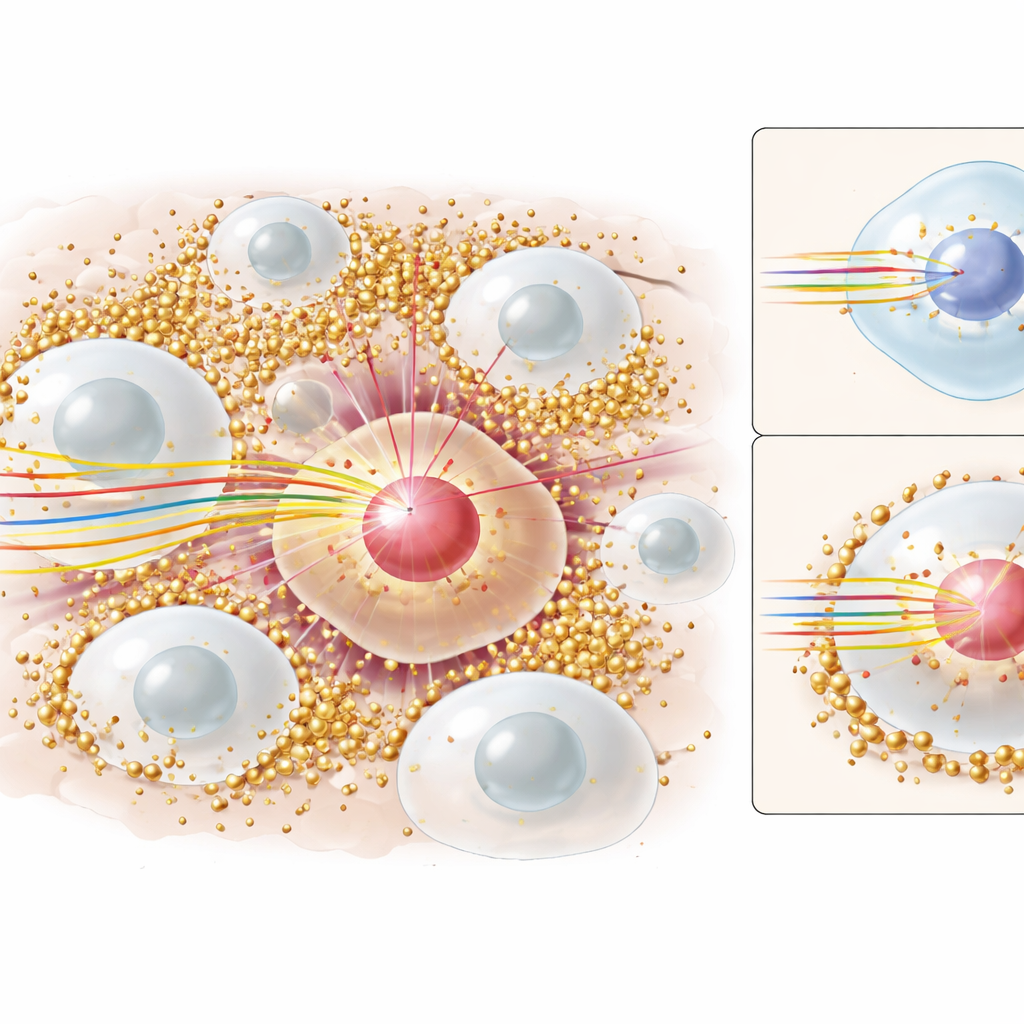
Las nanopartículas de oro ya son famosas en tratamientos con rayos X y gamma, donde aumentan el daño principalmente al emitir enjambres de electrones energéticos. Esos electrones viajan distancias cortas y rompen el ADN en células cercanas. Durante años, muchos supusieron que el mismo argumento básico valía para la terapia con protones: los protones golpean el oro, salen electrones adicionales y las células cancerosas sufren. Pero había un problema. Modelos por ordenador detallados que siguen cada partícula y su energía —del tipo usado en este estudio— seguían prediciendo muy poco aumento de dosis en el núcleo celular por parte de esos electrones, sobre todo porque la mayoría de las nanopartículas se sitúan en la región externa de la célula, no dentro del núcleo donde reside el ADN. Al mismo tiempo, los experimentos de laboratorio con células mostraban aumentos claros en la muerte celular y en la eficacia del tratamiento cuando había oro presente. Los números sencillamente no cuadraban.
Nuevo panorama: frenando los propios protones
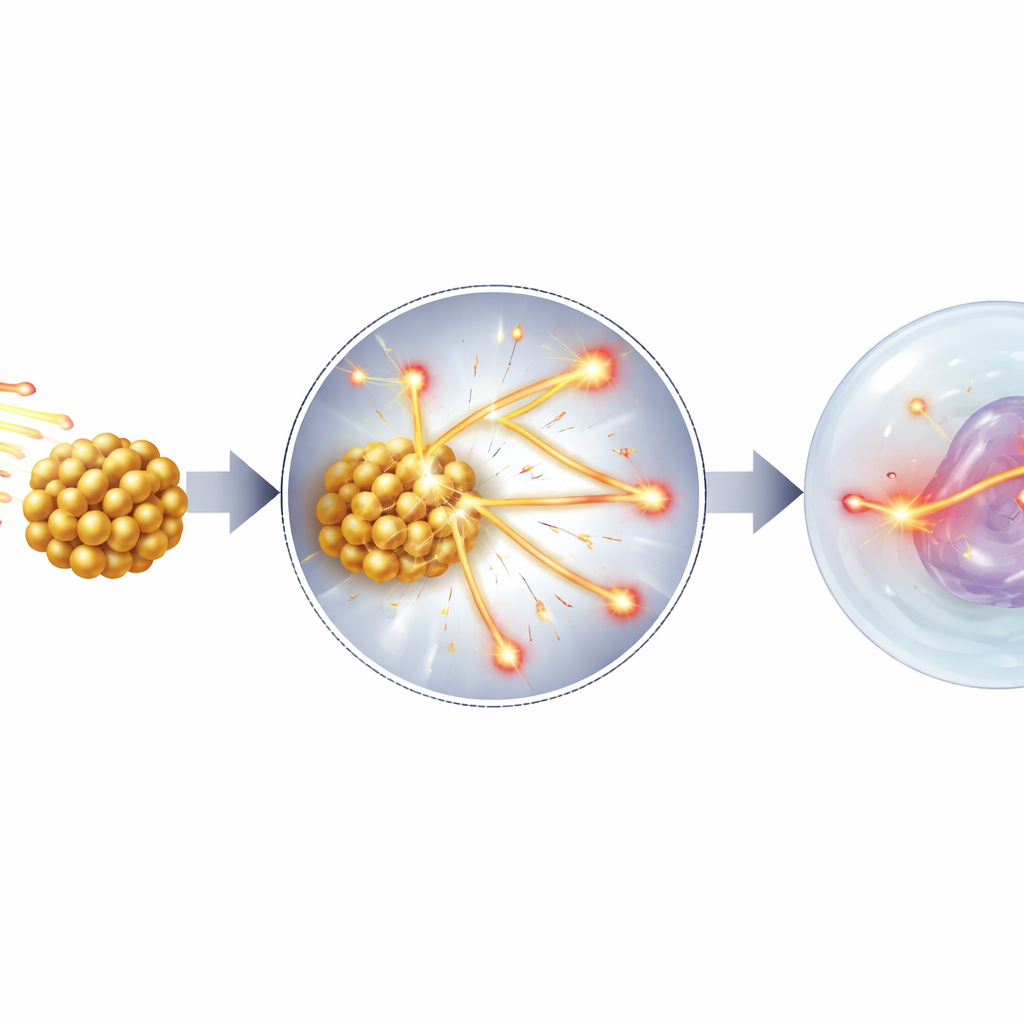
Este trabajo propone y prueba un mecanismo principal distinto: en lugar de comportarse principalmente como emisores de electrones, las nanopartículas de oro actúan como pequeños topes de velocidad para los protones. Cuando un protón atraviesa una región salpicada de metales de alta densidad y alto número atómico como el oro o el hierro, sufre muchas colisiones pequeñas con esos átomos pesados. Cada colisión extrae un poco más de energía de lo que ocurriría en tejido normal, por lo que el protón se desacelera más rápido y su pérdida de energía por unidad de distancia —conocida en física como transferencia lineal de energía, o LET— aumenta. Las trayectorias de alto LET son especialmente dañinas para el ADN porque generan racimos densos de rupturas que la célula tiene dificultades para reparar. Al ejecutar simulaciones Monte Carlo detalladas con la caja de herramientas Geant4, el autor muestra que el oro y otras nanopartículas pesadas aumentan de manera significativa el número de protones lentos y de alto LET que alcanzan el núcleo celular, aunque la longitud total del recorrido esté en la escala de micrómetros, muy por encima del alcance de los electrones de baja energía tradicionalmente responsables.
Haciendo coincidir las simulaciones con experimentos celulares reales
Para comprobar si este nuevo panorama se mantiene, el estudio recrea varios experimentos celulares publicados en los que tumores fueron tratados con haces de protones más diversas nanopartículas (oro, hierro y platino) de distintos tamaños y concentraciones. Para cada caso, las simulaciones calculan cuánto aumento de dosis recibe el núcleo —resumido como una relación de mejora de dosis— y luego lo introducen en una fórmula radiobiológica estándar que relaciona la dosis administrada con la supervivencia celular. Este enfoque modifica la curva habitual que describe cuántas células viven o mueren tras una dosis determinada de radiación. En la mayoría de los experimentos examinados, las curvas de supervivencia predichas con nanopartículas se alinearon estrechamente con los datos medidos, a menudo con un error de aproximadamente un uno por ciento. Al mismo tiempo, las simulaciones muestran que la dosis de electrones en el núcleo cambia apenas cuando se añaden nanopartículas, mientras que la fluencia de protones más lentos y dañinos aumenta claramente. Quedan algunos desacuerdos, que el autor atribuye a incertidumbres en cómo se montaron o informaron ciertos experimentos, pero la tendencia global apoya con fuerza la explicación de la desaceleración de protones.
Límites, excepciones y cuándo el oro ayuda más
El artículo también explora situaciones en las que las nanopartículas no parecen ayudar mucho. Para haces de protones de energía muy baja que se detienen en apenas unas pocas capas celulares, simplemente no hay suficiente distancia para que los protones encuentren muchas nanopartículas y se desaceleren de forma significativa, por lo que no se observa un gran aumento de eficacia. De igual modo, algunas formas complejas de nanopartículas o geometrías experimentales mal descritas son difíciles de reproducir en simulaciones, lo que puede explicar algunos valores atípicos donde los modelos y las medidas no coinciden. El autor señala que si partículas extremadamente pequeñas penetraran realmente en el núcleo, entonces la emisión de electrones y las reacciones químicas con moléculas celulares podrían añadirse al efecto. Aun así, en muchas condiciones de tratamiento realistas, el patrón dominante es coherente: una mayor desaceleración de protones en regiones ricas en oro conduce a un daño más concentrado en el núcleo.
Qué significa esto para la atención futura del cáncer
Para no especialistas, la conclusión es que las nanopartículas de oro en la terapia con protones funcionan menos como pequeñas pistolas de electrones y más como frenos invisibles que convierten protones rápidos y relativamente suaves en impactos más lentos y potentes justo donde importa —el ADN de la célula tumoral. Al clarificar este mecanismo y mostrar que puede reproducir con precisión datos reales de supervivencia celular, el estudio ayuda a resolver un conflicto de larga duración entre teoría y experimento. Esta idea podría orientar diseños más inteligentes de tratamientos basados en nanopartículas, como la elección de materiales, tamaños y concentraciones que maximicen la desaceleración de protones cerca de los núcleos tumorales mientras se minimizan los efectos secundarios. A la larga, esto podría hacer la terapia con protones más precisa y potente, ofreciendo mejores resultados para pacientes con cánceres difíciles de tratar.
Cita: Tabbakh, F. Resolving the contradiction between simulation and experimental results of using gold nanoparticles in proton therapy. Sci Rep 16, 8012 (2026). https://doi.org/10.1038/s41598-026-39621-1
Palabras clave: terapia con protones, nanopartículas de oro, radiosensibilización, radioterapia contra el cáncer, nanomedicina