Clear Sky Science · es
Una caja de herramientas multimodal en pez cebra para estudiar la barrera hematoencefálica en salud y enfermedad
Por qué importan los vasos cerebrales filtrantes
Cuando los vasos sanguíneos del cerebro o del ojo empiezan a filtrar, el líquido y las proteínas se infiltran en el tejido nervioso circundante, provocando hinchazón que puede difuminar la visión o afectar la capacidad de pensar. Este tipo de “anegamiento” —conocido como edema vasogénico— participa en la pérdida de visión diabética, el ictus, el traumatismo craneal y algunas formas de demencia. Sin embargo, los científicos aún carecen de métodos sencillos y económicos para observar en tiempo real el fallo de esta barrera protectora. Este estudio presenta un modelo versátil en pez cebra que permite a los investigadores ver, medir y sondear cómo la glucosa sanguínea elevada debilita la barrera de los vasos cerebrales, acelerando potencialmente la búsqueda de nuevos tratamientos.
Un pez diminuto con una ventaja clara
Las larvas de pez cebra ofrecen una ventana única al cerebro vivo. A diferencia de los mamíferos, sus cuerpos son transparentes en las fases iniciales y sus vasos sanguíneos cerebrales pueden visualizarse con fluorescencia al microscopio. Los autores aprovecharon esto centrándose en la barrera hematoencefálica, el cierre hermético entre la sangre y el tejido cerebral que se parece a la barrera hematorretiniana interna que protege nuestros ojos. Dado que los mismos tipos celulares y muchas de las mismas proteínas protectoras se comparten entre cerebro y retina, el equipo usó la barrera cerebral en pez cebra como un sustituto para estudiar enfermedades como el edema macular diabético y otros trastornos neurovasculares, pero en un sistema más rápido, más ético y menos costoso que los modelos tradicionales en roedores.
Aumentar la glucosa en larvas de pez cebra
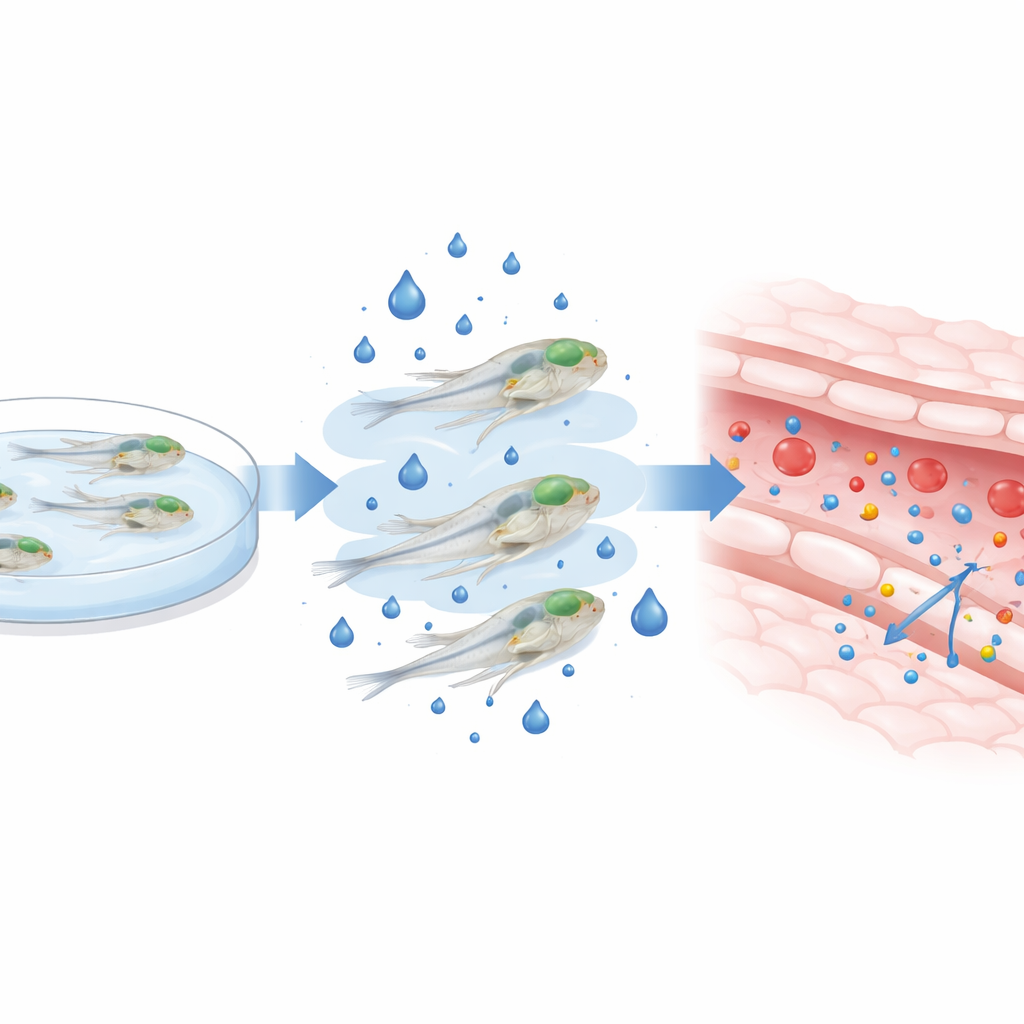
Para imitar la hiperglucemia presente en la diabetes, los investigadores criaron larvas de pez cebra en agua con glucosa adicional entre el tercer y el quinto día tras la fertilización —una ventana crítica en la que la barrera cerebral todavía está madurando. Confirmaron que este baño externo de azúcar elevó los niveles internos de glucosa varias veces sin matar a las larvas ni alterar su morfología general. Con los peces aún vivos y nadando, inyectaron colorantes fluorescentes de distintos tamaños en la circulación y usaron microscopios confocales de alta resolución para rastrear cuánto colorante se filtraba desde los vasos cerebrales hacia el tejido circundante. Tras dos días de exposición a alta glucosa, tanto las moléculas de tinte pequeñas como las grandes se filtraron más en el cerebro, especialmente con la dosis de azúcar más alta, lo que indica que la barrera se había vuelto más permeable.
Qué sucede en la pared vascular
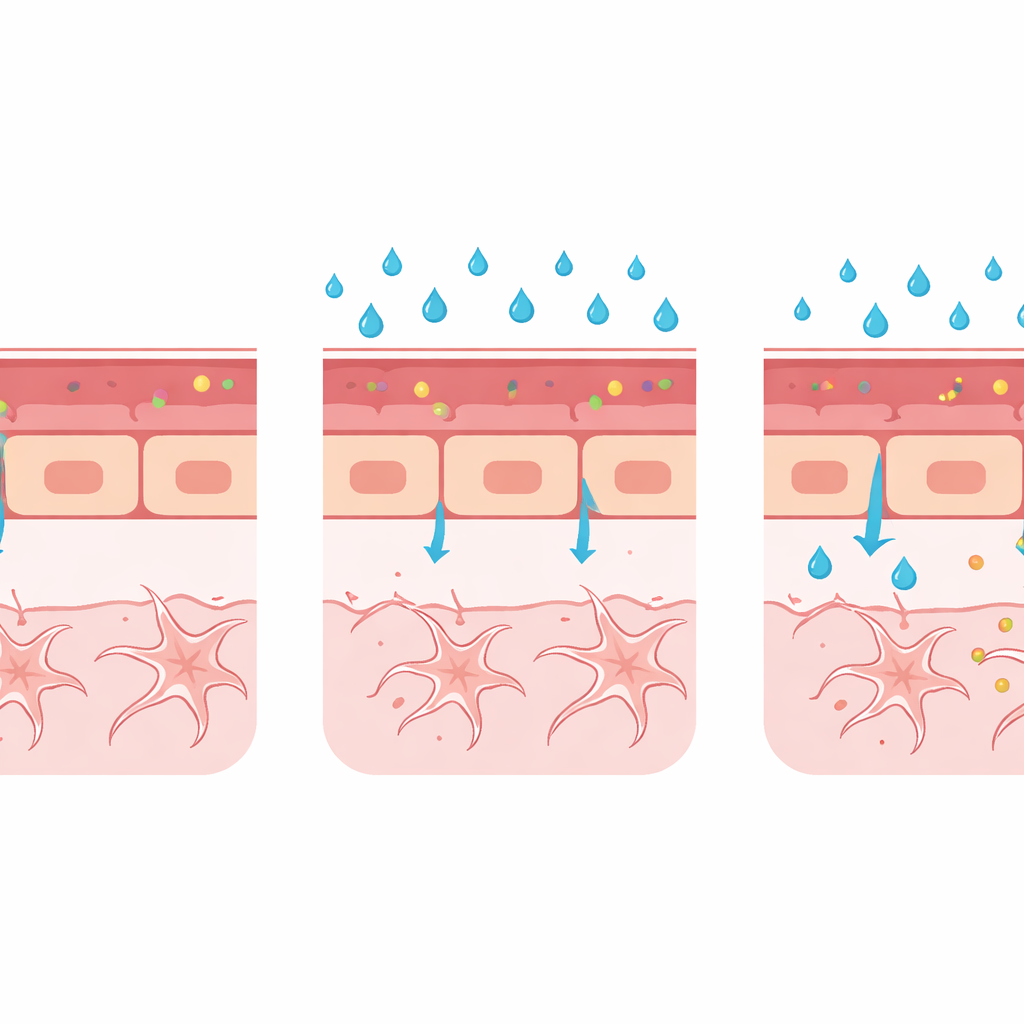
Más allá de medir simplemente la fuga, el equipo construyó una “caja de herramientas” multimodal para examinar qué fallaba en la propia pared vascular. Midieron el ancho de una arteria cerebral clave y encontraron que la glucosa alta provocó la dilatación del vaso —un cambio temprano también observado en personas con enfermedad ocular diabética. Usando peces cebra modificados para iluminar proteínas específicas, mostraron que la glucosa elevada redujo los niveles de claudina-5, un componente principal de los sellos estrechos entre células vasculares adyacentes, y aumentó los niveles de PLVAP, una proteína asociada a vasos inmaduros y propensos a fugas que transportan material a través de la capa celular. La microscopía electrónica, que puede revelar estructuras a escala nanométrica, confirmó un sutil ensanchamiento en las uniones entre células, aunque las pequeñas vesículas de transporte llamadas caveolas fueron demasiado escasas para cuantificarlas de forma fiable en esta primera aproximación.
Una plataforma flexible para la investigación futura de enfermedades
En conjunto, estos cambios —mayor filtración de colorante, vasos más anchos, uniones celulares debilitadas y aumento de PLVAP— dibujan un panorama coherente: la glucosa elevada puede retrasar o desviar la formación adecuada de la barrera en el cerebro en desarrollo. El modelo todavía no captura la ruptura de una barrera completamente madura, como ocurre en enfermedades humanas crónicas, pero sobresale en mostrar cómo condiciones perjudiciales durante el desarrollo pueden impedir que la barrera se selle correctamente. Dado que las técnicas son compatibles con una variedad de líneas reporteras fluorescentes e imágenes avanzadas, la misma plataforma puede ampliarse para estudiar otros desencadenantes de fallo de la barrera, como moléculas inflamatorias, alteraciones en células de soporte como pericitos y glía, o perturbaciones en vías de señalización clave.
Qué significa esto para los pacientes
Para el público general, el mensaje central es que este trabajo ofrece un banco de pruebas práctico y vivo para observar cómo la pared protectora del cerebro falla bajo estrés, usando pequeños peces transparentes en lugar de mamíferos de mayor tamaño. Siguiendo en tiempo real cómo la glucosa alta remodela la estructura y función vascular, los investigadores pueden identificar más rápido qué moléculas y tipos celulares hay que apuntar para mantener la barrera intacta. En última instancia, estos conocimientos podrían orientar el desarrollo de nuevos fármacos o estrategias terapéuticas para prevenir o reducir la fuga de líquido en ojos y cerebro —ayudando a preservar la vista y proteger la función cognitiva en personas con diabetes y otras enfermedades neurovasculares.
Cita: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Palabras clave: barrera hematoencefálica, modelo de pez cebra, complicaciones diabéticas, fuga vascular, enfermedad neurovascular