Clear Sky Science · es
Caracterización genómica e in vitro de dos bacteriófagos líticos que infectan la cepa multirresistente de Erwinia AnSW2-5
Por qué importan a todos las bacterias que arruinan cosechas
En todo el mundo, los agricultores luchan contra enfermedades bacterianas que pudren frutos, marchitan hojas y arrasan las cosechas. Muchos de estos brotes ahora son causados por cepas que ya no responden a antibióticos comunes, poniendo en peligro tanto el suministro de alimentos como los medios de vida que dependen de ellos. Este estudio explora una alternativa emergente: el uso de virus que atacan bacterias, llamados bacteriófagos, para desactivar de forma segura a un patógeno vegetal particularmente persistente hallado en suelos vinculados al uso intensivo de antibióticos.
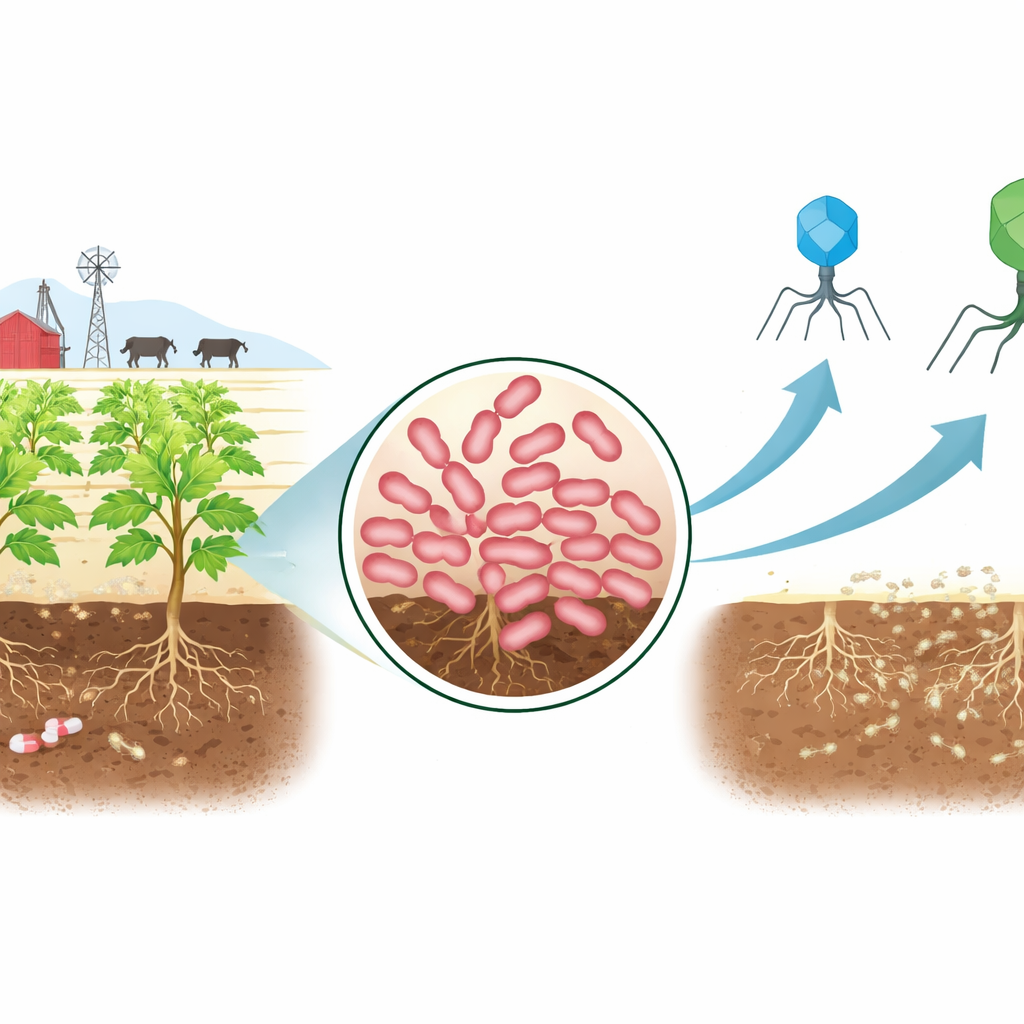
Un nuevo invasor difícil en el campo
Los investigadores empezaron muestreando suelo de un corral de ganado conocido por recibir desechos animales y antibióticos. De este entorno hostil aislaron una cepa de Erwinia, un grupo bacteriano que incluye a notorios causantes del fuego bacteriano en manzanas y la pudrición blanda en patatas. Las pruebas mostraron que esta cepa, denominada AnSW2-5, podía resistir múltiples familias de antibióticos importantes, incluidas drogas usadas contra una amplia gama de infecciones. El análisis genético confirmó la razón: su ADN portaba varios genes de resistencia conocidos y potentes bombas moleculares que expulsan antibióticos fuera de la célula. Al mismo tiempo, las comparaciones genómicas revelaron que esta cepa es distinta de las especies de Erwinia descritas anteriormente, lo que la convierte en un modelo útil para estudiar cómo controlar nuevos patógenos vegetales difíciles de tratar.
Dos pequeños depredadores con fortalezas distintas
Para encontrar enemigos naturales de esta bacteria multirresistente, el equipo recurrió al agua dulce del mismo sitio y la enriqueció para obtener bacteriófagos capaces de infectar AnSW2-5. Aislaron dos candidatos prometedores, etiquetados P-A y P-K. Bajo el microscopio electrónico, P-A aparecía compacto con una cola corta, un diseño asociado con una infección rápida y directa. P-K, en contraste, tenía una cola más larga y contráctil con una estructura de base compleja, lo que sugiere una forma más enérgica de perforar su huésped. La secuenciación de sus genomas mostró que ambos fagos son estrictamente líticos: invaden, se replican y hacen estallar la célula, en lugar de permanecer ocultos en el ADN bacteriano. Sin embargo, lo hacen con herramientas genéticas muy distintas: el genoma depurado de P-A favorece un ataque rápido, mientras que el genoma más grande de P-K codifica maquinaria estructural y de replicación más elaborada.
Cómo ataca el equipo viral
Cuando los científicos siguieron el ciclo vital de cada fago en el laboratorio, encontraron que P-A ataca con rapidez: necesita solo alrededor de 20 minutos antes de que comiencen a aparecer nuevas partículas virales, y cada bacteria infectada libera alrededor de 70 descendientes. P-K tarda más —unos 35 minutos antes de empezar a producir nuevos fagos— pero cada célula infectada rinde aproximadamente 110 nuevas partículas. En pruebas de cocultivo donde bacterias y fagos crecieron juntos durante tres días, ambos fagos por separado frenaron el crecimiento bacteriano pero no lo impidieron por completo. Las bacterias terminaron recuperándose, reflejando la aparición de supervivientes resistentes. Sin embargo, cuando P-A y P-K se combinaron en un mismo cóctel, redujeron la población bacteriana en más del 80% y la mantuvieron suprimida durante las 72 horas del experimento.
Evitar que la resistencia consiga un punto de apoyo
Uno de los hallazgos más llamativos fue cómo la pareja de fagos afectó la aparición de mutantes resistentes. Cuando se expusieron a P-A o P-K por separado, una pequeña fracción de bacterias —aproximadamente una entre un millón y una entre diez millones— consiguió escapar y crecer a pesar del ataque del fago. Pero cuando se usaron ambos fagos juntos, las colonias resistentes se volvieron tan raras que quedaron por debajo del límite de detección del experimento. Esto sugiere que los dos virus probablemente se adhieren a dianas diferentes en la superficie bacteriana o alteran la célula de maneras complementarias. Para que una sola bacteria sobreviva, tendría que superar ambos mecanismos a la vez, un suceso prácticamente imposible. En términos prácticos, esto hace que el cóctel sea mucho más resistente frente a los trucos evolutivos que a menudo condenan a los antibióticos.
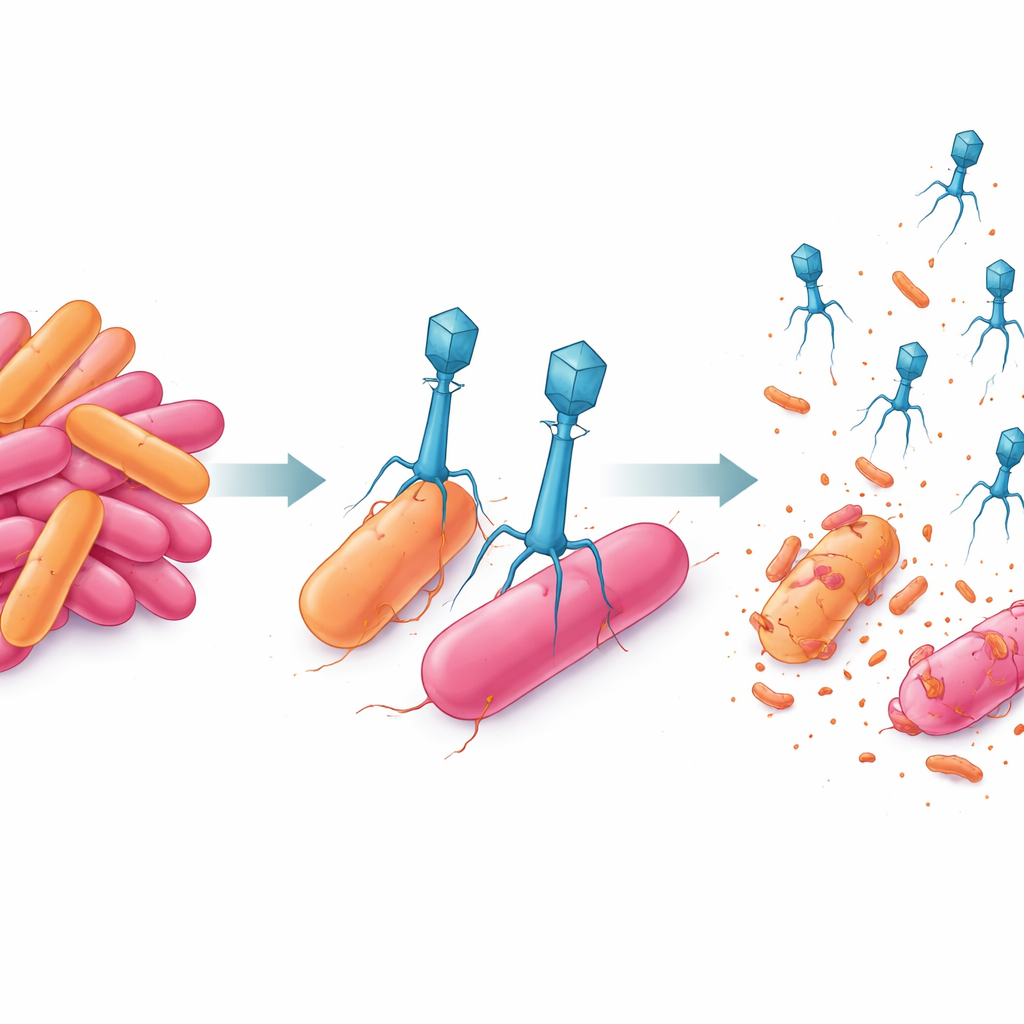
Qué podría significar esto para las cosechas futuras
En conjunto, el trabajo muestra que pares de bacteriófagos cuidadosamente elegidos pueden hacer más que simplemente reducir bacterias vegetales peligrosas: también pueden acotar la capacidad de las bacterias para evolucionar resistencia. Al combinar un fago de acción rápida con otro que produce un mayor número de descendientes, los investigadores crearon un equipo viral que mantuvo bajo control una cepa multirresistente de Erwinia durante días mientras prevenía variantes detectables de escape. Aunque estos ensayos se realizaron en el laboratorio y no en huertos o campos, apuntan a un futuro en el que mezclas de fagos específicas formen parte del manejo integrado de plagas, ayudando a los agricultores a proteger las cosechas con mucha menos dependencia de los antibióticos tradicionales.
Cita: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Palabras clave: biocontrol con bacteriófagos, enfermedades bacterianas de las plantas, resistencia a antibióticos en la agricultura, terapia con fagos contra Erwinia, cócteles de fagos