Clear Sky Science · es
Perfil proteómico del lavado broncoalveolar tras un desafío endotelínico segmentario humano: un posible modelo de exacerbación
Por qué importa una breve ráfaga de inflamación pulmonar
Las enfermedades pulmonares crónicas, como la enfermedad pulmonar obstructiva crónica (EPOC), suelen empeorar de forma súbita cuando las vías respiratorias se inflaman de manera aguda, con frecuencia por infecciones. Estos episodios, llamados exacerbaciones, provocan hospitalizaciones y pueden deteriorar de forma permanente la función respiratoria. Estudiarlas directamente en pacientes resulta difícil y arriesgado. Este estudio emplea una irritación pulmonar breve y controlada en voluntarios sanos para imitar ciertos aspectos de esas crisis, y luego mide cientos de proteínas en el líquido pulmonar para identificar qué señales se activan. Los hallazgos ayudan a los investigadores a comprender la química de la inflamación pulmonar y pueden acelerar la búsqueda de nuevos tratamientos.
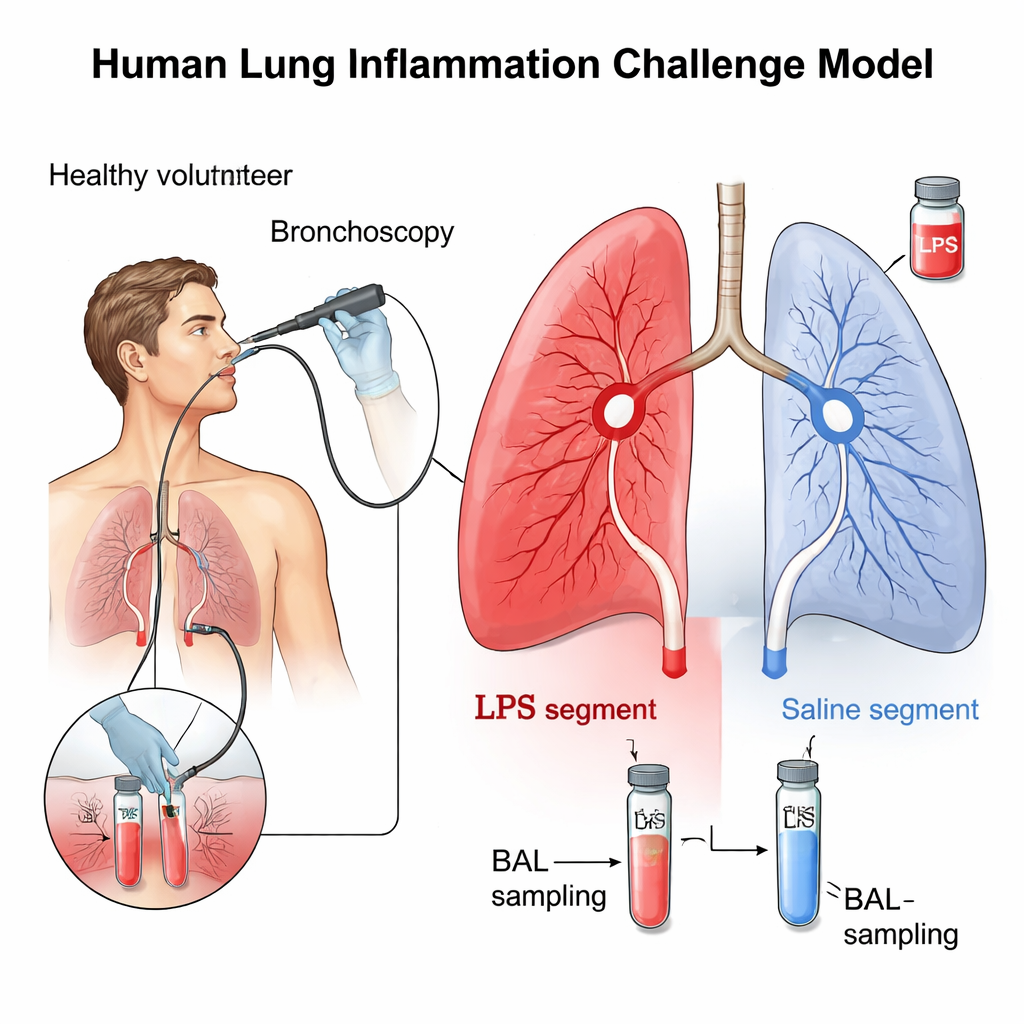
Crear un mini «brote pulmonar» seguro
Los investigadores usaron una técnica bien establecida que irrita de forma breve y localizada una pequeña región del pulmón. Diez adultos sanos no fumadores se sometieron a broncoscopia, en la que un tubo delgado y flexible se introduce en las vías respiratorias. A través de este tubo, el equipo administró una minidosis de endotoxina bacteriana, conocida como lipopolisacárido (LPS), en un segmento pulmonar y solución salina en un segmento equivalente del otro lado como control. El LPS es un componente natural de ciertas bacterias que activa con fuerza las defensas del organismo. Tras 24 horas, se lavaron las mismas áreas con solución salina en un procedimiento llamado lavado broncoalveolar (BAL) para recolectar el líquido y las células del interior del pulmón para un análisis detallado.
Hacer un censo de proteínas en el líquido pulmonar
En lugar de examinar solo unos pocos marcadores conocidos, el equipo empleó una tecnología de alto rendimiento (la plataforma SomaScan) que puede medir alrededor de 1.500 proteínas diferentes a la vez en el líquido de BAL. Compararon muestras tomadas antes de cualquier desafío, tras la saline y tras el LPS. Como era de esperar, las muestras predesafío y las de la saline fueron muy similares, lo que confirma que el procedimiento en sí no provocó inflamación. En contraste, los segmentos tratados con LPS mostraron un cambio dramático: 599 proteínas aumentaron de forma significativa y solo cuatro disminuyeron. Muchas de las proteínas elevadas son mensajeros inflamatorios bien conocidos, como IL‑6 e IL‑8, enzimas como la mieloperoxidasa (MPO) y MMP9, y proteínas de fase aguda como la proteína C reactiva (PCR) y el factor von Willebrand (VWF). Los análisis de componentes principales y de agrupamiento mostraron que las muestras con LPS formaron un grupo claramente separado, lo que subraya cuánto modifica este desafío local el entorno pulmonar.
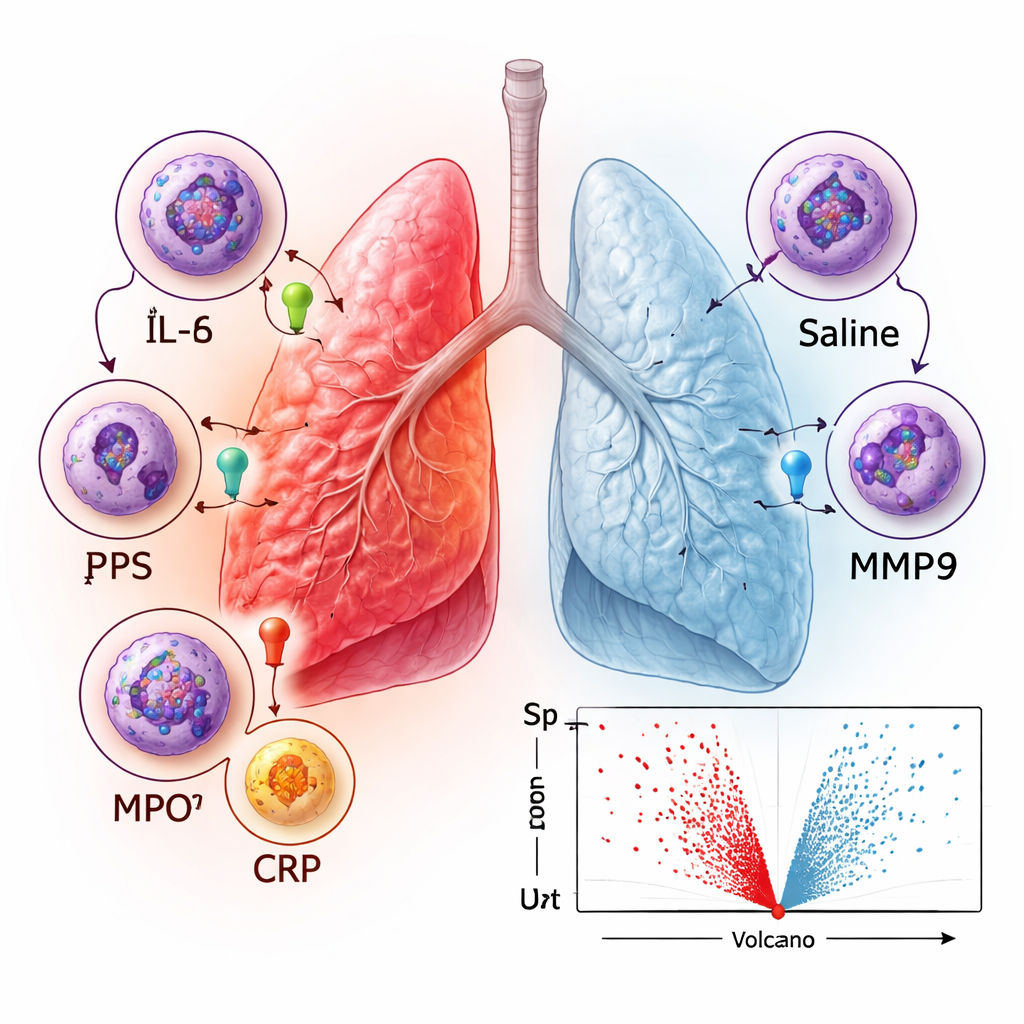
Qué revelan los patrones proteicos sobre las defensas pulmonares
Para ir más allá de los marcadores aislados, el equipo examinó qué tipos de procesos biológicos estaban más enriquecidos entre las proteínas que aumentaron tras el LPS. Las señales más fuertes involucraron la actividad inmune general y respuestas a estímulos externos o químicos, junto con procesos vinculados al movimiento celular y la muerte celular programada. El análisis de redes sobre cómo interactúan las proteínas destacó agrupaciones de quimiocinas (moléculas que atraen células inmunitarias), enzimas remodeladoras de tejido llamadas metaloproteinasas de matriz y componentes del inmunoproteasoma, una maquinaria celular que ayuda a procesar proteínas extrañas para su reconocimiento por el sistema inmunitario. Estos patrones coinciden con lo conocido sobre la respuesta pulmonar a la infección: células inmunitarias como los neutrófilos son atraídas a las vías respiratorias, los microbios dañinos son atacados y el tejido circundante se remodela y, si es necesario, se repara.
Conectando el modelo con las exacerbaciones reales de EPOC
Los autores plantearon luego hasta qué punto este modelo de LPS a corto plazo refleja las exacerbaciones de EPOC en el mundo real. Compararon sus datos del líquido pulmonar con una lista publicada de biomarcadores sanguíneos que aumentan cuando las personas con EPOC experimentan una crisis. De 17 marcadores evaluables, 16 —incluidos IL‑6, IL‑8, PCR, fibrinógeno y varias quimiocinas— también estaban elevados en BAL tras el LPS. Solo uno (sTREM‑1) no cambió, en consonancia con resultados previos variables sobre su utilidad. Esta fuerte superposición sugiere que muchas de las mismas vías inflamatorias se activan cuando un pulmón sano es desafiado brevemente con LPS y cuando un pulmón vulnerable con EPOC sufre una exacerbación grave. Al mismo tiempo, los autores señalan que la respuesta al LPS es temporal y no reproduce por completo el daño estructural crónico observado en la enfermedad de larga duración.
Qué significa esto para futuros tratamientos
En términos sencillos, este estudio muestra que una irritación controlada y de corta duración en una parte del pulmón de voluntarios sanos puede desencadenar una tormenta química que se asemeja mucho a lo que ocurre durante las exacerbaciones de EPOC. Al mapear cientos de proteínas que aumentan o disminuyen durante esta respuesta, los investigadores obtienen una imagen detallada de qué señales y vías podrían ser más importantes como dianas terapéuticas. Dado que el modelo es seguro, repetible y ya se usa en ensayos tempranos de fármacos, ofrece un terreno de prueba potente para nuevos medicamentos antiinflamatorios y para identificar biomarcadores más precisos que algún día podrían ayudar a los médicos a predecir, detectar y tratar mejor el empeoramiento súbito de la enfermedad pulmonar crónica.
Cita: Gress, C., Müller, M. & Hohlfeld, J.M. Proteomic profiling of bronchoalveolar lavage following human segmental endotoxin challenge—a potential exacerbation model. Sci Rep 16, 6145 (2026). https://doi.org/10.1038/s41598-026-39528-x
Palabras clave: inflamación pulmonar, exacerbación de EPOC, lavado broncoalveolar, desafío con endotoxina, proteómica