Clear Sky Science · es
Modelado estructural y análisis de acoplamiento de mutaciones de sentido erróneo canónicas y nuevas asociadas a resistencia en Escherichia coli de Sudán
Por qué importa para la salud cotidiana
Las infecciones resistentes a los antibióticos ya no son curiosidades médicas raras; amenazan cada vez más los tratamientos rutinarios de infecciones urinarias, cirugías y cuidados intensivos. Este estudio examina de cerca bacterias Escherichia coli procedentes de Sudán y plantea una pregunta muy concreta: ¿cómo remodelan pequeños cambios genéticos en proteínas bacterianas la eficacia de antibióticos comunes? Empleando modelado estructural por ordenador en lugar de costosos experimentos de laboratorio, los autores descubren patrones de resistencia ocultos que las pruebas estándar y las bases de datos globales pueden pasar por alto, especialmente en entornos con pocos recursos donde la resistencia está aumentando más rápido. 
Mirando dentro de la caja de herramientas bacteriana
Los investigadores se centraron en las mutaciones de “sentido erróneo” —cambios de una sola letra en el ADN que sustituyen un bloque constructivo de la proteína por otro. Analizaron genomas completos de 55 aislados de E. coli recogidos en Sudán y se enfocaron en proteínas bacterianas que son dianas directas de clases principales de antibióticos, incluidas las fluoroquinolonas, los macrólidos y la rifampicina. Estas dianas incluyen enzimas que retuercen el ADN (girasas y topoisomerasa IV), el ribosoma que fabrica proteínas y la ARN polimerasa. De 71 mutaciones encontradas en estas proteínas, 19 fueron señaladas por múltiples herramientas predictivas como probablemente dañinas para la función proteica y, de forma llamativa, la mayoría de estas parecían ser variaciones inéditas no recogidas aún en las bases de datos globales de resistencia.
Nuevos puntos problemáticos en dianas conocidas
Algunos de los cambios más importantes se agruparon en una proteína ribosómica llamada L22, que contribuye a formar el túnel por el que salen las proteínas recién sintetizadas del ribosoma. Esa región también actúa como sitio de acoplamiento para macrólidos como la eritromicina. El estudio identificó un conjunto denso de mutaciones en L22 no reportadas previamente, muchas dentro de una misma cepa, que se sitúan justo a lo largo de ese túnel y en puntos de contacto con el ARN ribosómico. Los análisis computacionales sugirieron que varias de estas alteraciones desestabilizan la estructura local o la hacen más flexible, lo que podría remodelar el túnel y hacer que las moléculas de macrólido encajen con menos ajuste. Al mismo tiempo, aparecieron mutaciones “canónicas” de resistencia más conocidas en las proteínas de procesamiento del ADN ParC y ParE y en la ARN polimerasa, confirmando que las cepas sudanesas comparten algunos rasgos de resistencia globales al tiempo que presentan variantes locales propias.
Cómo los cambios de forma debilitan el agarre del antibiótico
El equipo fue más allá de las listas de secuencias y preguntó cómo podrían alterar estas mutaciones el ajuste tridimensional entre antibióticos y sus dianas. Mediante simulaciones de acoplamiento molecular, compararon cómo se unían diferentes fármacos a proteínas normales y mutadas. Para la topoisomerasa IV ParC, mutaciones clave cerca del sitio de contacto con el fármaco debilitaron sustancialmente la unión prevista de la fluoroquinolona trovafloxacino, reflejando un agarre más flojo en la unión enzima–ADN–fármaco. En la proteína ParE relacionada, las mutaciones redujeron modestamente la unión de la novobiocina. En contraste, una mutación novedosa en la girasa GyrA pareció desestabilizar la estructura de la enzima sin cambiar de forma notable la afinidad de la fluoroquinolona moxifloxacino, lo que indica que la resistencia a veces puede surgir al perturbar sutilmente el rendimiento enzimático más que al expulsar simplemente el fármaco. 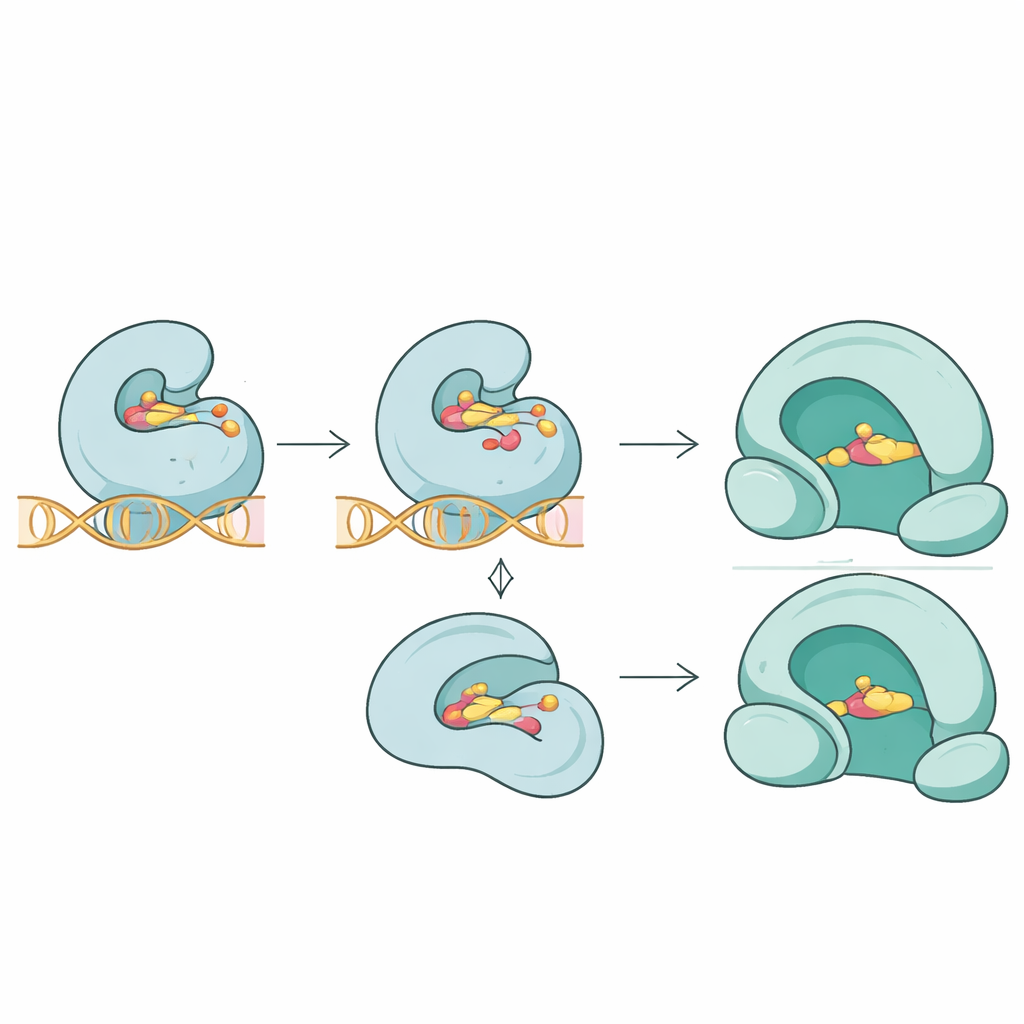
Efectos mixtos según el fármaco
No todas las mutaciones tuvieron el mismo impacto. Cambios clásicos asociados a resistencia a la rifampicina en la ARN polimerasa RpoB alteraron poco la unión de un inhibidor nuevo y estructuralmente distinto que se dirige a un sitio cercano, lo que sugiere que futuros fármacos podrían diseñarse para eludir patrones de resistencia existentes. Para la proteína ribosómica L22, los estudios de acoplamiento con eritromicina mostraron un mosaico de resultados: algunas mutaciones debilitaron la unión, otras tuvieron poco efecto e incluso una mejoró ligeramente el ajuste predicho. Estos resultados subrayan que la resistencia rara vez es de todo o nada; en su lugar, cada mutación empuja la estabilidad proteica, la flexibilidad y la unión al fármaco en distintas direcciones, y el efecto global sobre el tratamiento depende de cómo se combinen estos cambios dentro de una célula bacteriana viva.
Qué significa esto para pacientes y vigilancia
Desde una perspectiva no especializada, el mensaje clave es que las bacterias en lugares como Sudán están desarrollando resistencia tanto por vías bien conocidas como por rutas menos conocidas. Las vías conocidas implican mutaciones clásicas ya rastreadas por programas internacionales, pero este estudio muestra que muchas mutaciones adicionales, enriquecidas localmente, también pueden debilitar los antibióticos de maneras más sutiles. Al mapear estos cambios sobre estructuras proteicas detalladas, los autores ofrecen una lista corta de mutaciones que deberían probarse en el laboratorio y considerarse en paneles diagnósticos regionales. En términos prácticos, su trabajo defiende que el modelado computacional inteligente puede ayudar a países con capacidad de laboratorio limitada a vigilar mejor la resistencia emergente, apoyando en última instancia decisiones terapéuticas más fiables e inspirando diseños de fármacos que se adelanten a la evolución bacteriana.
Cita: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Palabras clave: resistencia a antimicrobianos, Escherichia coli, mutaciones de sentido erróneo, bioinformática estructural, Sudán