Clear Sky Science · es
Integrar aprendizaje profundo con modelado basado en física permite predicciones de alta precisión de la interfaz anticuerpo-antígeno
Por qué esto importa para los medicamentos del futuro
Los anticuerpos son los misiles teledirigidos de nuestro sistema inmunitario y de muchos fármacos modernos. Para diseñar mejores anticuerpos, los científicos necesitan saber exactamente cómo un anticuerpo sujeta su molécula objetivo, o antígeno. Medir estas estructuras experimentalmente es lento y caro. Este estudio demuestra que combinar aprendizaje profundo con modelado clásico de estilo físico puede mejorar de forma notable las predicciones informáticas sobre dónde toca un anticuerpo al antígeno, acelerando potencialmente el diseño y el cribado de anticuerpos.
Encontrar la zona de apretón de manos
Los anticuerpos reconocen sus objetivos usando pequeños bucles flexibles en sus extremos, llamados regiones de unión, que se juntan para formar un parche de contacto. Estos bucles pueden doblarse y torsionarse, y la zona coincidente en el antígeno suele estar extendida y ser superficial en lugar de formar un bolsillo profundo. Esa flexibilidad y sutileza hacen que el problema de acoplamiento —determinar cómo encajan las dos formas— sea extremadamente difícil para los ordenadores. Los programas de acoplamiento tradicionales prueban muchas posiciones relativas de las dos proteínas y las puntúan con reglas físicas como la atracción electrostática y el desplazamiento de agua, pero sin pistas biológicas con frecuencia se conforman con emparejamientos incorrectos.
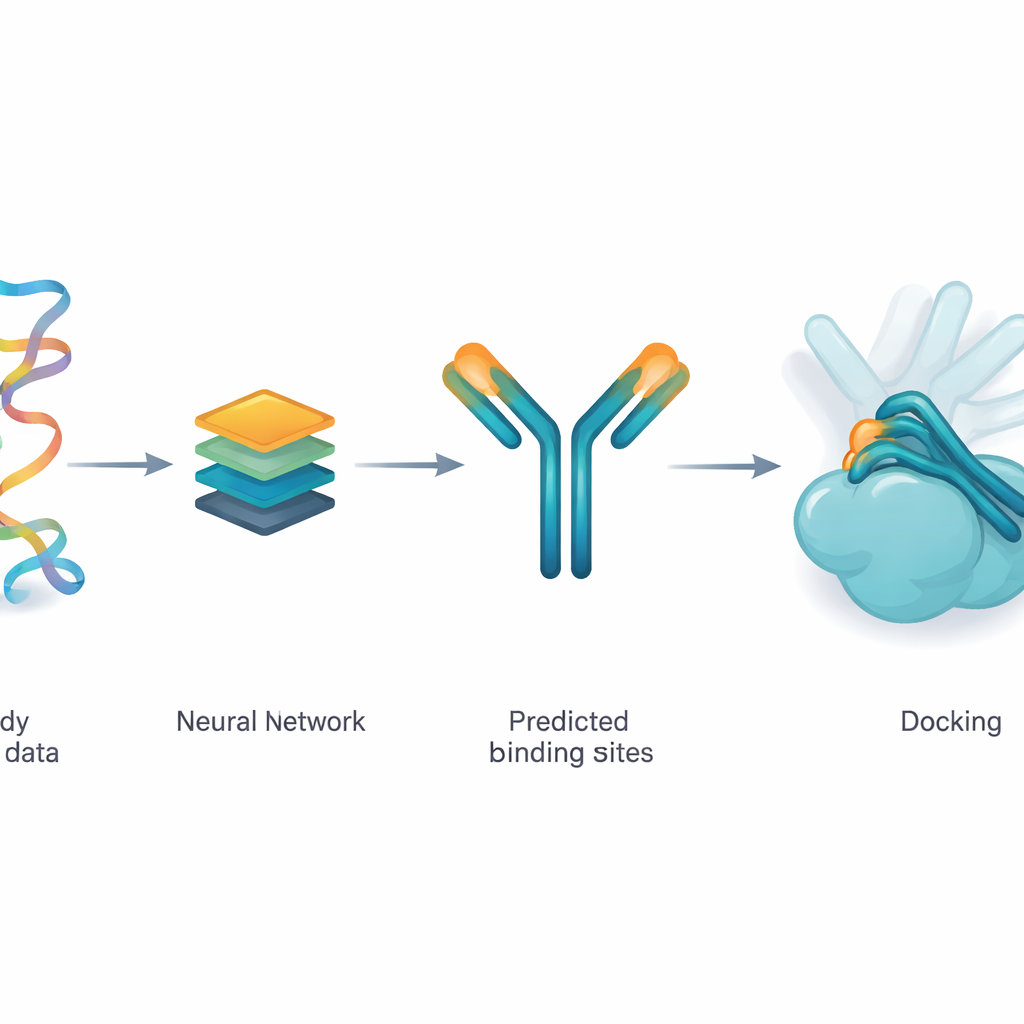
Entrenar una red para sugerir puntos de contacto probables
Los autores usan un modelo de aprendizaje profundo llamado ParaDeep para estimar qué aminoácidos de un anticuerpo tienen más probabilidad de tocar el antígeno. ParaDeep hace esto usando solo la secuencia del anticuerpo —el orden de sus bloques constructivos— en lugar de necesitar una estructura 3D completa. Lee las secuencias de las cadenas pesada y ligera juntas, codifica sus características químicas y posicionales, y emplea mecanismos de atención para resaltar residuos que parecen buenos candidatos para la unión. Cada posición recibe una puntuación de probabilidad; las que superan un umbral se tratan como una zona de contacto predicha que puede volver a mapearse sobre la estructura del anticuerpo.
Guiar un motor físico en lugar de reemplazarlo
En vez de usar aprendizaje profundo para generar complejos anticuerpo–antígeno completos desde cero, el equipo introduce los residuos de contacto predichos por ParaDeep en un motor de acoplamiento basado en física existente llamado PyDockWEB. Este programa de acoplamiento muestrea miles de posibles maneras en que el anticuerpo y el antígeno podrían encontrarse y las puntúa con una función de energía. En el nuevo marco, los residuos de contacto predichos actúan como restricciones suaves: sesgan la búsqueda de modo que muchas orientaciones muestreadas acerquen esos residuos a la superficie del antígeno. Es importante que la puntuación física subyacente y el tratamiento como cuerpos rígidos de las proteínas permanezcan sin cambios, lo que hace el proceso transparente y relativamente ligero de ejecutar.
¿Cuánto mejoran las predicciones?
Los investigadores probaron su enfoque híbrido en 50 complejos anticuerpo–antígeno conocidos procedentes de una base de datos curada. Para cada caso compararon el acoplamiento «a ciegas» estándar con el acoplamiento guiado por las restricciones de ParaDeep. Midiieron la precisión local de la interfaz (qué tan de cerca coincidía la región de contacto predicha con la real), la similitud global de forma y una puntuación de calidad combinada ampliamente usada para evaluar modelos de acoplamiento. En este conjunto, el método guiado redujo considerablemente los errores en el sitio de unión, acercó las estructuras globales a los complejos reales y movió muchas predicciones de claramente erróneas a categorías de calidad media o alta. Casi la mitad de los modelos guiados alcanzaron rango de alta calidad, frente a aproximadamente una cuarta parte con el acoplamiento a ciegas.
Qué hace que algunos emparejamientos sean más fáciles que otros
El equipo también analizó por qué algunos complejos se beneficiaron más que otros. Encontraron que predecir simplemente más residuos de contacto no garantizaba el éxito; lo que importaba era colocar las restricciones en la zona correcta, no su número. Las interfaces más hidrofílicas y con más segmentos flexibles tipo coil tendieron a acoplar mejor, probablemente porque funcionaban bien con el énfasis de PyDockWEB en la electrostática y resultaban más fáciles de alinear sin grandes cambios de forma. Cuando los investigadores repitieron algunos casos fallidos usando información de contacto «oráculo» extraída directamente de estructuras experimentales, la mayoría mejoró, confirmando que la localización precisa del parche de contacto es un ingrediente clave —pero el acoplamiento de cuerpos rígidos sigue teniendo límites cuando se requieren grandes ajustes de forma.
Qué significa esto de cara al futuro
En términos cotidianos, este trabajo muestra que darle a un programa de acoplamiento basado en física una pista inteligente sobre dónde es probable que un anticuerpo agarre su objetivo puede mejorar mucho su puntería, sin convertir el proceso en una caja negra opaca. La canalización combinada ParaDeep–PyDockWEB no reemplaza métodos más avanzados y flexibles o generativos, pero ofrece una forma práctica de usar señales de aprendizaje profundo a nivel de secuencia para guiar herramientas de acoplamiento familiares e interpretables. A medida que los esfuerzos de descubrimiento e ingeniería de anticuerpos generen bibliotecas de secuencias cada vez mayores, estos enfoques híbridos podrían ayudar a los investigadores a filtrar rápidamente candidatos que sean estructuralmente consistentes con un objetivo deseado, haciendo el camino de la secuencia a un anticuerpo utilizable más rápido y mejor informado.
Cita: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
Palabras clave: acoplamiento de anticuerpos, aprendizaje profundo, predicción de paratopos, interacciones proteína–proteína, diseño de anticuerpos