Clear Sky Science · es
Impacto de la quimioterapia neoadyuvante en la funcionalidad de las células estromales mesenquimales derivadas del tejido adiposo y sus efectos moduladores sobre los fibroblastos en pacientes oncológicos
Por qué esto importa para los supervivientes de cáncer
Muchas personas que reciben tratamiento contra el cáncer sufren después problemas de cicatrización lenta y complicaciones tras la cirugía. Al mismo tiempo, los médicos exploran cada vez más formas de utilizar las propias células reparadoras derivadas de la grasa del paciente para ayudar a recuperar los tejidos. Este estudio plantea una pregunta práctica y urgente: después de la quimioterapia, ¿siguen siendo utilizables esas células reparadoras y, si no, cuáles son las más afectadas?
Los reparadores ocultos del cuerpo
El tejido graso es más que almacenamiento de energía. Alberga una población abundante de células reparadoras versátiles llamadas células estromales mesenquimales derivadas del tejido adiposo, o AD-MSCs. Estas células no permanecen inactivas: liberan un cóctel de moléculas señalizadoras que pueden calmar la inflamación, estimular la formación de nuevos vasos sanguíneos y animar a las células vecinas a crecer y reconstruir el tejido dañado. Justo por encima de la grasa, en la piel, residen los fibroblastos: células trabajadoras que migran hacia las heridas y depositan colágeno, la estructura proteica que aporta resistencia al tejido nuevo. Juntos, los AD-MSCs y los fibroblastos ayudan a determinar cuánto se recupera la piel tras una lesión o una operación.
Evaluando las células reparadoras de la grasa antes y después del tratamiento
Los investigadores recogieron pequeñas muestras de piel y grasa de 66 pacientes sometidos a cirugía, algunos de los cuales habían recibido quimioterapia previamente y otros no. A partir de la grasa aislaron AD-MSCs y confirmaron que estas células conservaban la apariencia y el comportamiento propios de células reparadoras: presentaban los marcadores de superficie esperados y podían diferenciarse en células tipo hueso, cartílago y grasa en el laboratorio. De la piel aislaron fibroblastos. El equipo comparó después cómo crecían los AD-MSCs y los fibroblastos de pacientes expuestos o no a quimioterapia, su ciclo de división, las moléculas señalizadoras que liberaban y la expresión de genes relacionados con la cicatrización y la regeneración.
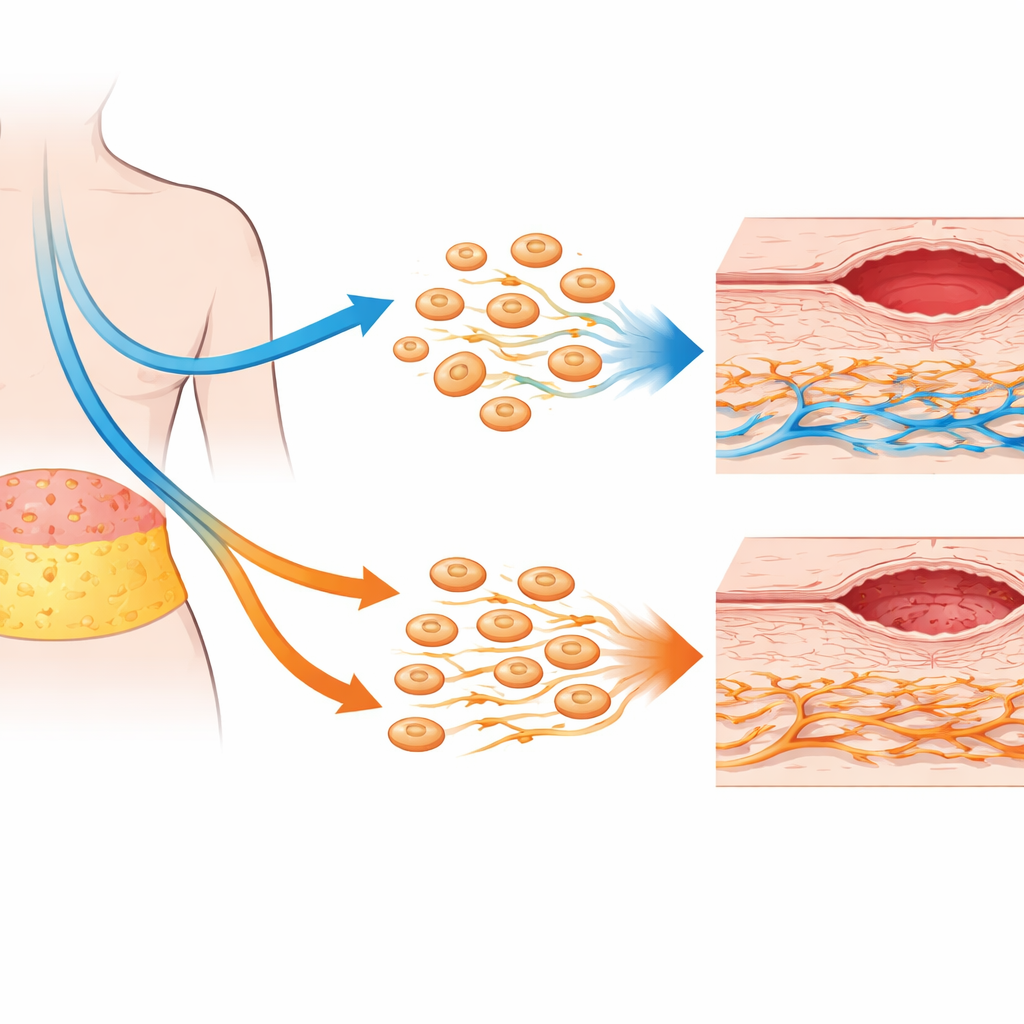
Las células reparadoras de la grasa se mantienen sorprendentemente fuertes
Contrariamente a la preocupación de que la quimioterapia pudiera mermar la capacidad de los AD-MSCs, el estudio encontró que estas células derivadas de la grasa eran notablemente resistentes. Sus marcadores de identidad básicos, su patrón de crecimiento y su perfil de proteínas secretadas se mantuvieron en gran medida sin cambios tras la quimioterapia previa. La actividad génica asociada con el crecimiento, la autorrenovación y la reparación de heridas mostró sólo pequeños cambios sin significado práctico. De hecho, los AD-MSCs de pacientes tratados con quimioterapia exhibieron una actividad mitocondrial ligeramente superior, lo que sugiere un metabolismo más activo en lugar de daño. En experimentos de cocultivo —donde AD-MSCs y fibroblastos compartían el mismo medio pero sin contacto directo— los AD-MSCs continuaron potenciando ciertos comportamientos de los fibroblastos, como el movimiento dirigido hacia señales de reparación, especialmente en muestras de pacientes que no habían recibido quimioterapia.
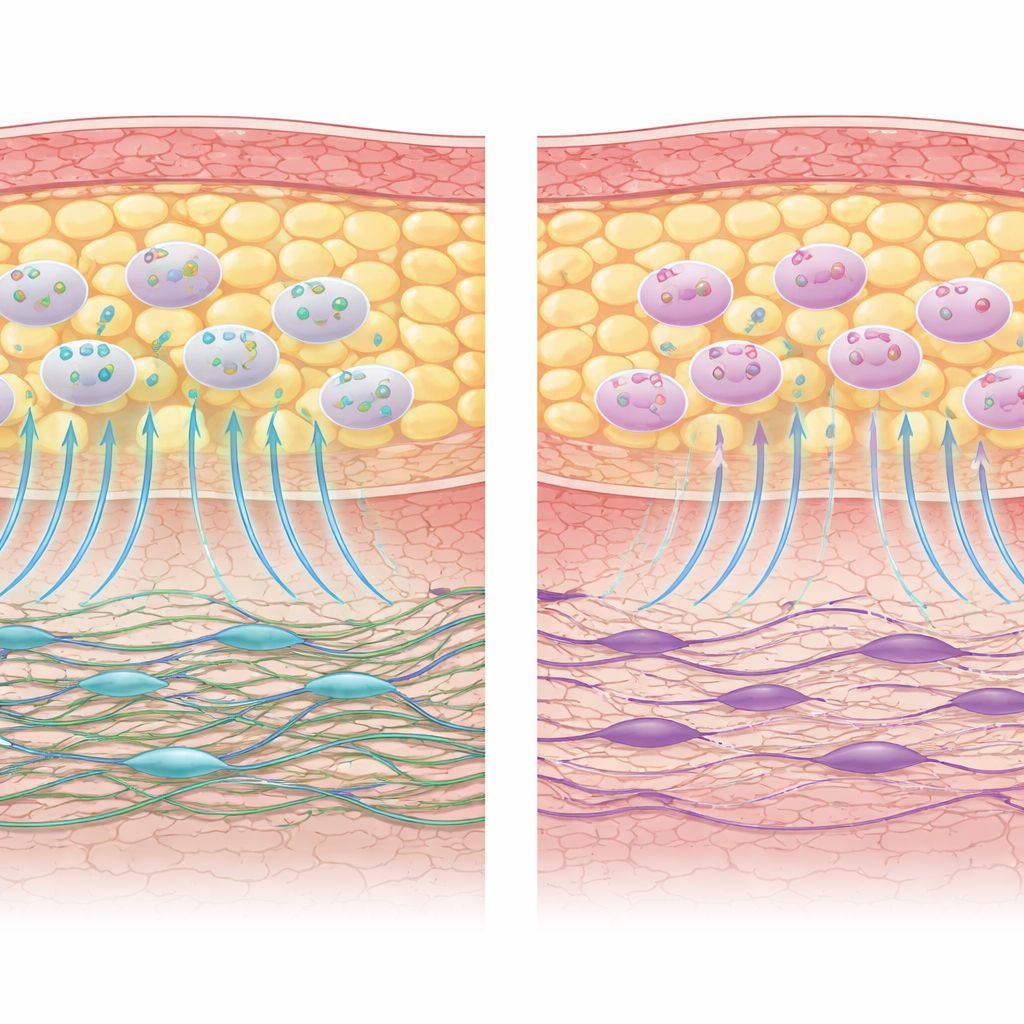
Los constructores de la piel sufren el mayor impacto de la quimioterapia
La situación fue muy distinta para los fibroblastos. Las células obtenidas de la piel de pacientes tratados con quimioterapia mostraron claros signos de menor vigor biológico. Su capacidad para migrar hacia una “herida” tipo arañazo en una placa de cultivo estaba significativamente reducida y su producción de colágeno tendía a ser menor. El perfil de moléculas señalizadoras que liberaban se inclinó hacia un estado más inflamatorio y menos regenerativo, y muchos genes asociados con señales de crecimiento, sus receptores y el potencial regenerativo estaban disminuidos. Incluso cuando estos fibroblastos se cocultivaron con sus propios AD-MSCs, la mayoría de sus funciones —movilidad, producción de colágeno y actividad génica beneficiosa— permanecieron deprimidas en comparación con los fibroblastos de pacientes que no habían recibido quimioterapia.
Qué significa esto para futuras terapias de cicatrización
Para un lector no especializado, la conclusión de este trabajo es que la quimioterapia no parece arruinar la reserva de células reparadoras basadas en la grasa del cuerpo, pero sí deja a los constructores de primera línea de la piel —los fibroblastos— menos capacitados para incorporarse rápidamente a las heridas y reconstruir tejido resistente. Dado que los AD-MSCs mantienen su funcionalidad, siguen siendo candidatos prometedores para su uso en procedimientos reconstructivos, cuidado de heridas e injertos de grasa tras el tratamiento del cáncer. No obstante, el deterioro de los fibroblastos puede limitar cuánto beneficio pueden aportar por sí solos estas células similares a las madre. Los autores sugieren que las terapias futuras podrían necesitar apoyar a ambas partes de la asociación reparadora: preservar o restaurar la salud de los fibroblastos mientras se aprovechan AD-MSCs robustos, idealmente en modelos más complejos y fieles al organismo que capten mejor el entorno real de cicatrización en los supervivientes de cáncer.
Cita: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Palabras clave: quimioterapia, cicatrización de heridas, células madre derivadas de la grasa, fibroblastos, medicina regenerativa