Clear Sky Science · es
Papel de la microscopía de fuerza atómica en la caracterización de esferoides cancerígenos heterotípicos y su interacción con partículas de microplástico
Por qué importa la textura del tejido canceroso
El cáncer suele describirse en términos de genes y células defectuosas, pero su sensación física —qué tan blando o rígido es el tejido— también influye en cómo crece un tumor y cómo responde a su entorno. Este estudio examina pequeños agregados tridimensionales de células de cáncer de pulmón, llamados esferoides, y plantea dos preguntas prácticas: ¿podemos usar un microscopio táctil de alta resolución para medir con fiabilidad la rigidez de estos mini‑tumores, y esa rigidez, influye en cómo interaccionan con partículas de microplástico en suspensión que puedan alcanzar los pulmones?
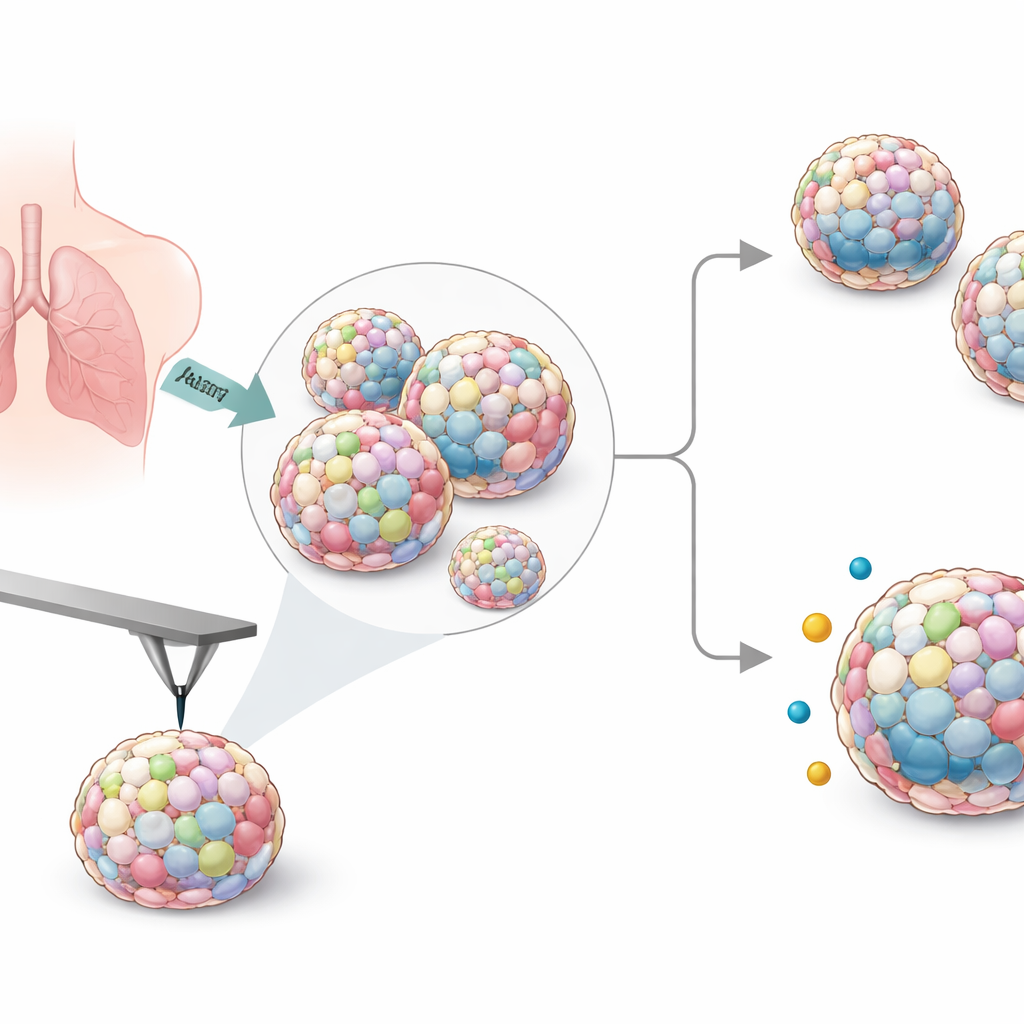
Construir mini tumores pulmonares en el laboratorio
Para imitar la composición compleja de tumores reales, los investigadores cultivaron esferoides mixtos a partir de seis líneas celulares humanas de cáncer de pulmón junto con células de apoyo llamadas fibroblastos, y en algunos casos macrófagos con comportamiento similar al inmunitario. Probaron varias maneras de formar estos agregados y optaron por placas especiales de baja adhesión que producían de forma fiable esferoides redondos y estables lo bastante grandes para manipular. Ajustando el número y la proporción de células, crearon esferoides tanto pequeños como más grandes, y luego eligieron una receta estándar que funcionó de forma consistente en todos los tipos celulares cancerosos.
Echar un vistazo interior y comprobar la salud celular
Una vez formados los esferoides, el equipo examinó su estructura interna y el comportamiento celular usando diversas tinciones y métodos de seccionado. Cortes finos mostraron que algunas combinaciones de células cancerosas formaron bolas muy compactas, mientras que otras eran más laxas y con espacios más abiertos. Los fibroblastos tendían a situarse hacia el centro, especialmente en la mayoría de las combinaciones celulares, mientras que las células cancerosas se concentraban cerca del exterior. La tinción de vivos‑muertos reveló un patrón familiar visto en tumores reales: células vivas bien nutridas en el borde y más células dañadas o en proceso de morir en el núcleo con baja oxigenación. Una prueba de marcado de ADN para detectar división celular mostró que, en la mayoría de los esferoides, las células de toda la estructura aún podían proliferar, aunque una línea celular cancerosa (Calu‑3) se dividía principalmente en el borde exterior.
Medir la rigidez con una sonda a nanoescala
Para convertir la textura en números, los científicos usaron microscopía de fuerza atómica, en la que una sonda diminuta y afilada presiona suavemente la superficie del esferoide y registra cuánto se deprime. A partir de esto calcularon el módulo de Young, una medida estándar de rigidez. Aunque los esferoides eran similares en tamaño, su rigidez varió sustancialmente según la línea de cáncer de pulmón que contenían. Los esferoides con células A549 fueron de los más blandos, mientras que los que contenían H23 o HCC827 fueron notablemente más rígidos. La adición de macrófagos aumentó en general la rigidez para varios tipos de cáncer. Al comparar estos valores con la velocidad de crecimiento de las células cancerosas originales en cultivo plano, encontraron que las células de división más lenta tendían a formar esferoides más rígidos, vinculando el comportamiento de crecimiento con las propiedades mecánicas.
Probar el contacto con microplásticos
Dado que se han detectado fragmentos microscópicos de plástico en tumores pulmonares, los investigadores expusieron sus esferoides a partículas fluorescentes de poliestireno de aproximadamente un micrómetro de diámetro, a concentraciones similares a las medidas en sangre humana. En condiciones estáticas, las partículas se aglomeraban y se adherían de forma desigual a un lado de los esferoides, por lo que el grupo cambió a una ligera oscilación de las muestras para imitar mejor los fluidos corporales en movimiento. En estas condiciones dinámicas, sólo unas pocas partículas individuales se adherieron o penetraron las capas celulares externas, demasiado pocas para contarlas con precisión. En su lugar, el equipo volvió a las mediciones de rigidez. Tras la exposición, muchos tipos de esferoides se volvieron ligeramente más rígidos, consistente con cuentas rígidas de plástico que se adhieren o quedan alojadas en la superficie, pero este cambio no mostró una dependencia clara y simple respecto a la rigidez inicial del esferoide.
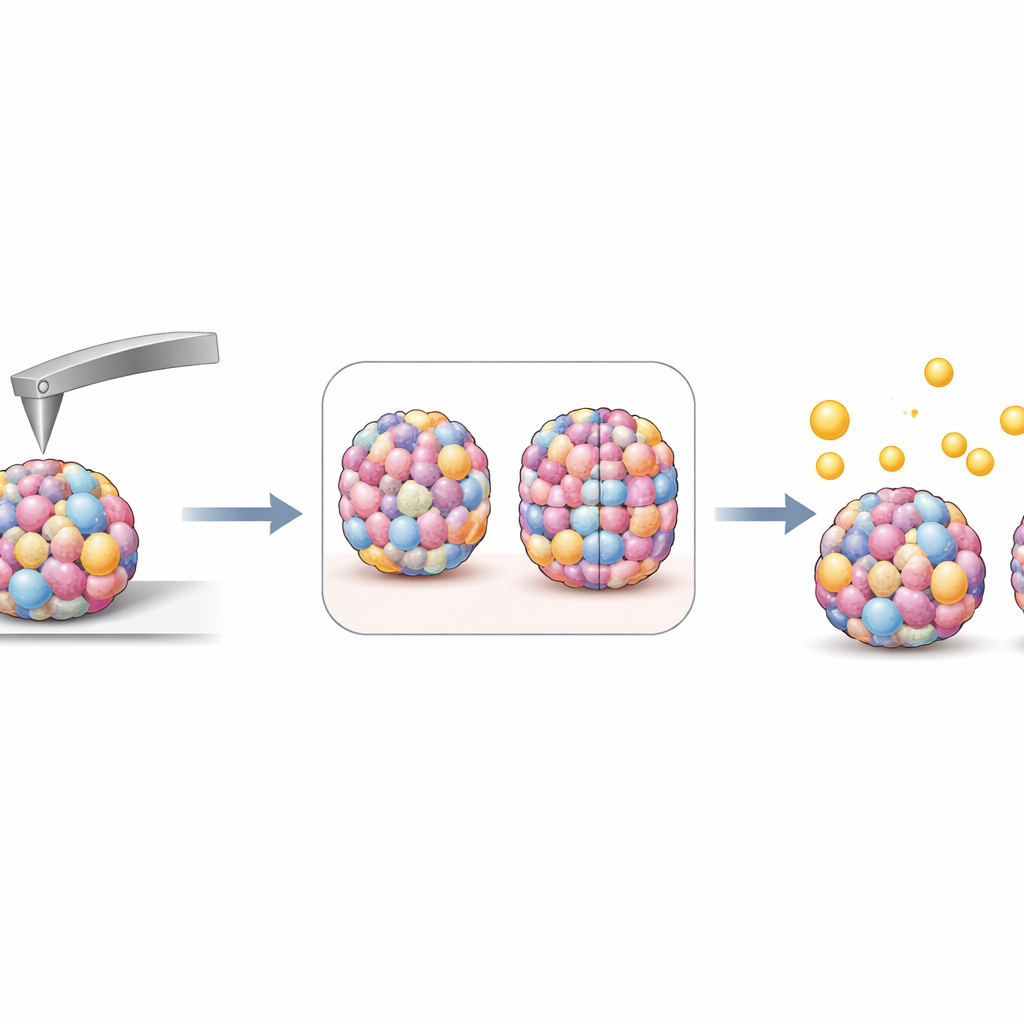
Qué significa esto para futuros estudios sobre cáncer y contaminación
El trabajo muestra que la rigidez es un parámetro informativo adicional para describir modelos cancerosos tridimensionales que por lo demás parecen similares en tamaño y forma. La forma en que las células se organizan dentro del esferoide y la rapidez con la que se dividen solo explican parcialmente estas diferencias mecánicas, lo que sugiere que la rigidez captura aspectos ocultos de la biología tumoral. Aunque este estudio no encontró una regla directa que vincule la rigidez del esferoide con la captación de microplásticos a niveles realistas de partículas, pone de manifiesto que, bajo condiciones suaves y en movimiento, sólo un número pequeño de tales partículas es probable que se adhieran a tejidos semejantes a tumores. A largo plazo, combinar mediciones detalladas de rigidez con métodos de seguimiento de partículas más sensibles podría ayudar a los investigadores a predecir mejor cómo responden los tumores tanto a fármacos anticancerígenos como a contaminantes ambientales que alcanzan los pulmones.
Cita: Kolesnik, T., Öhlinger, K., Absenger-Novak, M. et al. Role of atomic force microscopy in characterization of heterotypic cancer spheroids and their interaction with microplastic particles. Sci Rep 16, 8303 (2026). https://doi.org/10.1038/s41598-026-39445-z
Palabras clave: esferoides de cáncer de pulmón, microscopía de fuerza atómica, rigidez celular, microplásticos, microambiente tumoral