Clear Sky Science · es
Descubrimiento de compuestos antivirales potenciales y aceleración del hallazgo terapéutico contra el virus de la viruela del mono
Por qué esta investigación importa ahora
La viruela del mono, ahora con frecuencia denominada mpox, ha pasado de ser una infección tropical rara a una preocupación global, con brotes reportados en varios continentes en los últimos años. A diferencia de la COVID-19, todavía no existe un fármaco diseñado específicamente para detener este virus. Este estudio utiliza herramientas informáticas avanzadas para buscar nuevas moléculas pequeñas que puedan desactivar al virus donde más le perjudica: su capacidad para ocultarse de nuestro sistema inmune. Si se confirman en el laboratorio, estos compuestos candidatos podrían convertirse en el punto de partida para una nueva clase de medicamentos antivirales.
Cómo el virus se oculta de nuestras defensas
La viruela del mono pertenece a la misma familia ampliada que la viruela, y utiliza un truco inteligente para eludir al sistema inmunitario. Nuestras células liberan una proteína de señalización llamada interferón-gamma, que normalmente alerta a las células vecinas y activa defensas antivirales. Sin embargo, el virus produce su propia proteína secretada, denominada B8R, que flota fuera de las células infectadas. B8R imita de forma muy cercana al receptor humano del interferón-gamma y captura estas señales inmunes antes de que lleguen a su verdadero blanco. En efecto, actúa como una esponja, absorbiendo los mensajes de alarma del organismo e impidiendo una respuesta antiviral completa.
Usar ordenadores para diseñar tratamientos más inteligentes
El descubrimiento tradicional de fármacos puede llevar muchos años y recursos enormes. Aquí, los investigadores recurren al diseño asistido por ordenador para acelerar el proceso. Dado que no existe una estructura 3D experimental de la proteína B8R, primero utilizaron herramientas basadas en AlphaFold para predecir su forma atómica y comprobaron cuidadosamente la calidad de ese modelo. Con una estructura 3D fiable en mano, realizaron un cribado virtual de una biblioteca química de 5000 moléculas pequeñas. Se aplicaron reglas que describen lo que suele convertir una molécula en un fármaco tipo píldora (como tamaño, forma y solubilidad) para filtrar los candidatos pobres, dejando 2890 compuestos prometedores para pruebas detalladas contra el modelo de la proteína B8R.
Encontrar una “llave” química prometedora
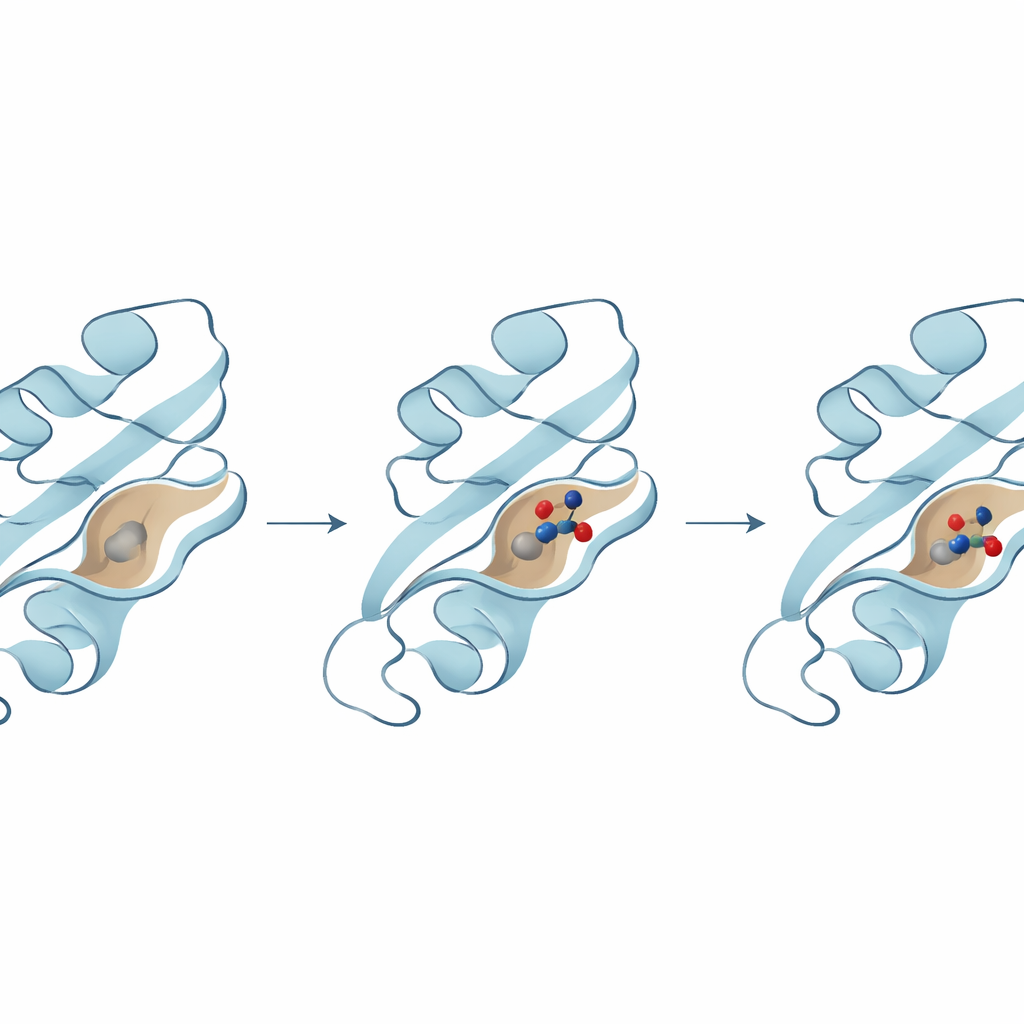
El siguiente paso fue ver qué moléculas podían encajar estrechamente en un bolsillo importante de la superficie de B8R, donde normalmente interactúa con el interferón-gamma. El equipo usó acoplamiento molecular (docking), una técnica que prueba miles de millones de posibles posiciones para una molécula en el bolsillo de la proteína y puntúa la afinidad de unión. Surgieron tres candidatos principales, cada uno previsto para formar interacciones fuertes con aminoácidos clave en el bolsillo. Un compuesto en particular mostró la mayor energía de unión y estableció varios contactos estabilizadores con residuos críticos que ayudan a anclarlo en su lugar, lo que sugiere que podría ser especialmente eficaz para bloquear la actividad de B8R.
Observar cómo se mueven las moléculas en el tiempo
Las proteínas y las moléculas farmacológicas no son rígidas; se mueven, se flexionan y "respiran" en su entorno acuoso. Para capturar esto, los investigadores realizaron largas simulaciones de dinámica molecular —películas virtuales de cientos de nanosegundos— para ver cómo se comportaba cada pareja proteína–compuesto a lo largo del tiempo. Estas simulaciones revelaron que el compuesto de mejor rendimiento permanecía profundamente enterrado en el bolsillo de B8R, con la proteína ajustándose ligeramente a su alrededor mientras mantenía estabilidad estructural. En contraste, los otros dos compuestos vagaron más, se desplazaron a bolsillos alternativos o mostraron mayores fluctuaciones, lo que sugiere una unión más débil o menos fiable. Análisis adicionales de flexibilidad, energía y movimientos a gran escala señalaron al mismo ganador: un compuesto que produjo de forma consistente el complejo más estable y energéticamente favorable.
Qué podría significar esto para tratamientos futuros
El estudio no afirma haber descubierto un fármaco terminado, y todavía no se han realizado experimentos en células ni en animales. En cambio, ofrece un punto de partida sólido y basado en datos: una molécula pequeña específica que parece tener la forma ideal para encajar en la proteína B8R de la viruela del mono y potencialmente restaurar el sistema de alarma por interferón del organismo. Al dirigirse a la estrategia de evasión inmune del virus en lugar de a su maquinaria de replicación, este enfoque ofrece un ángulo novedoso para la terapia antiviral. Los autores sostienen que su compuesto líder debería ahora probarse en el laboratorio, donde se puede medir directamente su capacidad para bloquear B8R y frenar la infección por mpox. Si esas pruebas tienen éxito, podría abrir el camino hacia un tratamiento dirigido que ayude al sistema inmunitario a ver y detener el virus con mayor eficacia.
Cita: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Palabras clave: antiviral viruela del mono, evasión inmune, descubrimiento de fármacos, modelado computacional, señalización por interferón