Clear Sky Science · es
Optimización de monocitos THP-1-CAR utilizando fagocitosis mediada por señalización de CD32a para la activación antigénica de linfocitos T
Enseñando nuevas habilidades al sistema inmunitario
Las terapias celulares modernas ya reprograman células inmunitarias para localizar y combatir el cáncer, pero la mayoría dependen de los linfocitos T, que pueden tener dificultades en el entorno hostil de los tumores sólidos. Este estudio se centra en cambio en otro defensor poderoso: los macrófagos, los “comedores” profesionales del organismo, y plantea cómo rediseñarlos para que no solo ingieran con mayor eficiencia células dañinas o virus, sino que también recluten linfocitos T para un ataque más duradero y específico. El trabajo revela reglas de diseño para construir mejores receptores de antígeno quiméricos (CAR) en macrófagos que podrían aplicarse tanto a infecciones como la COVID-19 como a tumores sólidos difíciles de tratar.
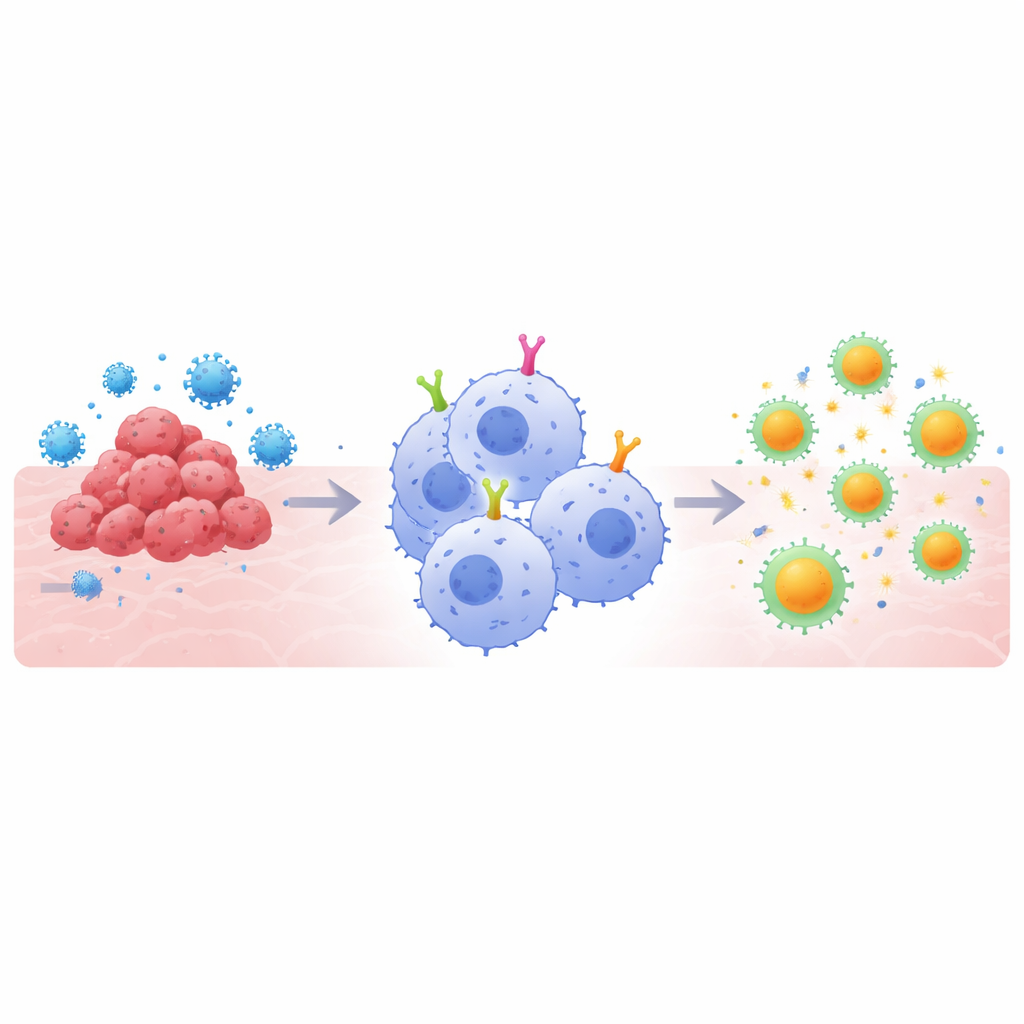
Por qué importan las células súper comedoras
Las terapias basadas en CAR funcionan equipando células inmunitarias con receptores superficiales a medida que reconocen un objetivo elegido, como una proteína tumoral o la espícula de un virus. Las versiones en linfocitos T han transformado el tratamiento de ciertos cánceres hematológicos, pero encuentran obstáculos frente a los tumores sólidos y en algunas infecciones. Los macrófagos ofrecen un ángulo distinto: naturalmente engullen amenazas y las descomponen en fragmentos que pueden presentarse a los linfocitos T, conectando los componentes “innato” y “adaptativo” de la inmunidad. Sin embargo, la mayoría de diseños de CAR se crearon originalmente para linfocitos T, no para macrófagos. Los autores razonaron que, para aprovechar plenamente las fortalezas de los macrófagos, las partes internas de señalización de los CAR —los segmentos que indican a la célula qué hacer una vez que se une un objetivo— tendrían que adaptarse específicamente a estas células comidasoras.
Encontrando el mejor cableado interno
El equipo comparó sistemáticamente varios dominios de señalización internos dentro de CARs introducidos en una línea celular humana de monocitos (THP‑1) que puede diferenciarse en macrófagos. Se centraron en dominios procedentes de receptores que normalmente impulsan la fagocitosis y la inflamación: CD3ζ (el módulo clásico de linfocitos T), CD32a (un receptor que se une a objetivos recubiertos por anticuerpos), componentes de CR3 CD11b y CD18 (receptores clave del complemento) y TLR4 (un sensor de peligro microbiano). Usando perlas y pseudovirus recubiertos con la proteína espícula de SARS‑CoV‑2, midieron qué tan bien cada diseño de CAR permitía a las células engullir objetivos, producir moléculas inflamatorias y, posteriormente, activar linfocitos T CD8 humanos que habían visto previamente el virus. Después transfirieron los diseños más prometedores a CARs dirigidos contra la mesotelina, una proteína sobreproducida en muchos tumores sólidos, para comprobar si las mismas reglas se aplicaban en un contexto tumoral.
Construyendo mejores comedores y amplificadores de señal
Surgió un patrón claro: los CAR basados en CD32a impulsaron de forma consistente una fagocitosis más fuerte y rápida que aquellos que usaban el dominio convencional CD3ζ, a pesar de que CD3ζ contiene más motivos clásicos de activación. En otras palabras, el “encaje” entre la señal y la maquinaria del macrófago importó más que la intensidad de la señal per se. Añadir fragmentos derivados de CR3 (CD11b o CD18) sobre CD32a no aumentó en la mayoría de condiciones la capacidad de ingestión, pero sí elevó los niveles de citocinas inflamatorias clave como TNF‑α e IL‑1β. Las combinaciones que incluían TLR4 fueron aún más allá en el aumento de señales inflamatorias y del marcador de superficie CD86, asociado con la capacidad de estimular linfocitos T, aunque esto conllevó compensaciones: niveles más bajos de CAR en la superficie celular y una fagocitosis algo reducida.
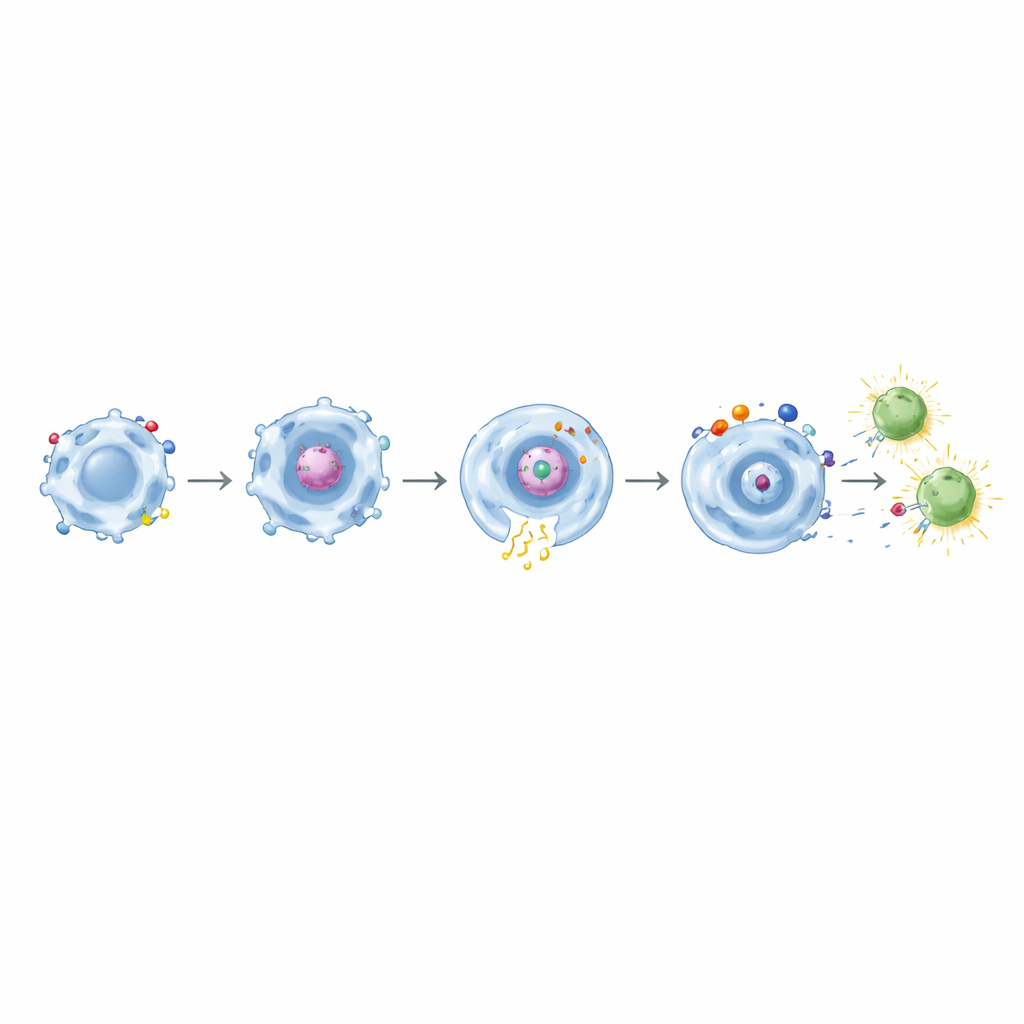
De comer a enseñar a los linfocitos T
De forma crucial, tras engullir la proteína espícula, los macrófagos portadores de CARs basados en CD32a fueron capaces de activar linfocitos T CD8 de memoria de personas previamente vacunadas contra la COVID‑19. Estos linfocitos T mostraron marcadores tempranos de activación y produjeron moléculas efectoras como interferón‑γ y TNF‑α. El efecto se fortaleció aún más con CARs de doble dominio que combinaban CD32a con CD11b, CD18 o TLR4. Cuando diseños similares dirigidos contra la mesotelina se probaron frente a células tumorales diseñadas, mostraron nuevamente fagocitosis precisa dependiente del objetivo combinada con una mayor señalización inflamatoria. De entre ellos, la combinación CD32a+TLR4 destacó como una poderosa “alarma tisular”, incrementando de forma más efectiva la secreción de citocinas y CD86 mientras mantenía la ingestión tumoral específica.
Qué podría significar esto para tratamientos futuros
Para un observador no especializado, este estudio muestra que diseñar macrófagos no es un problema de talla única. Al intercambiar y combinar módulos internos de señalización, los científicos pueden moldear células que se centren ya sea en la eliminación eficiente de células enfermas o en actuar como amplificadores inmunitarios que reconfiguran el entorno supresor del tumor y reclutan linfocitos T. Los CARs basados en CD32a surgieron como una base sólida para tales diseños, superando a los módulos tradicionales de linfocitos T en macrófagos y funcionando tanto con objetivos virales como tumorales. Aunque estos resultados provienen de modelos de laboratorio y deberán confirmarse en células humanas primarias y animales, proporcionan un plano para terapias de próxima generación con CAR‑macrófagos que podrían abordar mejor tumores sólidos e infecciones persistentes al unir una rápida fagocitosis con activación precisa de linfocitos T.
Cita: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Palabras clave: macrófagos CAR, señalización CD32a, fagocitosis, inmunoterapia de tumores sólidos, activación de linfocitos T