Clear Sky Science · es
El paisaje de metilación del ADN en killifish de vida naturalmente corta
Peces diminutos con grandes pistas sobre el envejecimiento
¿Por qué algunos animales recorren la vida a toda prisa mientras otros se mantienen durante años? Este estudio aborda ese enigma usando killifish anuales, diminutos peces africanos que viven solo unos meses pero muestran muchos de los mismos signos de envejecimiento que los humanos. Al cartografiar cómo cambian con el tiempo las marcas químicas en su ADN, los investigadores preguntan si estos peces de vida corta siguen los mismos patrones de envejecimiento «epigenético» observados en personas y otros mamíferos —y si esos patrones podrían algún día ayudar a predecir la salud y la longevidad en un animal de laboratorio sencillo.
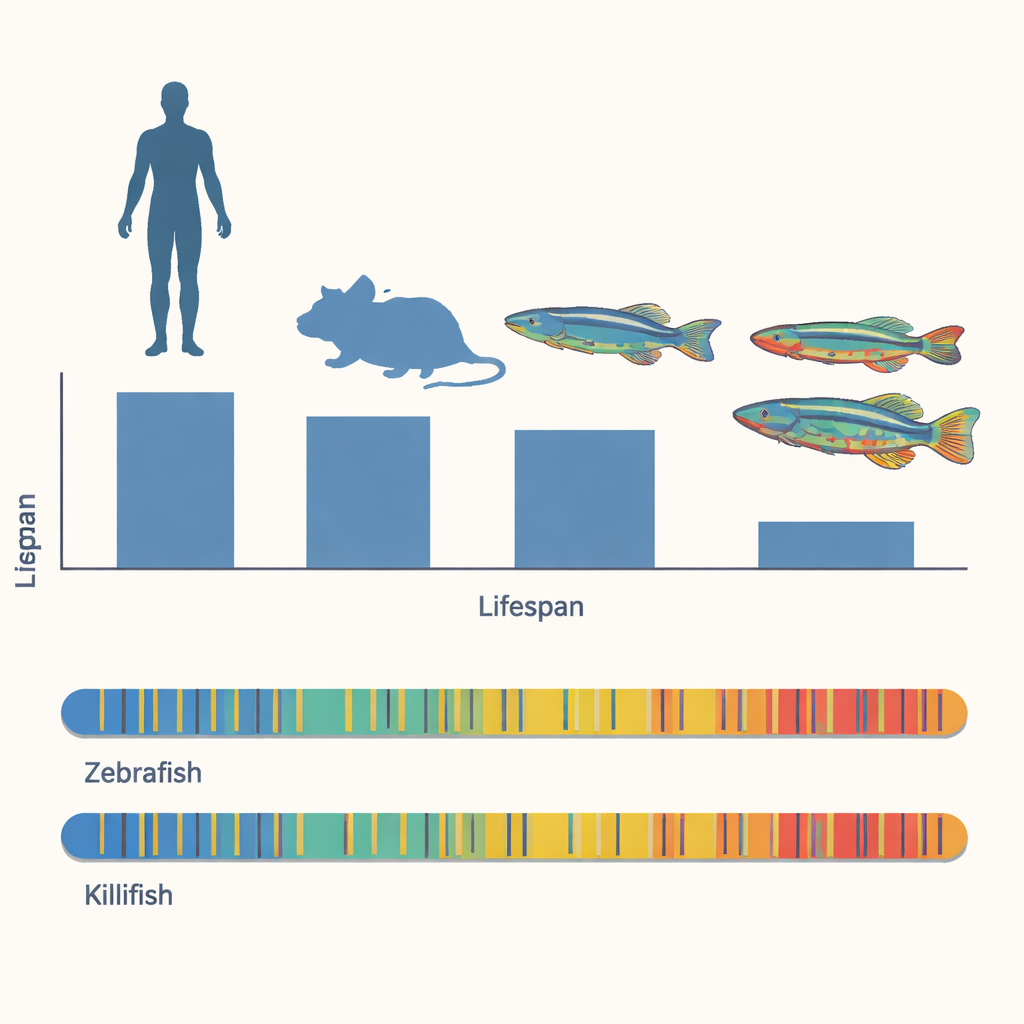
Vidas cortas en un mundo impredecible
Los killifish anuales han evolucionado para sobrevivir en charcas temporales que aparecen durante la estación de lluvias y desaparecen poco después. Sus huevos esperan en el barro seco y, cuando vuelve el agua, eclosionan y crecen a una velocidad notable. Una especie, Nothobranchius furzeri, suele vivir solo de tres a seis meses; su pariente cercano N. orthonotus puede alcanzar alrededor de diez meses en condiciones similares. Ambas especies desarrollan señales familiares de envejecimiento: fertilidad reducida, natación más lenta, cambios en el color de la piel y los ojos, problemas de memoria, declive inmunitario, desequilibrio intestinal y tumores. Como estos cambios ocurren en menos de un año, los peces ofrecen una oportunidad rara para estudiar la biología del envejecimiento en cámara rápida.
Mirando más allá del plano genético
Los investigadores quisieron saber si el envejecimiento rápido del killifish está escrito en la estructura de su genoma o, en cambio, en cómo se regula ese genoma. Primero compararon rasgos genómicos básicos de los dos killifish con los de humanos, ratones, pez cebra y el nematodo C. elegans. A pesar de sus vidas mucho más cortas, los genomas de los killifish son similares en tamaño y disposición génica a los del pez cebra. Ambos peces dedican alrededor de la mitad de su ADN a secuencias repetitivas, especialmente elementos genéticos móviles conocidos como elementos transponibles, y muestran distribuciones comparables de las letras del ADN donde los grupos metilo —las marcas químicas en cuestión— pueden unirse. Estas similitudes generales sugieren que la vida corta del killifish no puede explicarse simplemente por tener un genoma más pequeño o más compacto.
Marcas de ADN que cambian con el tejido y el tiempo
Para sondear la regulación en lugar de la secuencia cruda, el equipo produjo mapas de alta resolución de la metilación del ADN —el patrón de grupos metilo unidos a bases de citosina— a lo largo de los genomas completos de ambas especies. Analizaron cerebro, hígado y corazón de N. furzeri jóvenes y viejos, y cerebros de N. orthonotus jóvenes, viejos y muy viejos. En conjunto, el paisaje de metilación del killifish se parecía al de los mamíferos: la mayoría de los sitios estaban o bien muy marcados o apenas marcados, y las regiones cercanas al inicio de los genes tendían a tener menos marcas. Las diferencias entre tejidos fueron mucho más pronunciadas que las diferencias entre edades. Cerebro, hígado y corazón presentaron firmas de metilación distintas, y las regiones con baja metilación específicas del cerebro a menudo se ubicaban cerca de genes importantes para la identidad de las neuronas, lo que sugiere que estos patrones ayudan a definir y mantener la función de cada órgano.
Huellas sutiles del envejecimiento y ADN móvil
Los cambios relacionados con la edad estaban presentes pero eran modestos. A lo largo del genoma en su conjunto, los niveles de metilación se mantuvieron en gran medida estables con la edad en ambas especies de killifish. Sin embargo, una inspección más detallada reveló miles de regiones específicas donde la metilación sí cambió entre animales jóvenes y viejos. Muchos de estos cambios ocurrieron dentro o cerca de elementos transponibles —las secuencias de ADN móviles que constituyen una gran fracción del genoma del killifish. Diferentes tejidos mostraron conjuntos parcialmente superpuestos de elementos sensibles a la edad, lo que sugiere efectos de envejecimiento tanto compartidos como específicos por órgano. En el más longevo N. orthonotus, los análisis detallados del cerebro identificaron grupos de sitios de metilación cuyos niveles cambiaban de forma correlacionada con la edad del pez, y estos sitios pudieron combinarse en un modelo estadístico que predijo, de manera aproximada, si un individuo era joven, viejo o muy viejo.
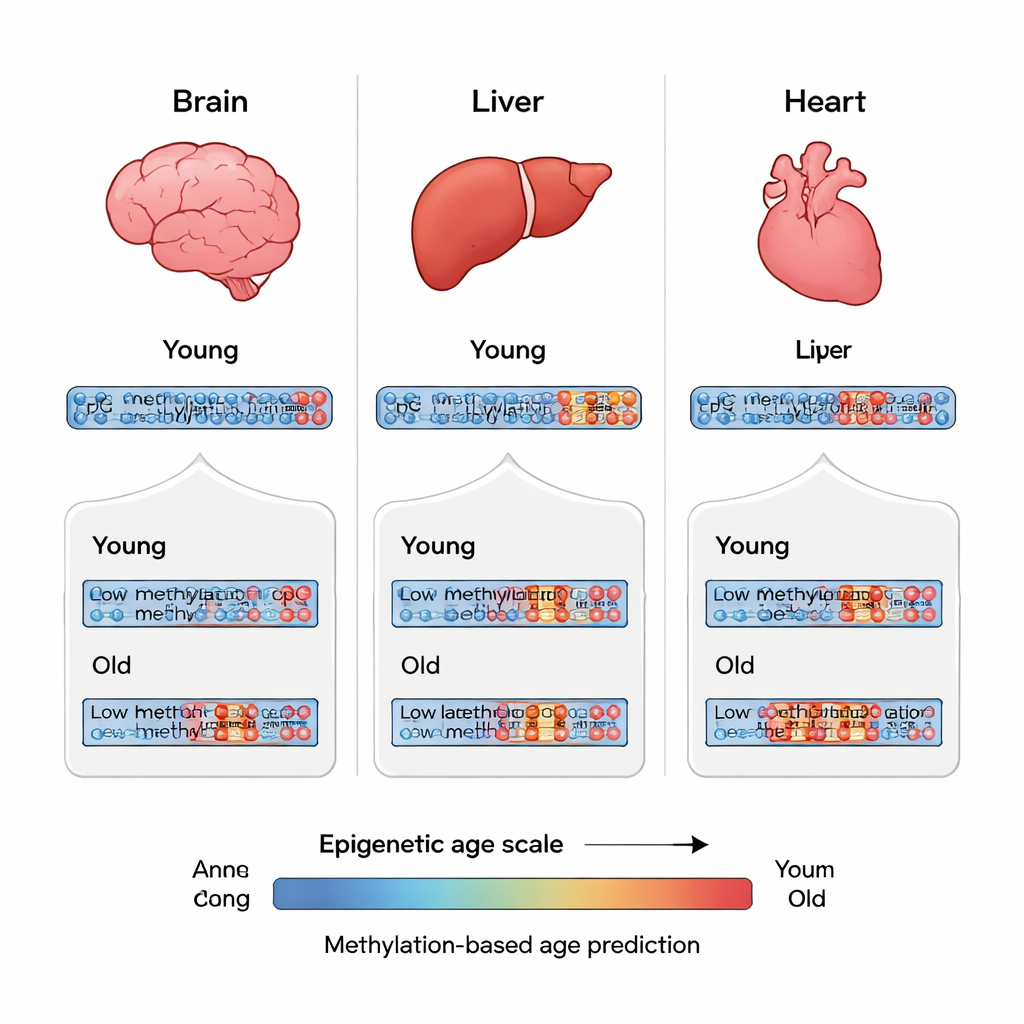
Lo que estos peces diminutos nos dicen sobre envejecer
El estudio demuestra que incluso en un vertebrado que vive solo meses hay cambios reconocibles en la metilación del ADN conforme los animales envejecen, de manera similar a los utilizados para construir «relojes epigenéticos» en humanos y ratones. Aun así, los cambios en los killifish son relativamente pequeños y están repartidos por muchos sitios en lugar de concentrarse en unas pocas vías clave. Esto puede reflejar la vida comprimida de estos peces: puede haber menos tiempo para que la deriva epigenética gradual se acumule. Al ofrecer los primeros mapas de metilación completos para killifish anuales, el trabajo sienta las bases esenciales para convertir a estos animales en un sistema rápido y flexible para probar cómo los genes, el entorno y posibles tratamientos influyen en el ritmo del envejecimiento biológico.
Cita: Steiger, M., Singh, N., Tyers, A.M. et al. The DNA methylation landscape of naturally short-lived killifish. Sci Rep 16, 7173 (2026). https://doi.org/10.1038/s41598-026-39352-3
Palabras clave: envejecimiento epigenético, metilación del ADN, killifish anual, elementos transponibles, biología de la longevidad