Clear Sky Science · es
FAM120A: una proteína integrada en la red de la enfermedad ELA
Por qué esto importa para las personas y las familias
La esclerosis lateral amiotrófica (ELA) es una enfermedad devastadora que paraliza progresivamente a las personas al matar las células nerviosas que controlan el movimiento. Hoy todavía no comprendemos completamente por qué mueren estas neuronas motoras, y los tratamientos eficaces siguen siendo escasos. Este estudio arroja luz sobre una proteína poco conocida, llamada FAM120A, y sugiere que podría ayudar a las células nerviosas a lidiar con el estrés y a prevenir la acumulación de agregados proteicos dañinos, una característica distintiva de la ELA. Al desvelar cómo se comporta esta proteína durante la enfermedad, el trabajo abre una vía nueva para entender y, quizás eventualmente, tratar la ELA.
Encontrar un actor oculto en una red génica concurrida
Los investigadores no empezaron en el banco de laboratorio sino en el ordenador. Emplearon un enfoque de “análisis convergente” para combinar muchos conjuntos de datos existentes sobre genes vinculados a la ELA y sus interacciones. Esta visión en forma de red les permitió ver conglomerados de proteínas que trabajan juntas en procesos celulares clave, especialmente los relacionados con el manejo del ARN y el control de la calidad de las proteínas —ambos puntos problemáticos conocidos en la ELA. Dentro de uno de esos conglomerados, FAM120A emergió como una proteína previamente ignorada pero altamente conectada que interactúa con varias proteínas ya relacionadas con la ELA. Sus funciones conocidas en ayudar a las células a sobrevivir al estrés oxidativo y en la gestión del ARN la convirtieron en una candidata sólida para un estudio más profundo.
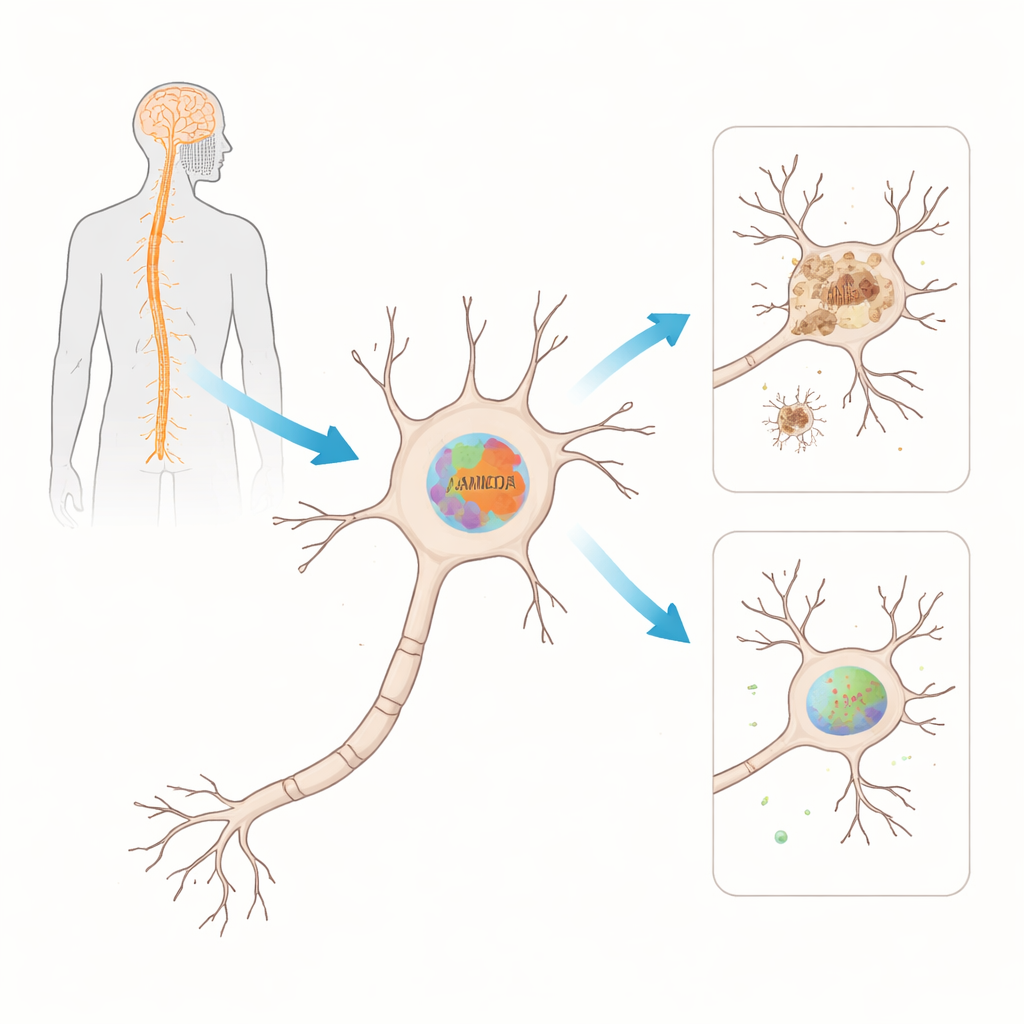
Seguir una proteína vulnerable durante la progresión de la enfermedad
Para comprobar si FAM120A realmente importa en la ELA, el equipo recurrió a un modelo de ratón ampliamente utilizado que porta una versión mutante del gen SOD1, una de las primeras causas genéticas identificadas en la ELA. Midieron tanto los mensajes de ARN como los niveles de la proteína de la versión murina, Fam120A, en la médula espinal a lo largo del tiempo, desde antes de que aparecieran los síntomas hasta las fases avanzadas de la enfermedad. Al principio, los niveles de ARN de Fam120A cayeron en la médula espinal antes de que los animales mostraran signos claros de enfermedad. Más tarde, a medida que se desarrolló la parálisis, la propia proteína Fam120A se redujo de forma marcada. Este desfase —el ARN cambia primero y la proteína después— sugiere que varios niveles de regulación se desmoronan conforme avanza la enfermedad.
Dónde se localiza esta proteína en la médula espinal
A continuación, los científicos preguntaron dónde se encuentra exactamente Fam120A en la médula espinal. Usando microscopía fluorescente en cortes de tejido, observaron que Fam120A está presente principalmente en las neuronas del asta ventral —la región rica en neuronas motoras que degeneran en la ELA. En animales en fase avanzada de la enfermedad vieron cierto señal en células de soporte llamadas astrocitos, pero el patrón dominante siguió siendo neuronal. Estas observaciones vinculan a Fam120A directamente con las mismas células que fallan en la ELA y respaldan la idea de que su pérdida podría debilitar su capacidad para manejar el estrés celular, contribuyendo posiblemente al deterioro de la función motora.
Poner FAM120A extra a trabajar en células tipo nervio
El equipo pasó luego a células cultivadas de tipo nervioso para explorar qué hace FAM120A. Diseñaron estas células para producir SOD1 normal o mutante, que tiende a formar agregados tóxicos, y después forzaron a las células a producir FAM120A humano en exceso. Cuando estaba presente la SOD1 mutante, aumentar FAM120A redujo de forma significativa tanto la cantidad de SOD1 insoluble detectada por pruebas bioquímicas como el número de agregados visibles al microscopio. Es importante que FAM120A tuvo poco efecto sobre la forma normal de SOD1, lo que sugiere que podría ayudar específicamente a las células a manejar proteínas mal plegadas o con tendencia a agregarse, un problema central en la ELA y en otras enfermedades neurodegenerativas.
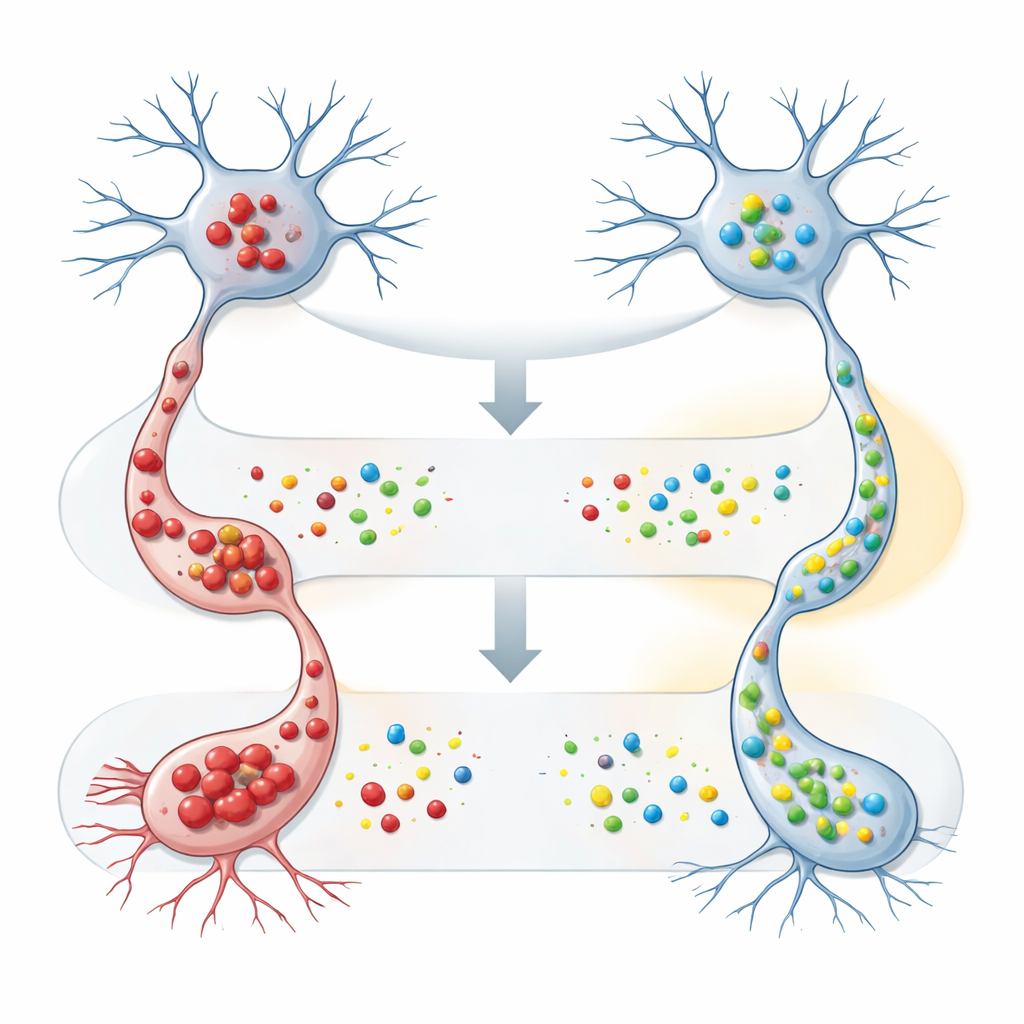
Construir un mapa más amplio de aliados y enemigos moleculares
Más allá de estos experimentos, los investigadores exploraron la red de interacción más amplia de FAM120A. Confirmaron que se asocia físicamente con PURA, una proteína de unión al ARN ya vinculada al desarrollo cerebral y la neurodegeneración, y hallaron que los niveles de PURA también disminuyen en la médula espinal del ratón con ELA, aunque más tarde en la enfermedad. Destacan vínculos adicionales entre FAM120A, su gen antisentido asociado FAM120Aos y otra proteína de unión al ARN, ELAVL1, que regula genes de inflamación y respuesta al estrés en el cerebro. Esta red en expansión sitúa a FAM120A en la encrucijada de la regulación del ARN, las respuestas al estrés y el control de la calidad proteica —precisamente los sistemas que fallan en la ELA.
Qué podría significar esto para futuros tratamientos de la ELA
En conjunto, los hallazgos sugieren que FAM120A no es solo un figurante sino una parte significativa de la red de la enfermedad ELA. Su declive temprano en neuronas motoras vulnerables, sus vínculos físicos con otras proteínas reguladoras del ARN y su capacidad para reducir los agregados tóxicos de SOD1 en células apuntan a un papel protector en el mantenimiento del equilibrio proteico. Aunque queda mucho trabajo por hacer —especialmente para ver si cambios similares ocurren en personas con ELA y en otros modelos de la enfermedad—, FAM120A destaca ahora como un objetivo prometedor para estudios futuros y, potencialmente, para terapias destinadas a preservar la salud de las neuronas motoras.
Cita: Vicencio, E., Gomez, L., Beltran, S. et al. FAM120A - a protein inserted in the ALS disease network. Sci Rep 16, 8200 (2026). https://doi.org/10.1038/s41598-026-39329-2
Palabras clave: esclerosis lateral amiotrófica, neuronas motoras, agregación de proteínas, proteínas de unión al ARN, neurodegeneración