Clear Sky Science · es
Toxicología de redes integrativa y evidencia experimental revelan mecanismos subyacentes al inicio y progresión del cáncer de endometrio inducidos por ftalato de dietilo
Químicos cotidianos y el riesgo de cáncer en mujeres
Los plastificantes están entretejidos en la vida moderna, presentes en envases, cosméticos y dispositivos médicos. Uno de ellos, el ftalato de dietilo (DEP), es tan omnipresente que su producto de degradación puede detectarse en la orina de la mayoría de las personas. Al mismo tiempo, las tasas de cáncer de endometrio —un cáncer del revestimiento uterino— han ido en aumento a nivel mundial. Este estudio plantea una pregunta de gran relevancia para quien se preocupa por la salud ambiental: ¿podría la exposición prolongada al DEP estar empujando de forma silenciosa a las células del útero hacia el cáncer y, de ser así, cómo?
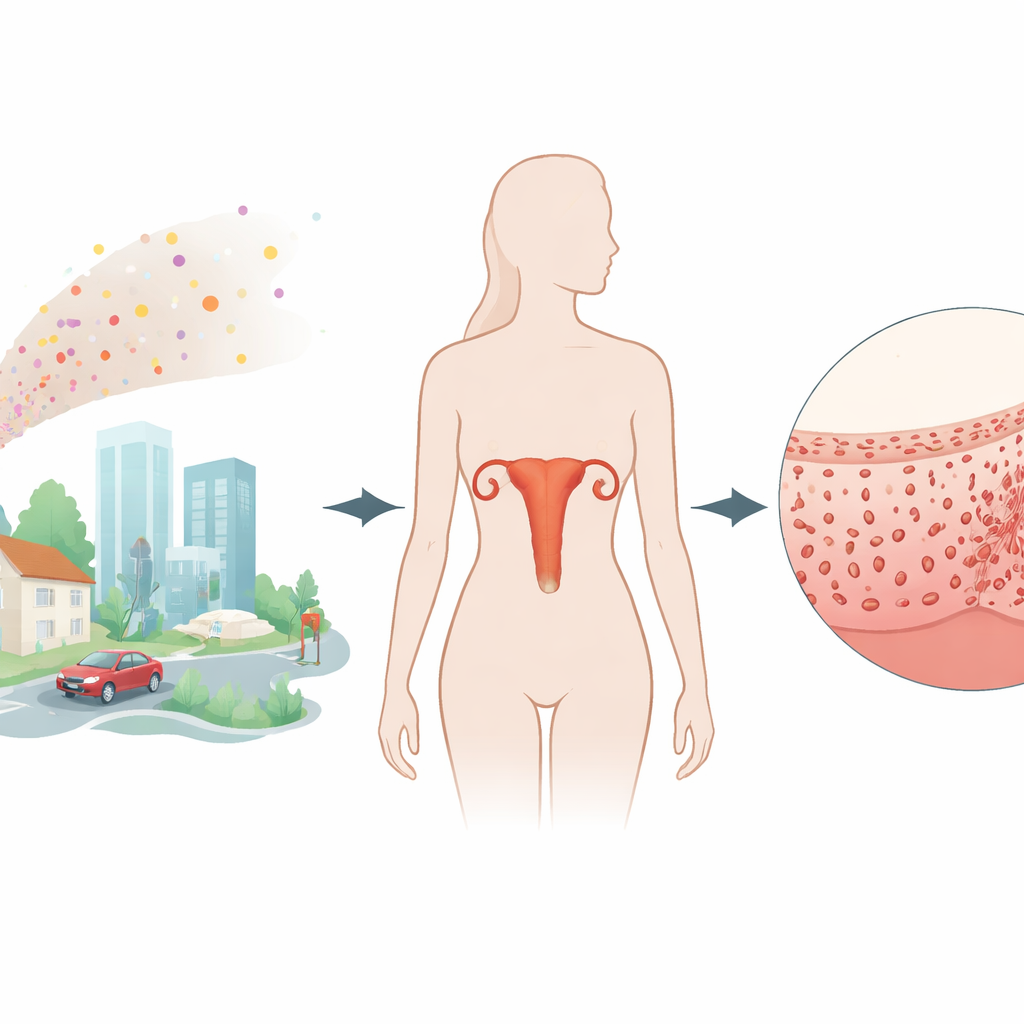
Cómo conectó el estudio la exposición con la enfermedad
Los investigadores empezaron mediante el minado de grandes bases de datos públicas que contienen perfiles de actividad génica de tejidos de cáncer de endometrio y de revestimiento uterino sano. Al comparar miles de genes a la vez, identificaron qué genes mostraban consistentemente mayor o menor actividad en el cáncer. Luego superpusieron ese mapa con un segundo: una lista de genes humanos que bases de datos químicas y herramientas predictivas previas sugieren que podrían interactuar con el DEP. Donde esos dos mapas se solaparon, hallaron 19 genes que se sitúan en la encrucijada entre la exposición al DEP y el cáncer de endometrio, lo que apunta a un vínculo mecanístico entre un químico cotidiano y el desarrollo tumoral.
Algoritmos inteligentes para encontrar los genes más críticos
Clasificar 19 genes candidatos sigue siendo una tarea exigente, por lo que el equipo recurrió al aprendizaje automático. Entrenaron y probaron más de 100 modelos predictivos distintos sobre conjuntos de datos combinados de pacientes para ver qué conjuntos de genes podían distinguir mejor el tejido canceroso del tejido normal. Empleando un método de interpretabilidad llamado SHAP, que revela cuánto cada gen "empuja" una predicción hacia el estado canceroso o saludable, ordenaron los candidatos. Cinco genes —FOS, JUN, NR4A1, ADRA2C y SLC6A2— emergieron como actores centrales, cada uno mostrando por separado una gran capacidad para separar muestras cancerosas de no cancerosas, y juntos formando una huella de cambios relacionados con el DEP en el revestimiento uterino.
Acercándose a los encuentros químico–proteína
Para investigar si el DEP podría unirse físicamente a las proteínas codificadas por esos genes, los investigadores utilizaron acoplamiento molecular y largas simulaciones computacionales del movimiento atómico. Estos análisis sugirieron que el DEP encaja en cavidades de varias de las proteínas, en particular ADRA2C, NR4A1 y SLC6A2, formando complejos estables a lo largo del tiempo. Tales experimentos virtuales no prueban por sí solos causalidad, pero refuerzan la idea de que el DEP puede unirse directamente a proteínas controladoras clave dentro o en la superficie de las células uterinas, potencialmente alterando su comportamiento en formas que favorecen el crecimiento tumoral.
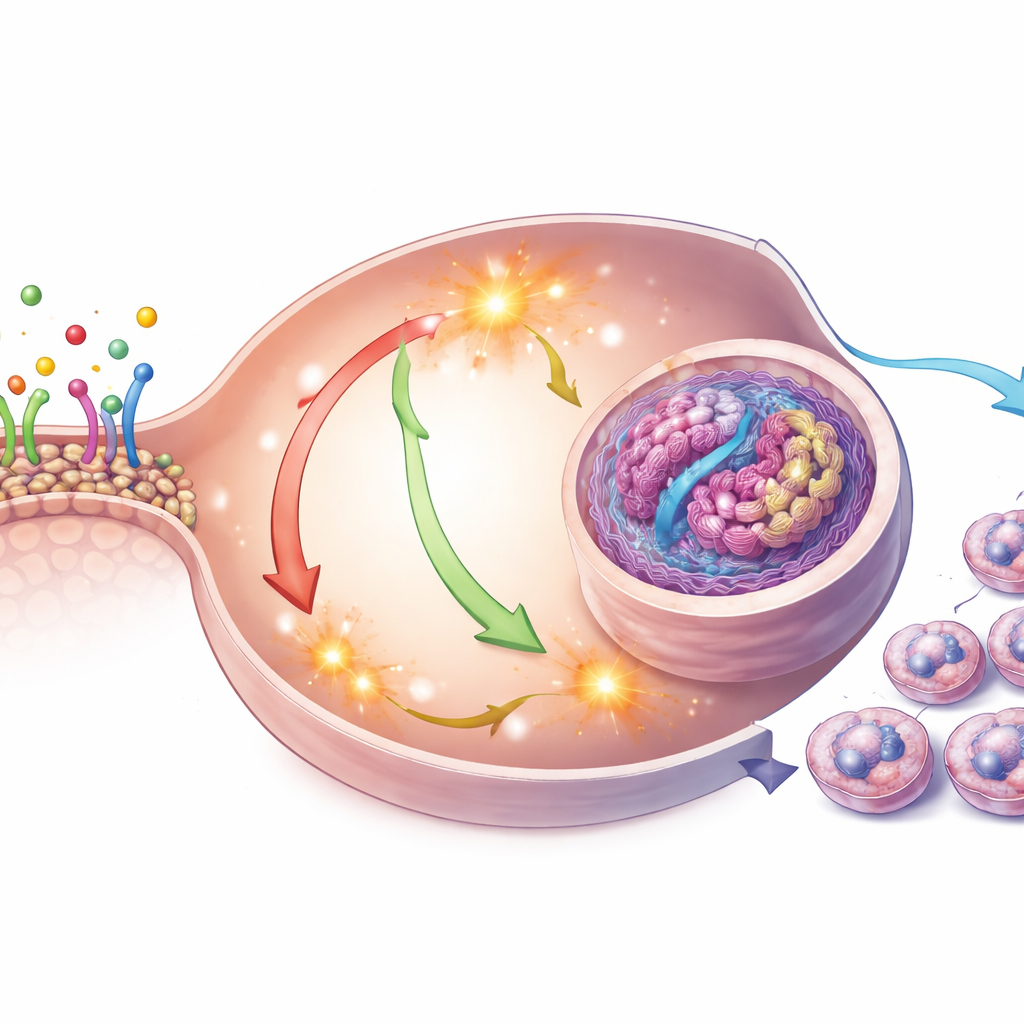
Qué ocurre dentro de las células uterinas
El equipo pasó entonces de los modelos computacionales a células vivas, exponiendo dos líneas celulares humanas de cáncer de endometrio al DEP en dosis seleccionadas para ser biológicamente activas pero no inmediatamente tóxicas. Encontraron que las células tratadas con DEP se multiplicaban más rápido e ingresaban con mayor facilidad en la fase de copia del ADN del ciclo celular. En el interior de estas células, aumentaron los niveles de especies reactivas de oxígeno —formas químicamente agresivas de oxígeno—, mientras que disminuyó una enzima antioxidante natural. Al mismo tiempo, las principales vías de control del crecimiento dentro de la célula, a menudo denominadas MAPK/ERK y PI3K/AKT, se activaron más. Esta activación coincidió con un aumento de Cyclin D1 y CDK4, dos proteínas que actúan como guardias que impulsan a las células desde un estado de reposo hacia la división activa.
Qué significa esto para la vida cotidiana
En conjunto, el estudio pinta un panorama multinivel: el DEP puede unirse a proteínas celulares específicas, desencadenar estrés oxidativo, activar circuitos de señalización que promueven el crecimiento y acelerar el ciclo celular en células de cáncer de endometrio. Para una persona no especializada, el mensaje es que un aditivo plástico común tiene el potencial de crear un terreno más "fértil" para el cáncer en el revestimiento uterino, especialmente en un organismo ya influido por hormonas y otros factores de riesgo. Aunque el trabajo se realizó en modelos celulares y aún requiere confirmación en animales y en humanos, subraya la importancia de escrutar las exposiciones químicas rutinarias y apoya los esfuerzos por reducir el contacto con compuestos disruptores endocrinos innecesarios.
Cita: Chen, X., Wang, Z., Wang, F. et al. Integrative network toxicology and experimental evidence reveal mechanisms underlying diethyl phthalate-induced initiation and progression of endometrial cancer. Sci Rep 16, 8066 (2026). https://doi.org/10.1038/s41598-026-39325-6
Palabras clave: cáncer de endometrio, ftalato de dietilo, disruptores endocrinos, toxicología ambiental, señalización celular