Clear Sky Science · es
Dinámica microbiológica y reológica de biopelículas mixtas formadas por bacterias y virus eucariotas
Comunidades ocultas en dispositivos hospitalarios
Muchas infecciones hospitalarias no empiezan con un solo germen, sino con comunidades viscosas e invisibles llamadas biopelículas que recubren catéteres y otros dispositivos médicos. Este estudio plantea una pregunta poco explorada pero con grandes implicaciones para la seguridad del paciente: ¿qué ocurre cuando no solo las bacterias, sino también virus que infectan a humanos, se integran juntos en esas biopelículas? Al observar cómo se comporta un virus mamífero común dentro de biopelículas bacterianas, los investigadores revelan cómo estas ciudades microbianas pegajosas podrían proteger silenciosamente a los virus y modificar su comportamiento.
Ciudades pegajosas de microbios
Las biopelículas son como ciudades microscópicas construidas por microbios sobre superficies húmedas: tuberías, rocas, dientes o tubos de plástico colocados en pacientes. Las bacterias se asientan, se multiplican y secretan una matriz similar a un pegamento que las protege contra la desecación, los químicos y el sistema inmune. En los hospitales, este tipo de biopelículas se forman comúnmente en catéteres urinarios y venosos, donde pueden originar infecciones del torrente sanguíneo e infecciones urinarias difíciles de tratar. Estas biopelículas suelen contener muchas especies distintas e incluso diferentes reinos de la vida, pero la mayor parte de la investigación se ha centrado en las bacterias por sí solas, dejando en gran medida sin explorar el papel de los virus.
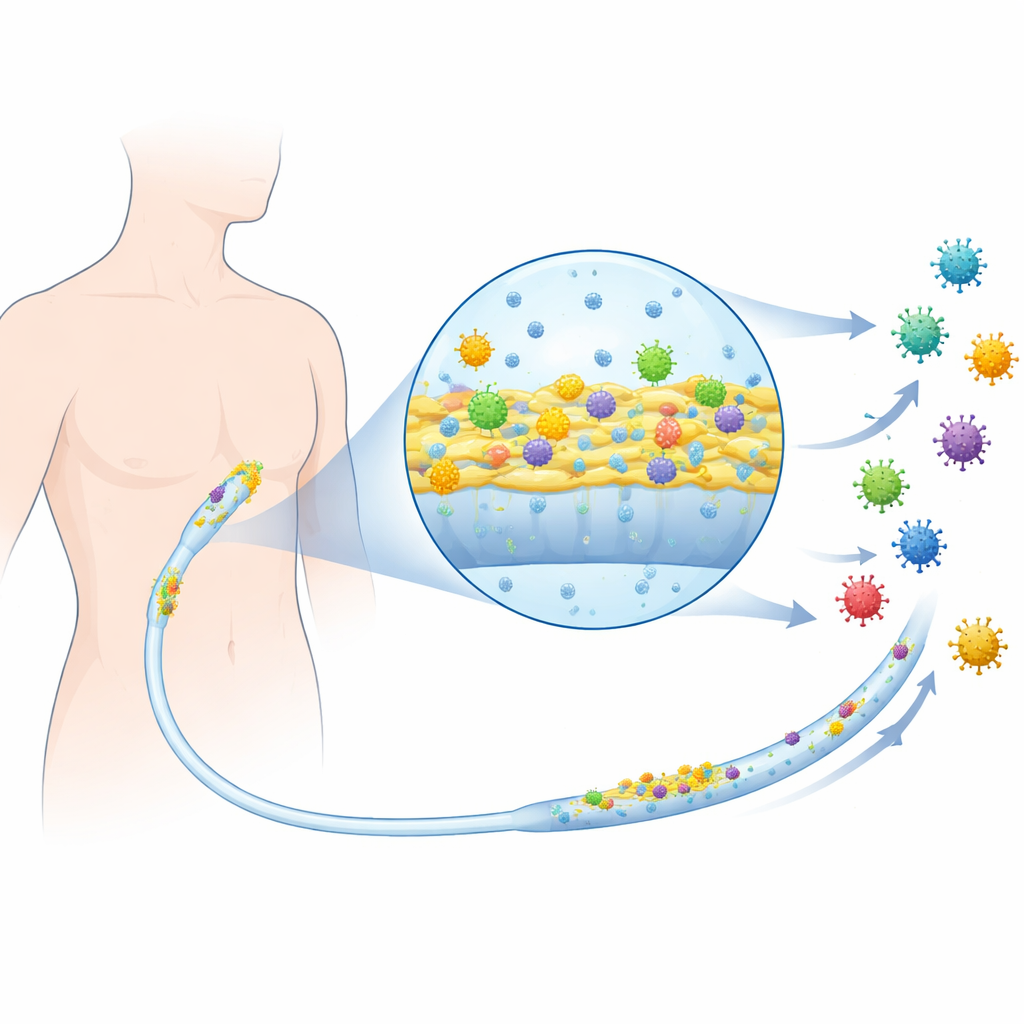
Introduciendo un virus mamífero en la mezcla
El equipo trabajó con cepas bacterianas clínicas que se sabe colonizan catéteres, incluyendo Escherichia coli uropatógena de infecciones urinarias y otras bacterias frecuentemente halladas en infecciones de vías centrales. A continuación introdujeron reovirus de mamífero, un virus no envuelto bien estudiado que infecta células animales, como sustituto de virus que infectan humanos de forma más general. Primero comprobaron si añadir material conteniendo virus afectaba al crecimiento bacteriano normal y libre. En muchas cepas, las bacterias crecieron y sobrevivieron igual con o sin el virus, demostrando que el virus no estaba matando directamente a las bacterias ni actuando como un antibiótico.
Las biopelículas cambian su textura, no su tamaño
Cuando las bacterias se establecen en biopelículas, la historia se volvió más matizada. En la mayoría de las cepas, la cantidad total de biopelícula —medida con una tinción estándar que cuantifica cuánto material recubre una superficie— apenas cambió en presencia del virus. Sin embargo, algunas cepas produjeron algo más o menos biopelícula según estuvieran presentes preparaciones virales, lo que insinúa efectos específicos por cepa. Para ir más allá de la mera cantidad, los investigadores recurrieron a herramientas de ciencia de materiales y midieron cuán “blanda” o “rígida” era cada biopelícula, de manera análoga a sondear la textura de un gel. Encontraron que cada cepa bacteriana formaba su propia firma mecánica. De forma importante, la adición de virus podía endurecer o ablandar esas biopelículas según la cepa: en una cepa de E. coli el virus volvió la matriz más rígida, mientras que en una cepa de Staphylococcus epidermidis el virus condujo a una estructura más débil y conforme.
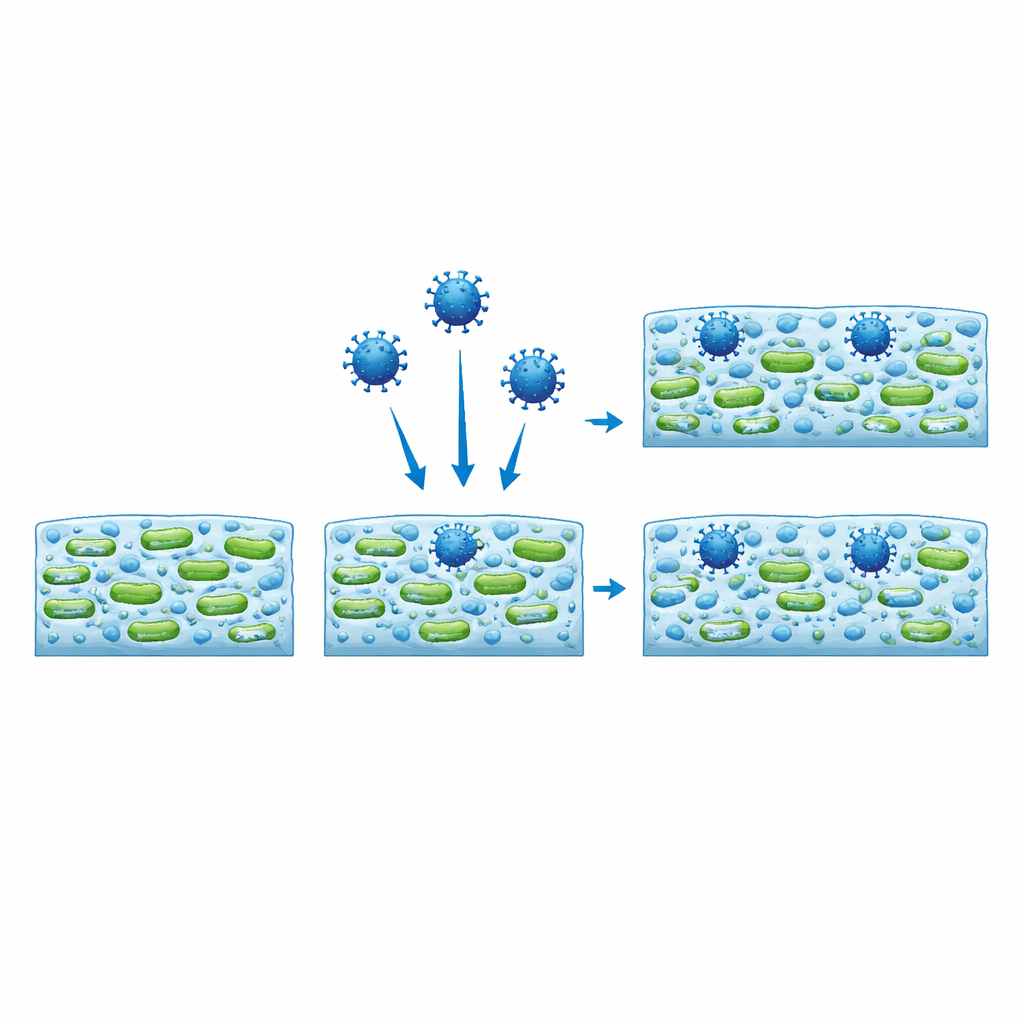
Los virus encuentran refugio y conservan su infectividad
Mediante microscopía de fluorescencia, los científicos marcaron las partículas virales para que brillaran y siguieron dónde acababan dentro de la biopelícula. A diferencia de las cuentas plásticas inertes de tamaño similar, que mayormente permanecían en regiones dispersas y eran arrastradas, los virus penetraron profundamente en la matriz y tendieron a agruparse donde las células bacterianas estaban más densas. En algunos casos, la presencia del virus incluso cambió la forma general de la biopelícula, transformando agregados compactos en redes más arácnidas o viceversa, dependiendo de la cepa bacteriana. Para comprobar si esos virus atrapados seguían siendo peligrosos, los autores los recuperaron de las biopelículas y los expusieron a células de mamífero. Los virus recuperados permanecieron infecciosos, a pesar de haber estado incrustados en la baba bacteriana durante dos días.
Por qué esto importa para los pacientes y más allá
Para un público general, el mensaje clave es que las biopelículas en dispositivos médicos pueden no solo proteger a las bacterias frente a los tratamientos, sino también ocultar y preservar virus que infectan células humanas o animales. El estudio muestra que los virus pueden alojarse dentro de la matriz bacteriana, alterar sutilmente la estructura de la biopelícula y, al mismo tiempo, mantener su capacidad de infectar nuevas células una vez liberados. Esto sugiere que los catéteres y otras superficies recubiertas por biopelículas podrían actuar como reservorios silenciosos donde los virus persisten, protegidos de la desecación, los desinfectantes y el ataque inmune. Comprender estas comunidades microbianas mixtas puede ser crucial para diseñar mejores materiales, estrategias de limpieza y terapias que apunten tanto a las bacterias como a sus colaboradores virales para reducir las infecciones asociadas a dispositivos que resultan persistentes.
Cita: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Palabras clave: biopelículas, infecciones por catéter, interacciones virus–bacteria, reovirus, comunidades microbianas