Clear Sky Science · es
Un modelo de física de polímeros del núcleo celular en interfase para simulaciones radiobiológicas
Por qué importa la forma de nuestro hogar del ADN
La radiación es una espada de doble filo en medicina: puede destruir células cancerosas, pero también dañar tejido sano. En el centro tanto de los riesgos como de los beneficios está nuestro ADN, empaquetado de forma muy compacta dentro del núcleo celular. Este artículo muestra cómo un modelo 3D detallado, inspirado en la física, de esa “ciudad del ADN” nuclear puede ayudar a los científicos a predecir cómo la radiación fragmenta y repara incorrectamente los cromosomas, con potencial para mejorar el tratamiento del cáncer y las estimaciones de riesgo por la radiación espacial.
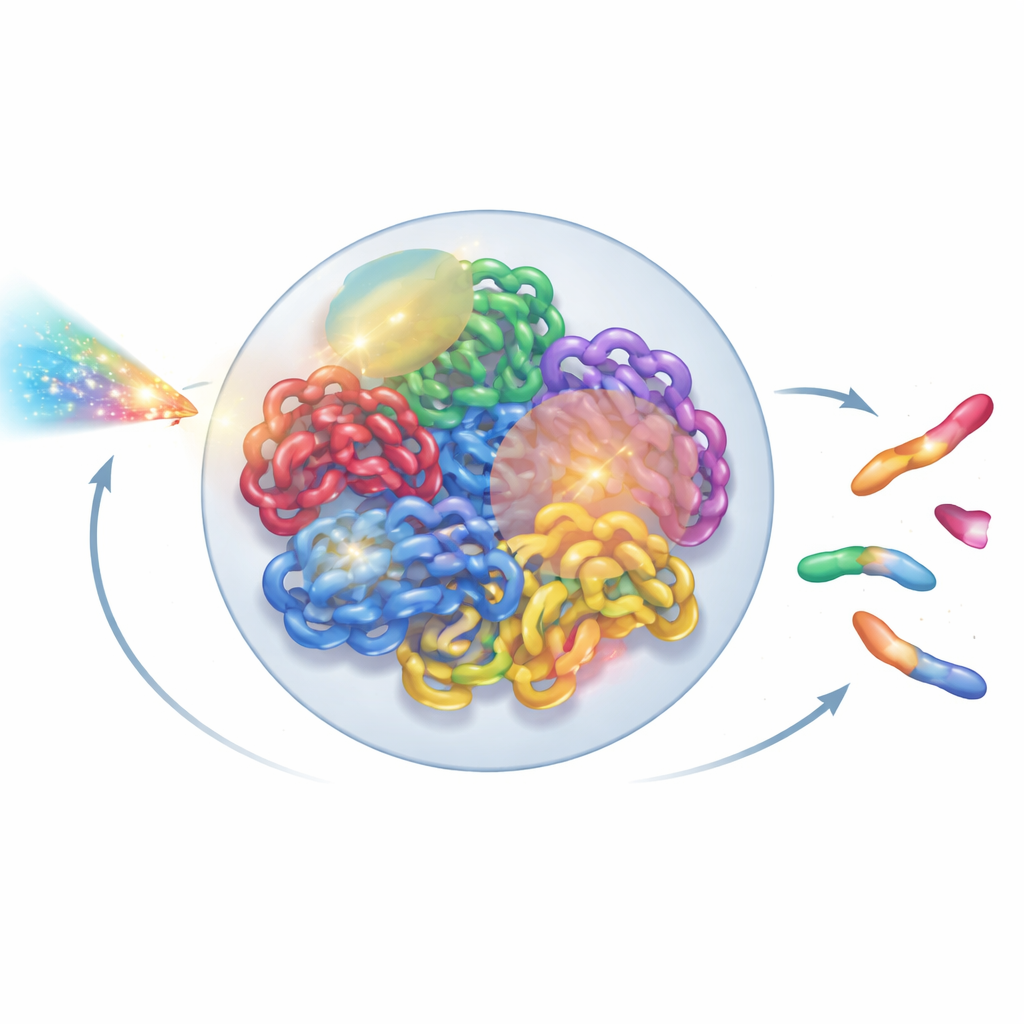
Ver el genoma como una estructura viva
Dentro de cada célula humana, dos metros de ADN se pliegan en un núcleo diminuto de solo unos pocos micrómetros. Este plegamiento no es aleatorio: cada cromosoma tiende a ocupar su propio territorio, a su vez dividido en vecindarios y dominios en bucle. Nuevas herramientas experimentales, como la microscopía de superresolución y los mapas de contactos Hi-C, han revelado este intrincado diseño 3D con un detalle notable. Sin embargo, la mayoría de los modelos de radiación siguen tratando el ADN como un enredo simplificado de líneas o bucles idealizados, pasando por alto esta organización de orden superior. Los autores se propusieron construir un modelo de núcleo completo que respete lo que los biólogos han aprendido sobre la arquitectura real de la cromatina, y que al mismo tiempo sea lo suficientemente rápido para ejecutarse en ordenadores de laboratorio convencionales.
Construir un núcleo virtual con física de polímeros
El equipo modeló los cromosomas como cadenas flexibles, tomando ideas de la física de polímeros, el mismo campo usado para entender plásticos y materiales blandos. Dividieron el problema en tres etapas de relajación para dominar el enorme coste computacional. Primero, colocaron grandes bloques constructores llamados dominios de cromatina a lo largo del núcleo, permitiéndoles repelerse entre sí, estirarse a lo largo de sus longitudes y agruparse en subcompartimentos más amplios. Segundo, hicieron zoom dentro de cada dominio para desplegar las fibras de cromatina más finas, incluidas las regiones en bucle mantenidas por proteínas de unión. Tercero, dejaron que todas las fibras interactuasen libremente de nuevo dentro del límite nuclear hasta aproximarse a una configuración final realista. Al dividir el proceso de este modo y añadir búsquedas jerárquicas y trucos de computación paralela, redujeron el tiempo de ejecución de unos imprácticos cuatro meses a aproximadamente tres horas por núcleo virtual en una estación de trabajo de 64 núcleos.
De las trayectorias de radiación a roturas y reparaciones del ADN
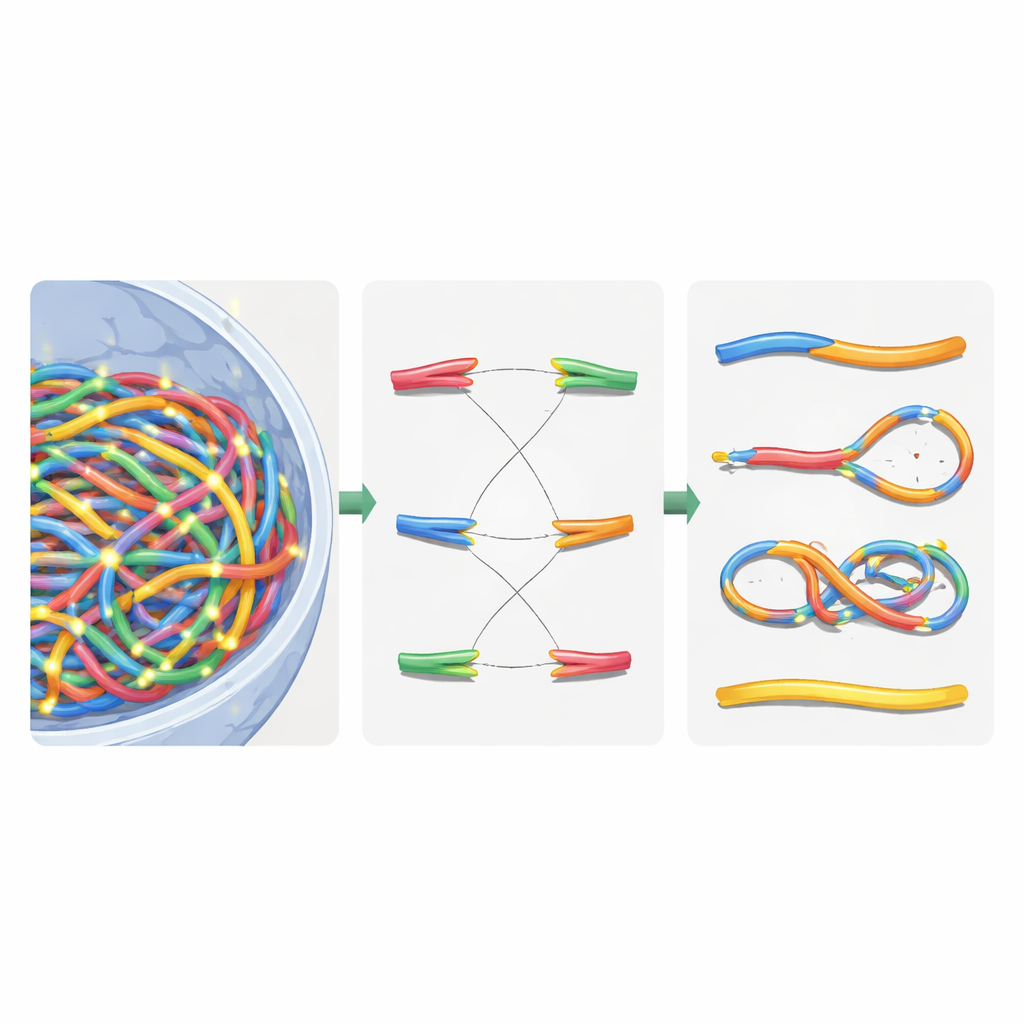
Una vez construido el núcleo virtual, los autores superpusieron trayectorias de radiación detalladas generadas por simulaciones Geant4-DNA. Usaron una búsqueda jerárquica para encontrar, para cada evento de ionización, qué dominio de cromatina, segmento de fibra y finalmente qué nucleótido estaba más cercano, sin nunca almacenar los diez mil millones de posiciones de nucleótidos en memoria. En su lugar, mantuvieron una plantilla de cromatina reutilizable y aplicaron transformaciones de coordenadas ingeniosas en tiempo real. Las ionizaciones en la columna vertebral del ADN se trataron como roturas de hebra, y roturas cercanas en hebras opuestas se convirtieron en roturas de doble hebra. Para imitar la maquinaria de reparación celular, los autores introdujeron una regla de reagrupe basada en la distancia: los extremos libres del ADN que yacen cerca tienen más probabilidad de reunirse. Las decisiones de reagrupamiento se tomaron paso a paso hasta que todos los extremos quedaron emparejados o sin reparar, recreando tanto reparaciones correctas como fragmentos mal unidos.
Clasificar cromosomas rotos con lógica de redes
Tras esta reparación virtual, el núcleo contenía una mezcla de cromosomas reensamblados y fragmentos sobrantes. Para clasificar lo ocurrido, los autores tradujeron el genoma reparado en un grafo no dirigido: los segmentos cromosómicos se convirtieron en aristas, y sus extremos y puntos de rotura en nodos. Usando un algoritmo estándar de componentes conectados, pudieron recuperar automáticamente cada nuevo objeto semejante a un cromosoma y contar características clave como el número de centrómeros (puntos de anclaje para la división celular) y telómeros (extremos naturales). A partir de esto, identificaron dicéntricos (cromosomas con dos centrómeros), anillos y deleciones. Luego compararon sus simulaciones con experimentos clásicos en células de piel humana expuestas a rayos gamma y a partículas alfa, encontrando que las aberraciones cromosómicas totales se reproducían dentro de aproximadamente un 20% de los valores medidos, una mejora sustancial respecto a modelos anteriores.
Qué significa esto para pacientes y astronautas
En términos sencillos, este trabajo muestra que «dónde» se sitúa el ADN en el núcleo y «cómo» se pliega influyen de forma fuerte en cómo el daño por radiación se acumula hasta producir cambios cromosómicos peligrosos. Al combinar una arquitectura genómica 3D realista, simulación eficiente basada en física y una lectura de cromosomas rotos basada en grafos, los autores proporcionan un puente poderoso entre la biología estructural y la radiobiología. Sostienen que refinamientos futuros —como añadir tiempos detallados de reparación y usar datos de secuenciación del genoma completo— podrían hacer este enfoque aún más preciso para predecir el impacto biológico de partículas de alta energía usadas en terapias contra el cáncer o encontradas en el espacio profundo. En última instancia, mejores modelos del hogar del ADN dentro de nuestras células podrían ayudar a personalizar tratamientos con radiación más seguros y eficaces y a afinar nuestra comprensión de los riesgos radiológicos a largo plazo.
Cita: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Palabras clave: daño en el ADN inducido por radiación, arquitectura 3D de la cromatina, aberrações cromosómicas, modelado por física de polímeros, terapia con partículas