Clear Sky Science · es
Activación transcripcional de PPP1R14C por KLF7 libera la actividad de CDK1 para promover el carcinoma escamoso de pulmón
Por qué importa este descubrimiento sobre el cáncer de pulmón
El cáncer de pulmón sigue siendo la principal causa de muertes por cáncer en todo el mundo, y una forma importante—el carcinoma escamoso de pulmón—se ha quedado atrás en la era de los fármacos dirigidos. A diferencia de otros tumores pulmonares que pueden tratarse con medicamentos dirigidos a mutaciones específicas, este subtipo a menudo obliga a los médicos a recurrir a la quimioterapia y la inmunoterapia, que no funcionan en todos los casos. Este estudio desvela un circuito de control hasta ahora oculto dentro de las células del carcinoma escamoso de pulmón que actúa como si cortara los frenos de la división celular, y señala un punto débil concreto que fármacos futuros podrían explotar.
Un eslabón perdido en un cáncer difícil de tratar
Los investigadores empezaron buscando en grandes bases de datos públicas de cáncer para ver si algún gen destacaba en el carcinoma escamoso de pulmón. Uno, llamado PPP1R14C, apareció de manera consistente a niveles elevados en las muestras tumorales frente al tejido pulmonar normal. Su abundancia aumentaba a medida que los cánceres avanzaban a estadios posteriores, y los pacientes cuyos tumores producían más de esta molécula tendían a vivir menos tiempo. Estos patrones se observaron tanto a nivel de ARN—los mensajes que las células usan para fabricar proteínas—como a nivel proteico, lo que sugiere que PPP1R14C no solo estaba presente sino que participaba activamente en impulsar la enfermedad. 
Cómo los tumores pulmonares liberan los frenos
Para entender por qué PPP1R14C es tan abundante en estos tumores, el equipo investigó el interruptor de encendido/apagado del gen, su promotor. Combinando varias bases de datos que registran dónde se unen diferentes proteínas reguladoras al ADN, identificaron a un factor llamado KLF7 como sospechoso principal. En células de carcinoma escamoso de pulmón cultivadas en el laboratorio, aumentar los niveles de KLF7 provocó un alza de PPP1R14C, mientras que reducir KLF7 lo disminuyó drásticamente. Experimentos que unían el promotor de PPP1R14C a un reportero luminoso confirmaron que KLF7 puede activar directamente ese interruptor; cambiar una breve secuencia de ADN donde KLF7 se ancla anuló el efecto. Una técnica que captura el ADN unido a KLF7 en células intactas mostró que este factor se asienta físicamente en el promotor de PPP1R14C, cerrando el caso de que KLF7 activa directamente este gen.
Del interruptor genético al comportamiento agresivo
Una vez que supieron qué eleva PPP1R14C, los científicos preguntaron qué hace realmente la molécula. Usando líneas celulares de carcinoma escamoso de pulmón, redujeron PPP1R14C con herramientas genéticas y observaron el comportamiento celular. Las células sin PPP1R14C crecían más despacio, formaban menos colonias, invadían menos a través de una matriz gelatinosa y eran más propensas a sufrir muerte celular programada. La imagen inversa también fue cierta: células diseñadas para producir PPP1R14C en exceso se dividían más rápido, formaban más colonias e invadían con mayor agresividad. Cuando estas células modificadas se implantaron en ratones, los tumores con PPP1R14C reducido crecieron menos y pesaron menos. En conjunto, estos hallazgos muestran que PPP1R14C no es un mero espectador sino un impulsor activo de rasgos cancerosos.
Un vistazo paso a paso dentro del motor del ciclo celular
Ahondando más, el equipo examinó qué programas celulares dependen de PPP1R14C. Barridos amplios de la actividad génica revelaron que eliminar PPP1R14C afectaba especialmente a genes que controlan el punto de control G2/M—el momento en que una célula se compromete a dividirse en dos. En el centro de este punto de control se encuentra CDK1, un interruptor maestro para la entrada en mitosis. En células cancerosas con PPP1R14C elevado, CDK1 presentaba una etiqueta fosfato activadora y sus dianas aguas abajo se activaban, señalando luz verde para la división. Cuando se redujo PPP1R14C, esta activación desapareció. Experimentos bioquímicos explicaron por qué: PPP1R14C se une a una enzima “borradora” celular llamada PP1, que normalmente elimina la etiqueta activadora de CDK1. Al aferrarse a PP1, PPP1R14C impide que ésta llegue a CDK1, de modo que la señal de activación persiste y las células continúan el ciclo. 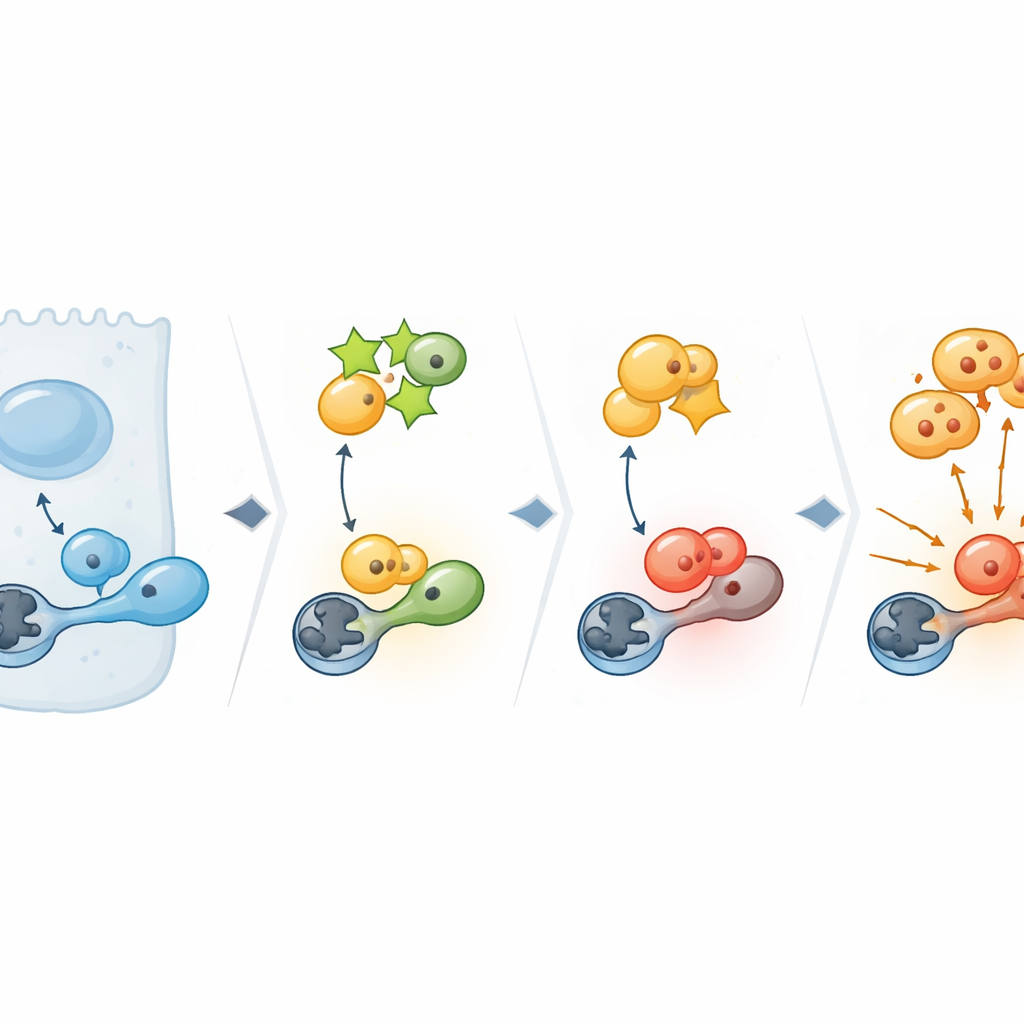
Convertir una visión molecular en una idea terapéutica
La parte más alentadora del trabajo llegó cuando los investigadores probaron un fármaco que bloquea directamente CDK1. En células sobrecargadas de PPP1R14C, este inhibidor de CDK1 eliminó la ventaja de crecimiento, redujo la formación de colonias y recortó la invasión, reaplicando eficazmente los frenos que PPP1R14C había liberado. Uniéndolo todo, el estudio describe una cadena clara de eventos: KLF7 activa PPP1R14C; PPP1R14C neutraliza a PP1; CDK1 permanece hiperactivo; y las células del carcinoma escamoso de pulmón se dividen sin control. Para los no especialistas, esto significa que los científicos han identificado tanto una señal de alerta—niveles altos de PPP1R14C que marcan tumores más peligrosos—como una palanca terapéutica prometedora: fármacos que inhiben CDK1, especialmente en pacientes cuyos tumores dependen de este circuito desbocado.
Cita: Xing, L., Yuan, C., Shen, X. et al. Transcriptional activation of PPP1R14C by KLF7 unleashes CDK1 activity to promote lung squamous cell carcinoma. Sci Rep 16, 9244 (2026). https://doi.org/10.1038/s41598-026-39174-3
Palabras clave: carcinoma escamoso de pulmón, ciclo celular, CDK1, PPP1R14C, terapia dirigida