Clear Sky Science · es
Aislamiento y caracterización de bacteriófagos líticos con potencial terapéutico frente a Klebsiella pneumoniae multirresistente procedentes de Etiopía
Por qué nos importan los virus diminutos en aguas sucias
Los hospitales de todo el mundo lidian con infecciones que ya no responden a los antibióticos. Uno de los culpables principales es Klebsiella pneumoniae, una bacteria que puede provocar neumonía grave, infecciones sanguíneas e infecciones del tracto urinario. En este estudio procedente de Etiopía, los investigadores buscaron enemigos naturales de este germen: virus llamados bacteriófagos, o fagos, que podrían convertirse en medicamentos vivos cuando los antibióticos fallan. Al muestrear las aguas residuales hospitalarias y ríos contaminados en Addis Abeba, descubrieron una rica colección de fagos capaces de matar Klebsiella multirresistente y comenzaron a evaluar cuán eficaces podrían ser estos depredadores microscópicos como terapias futuras.
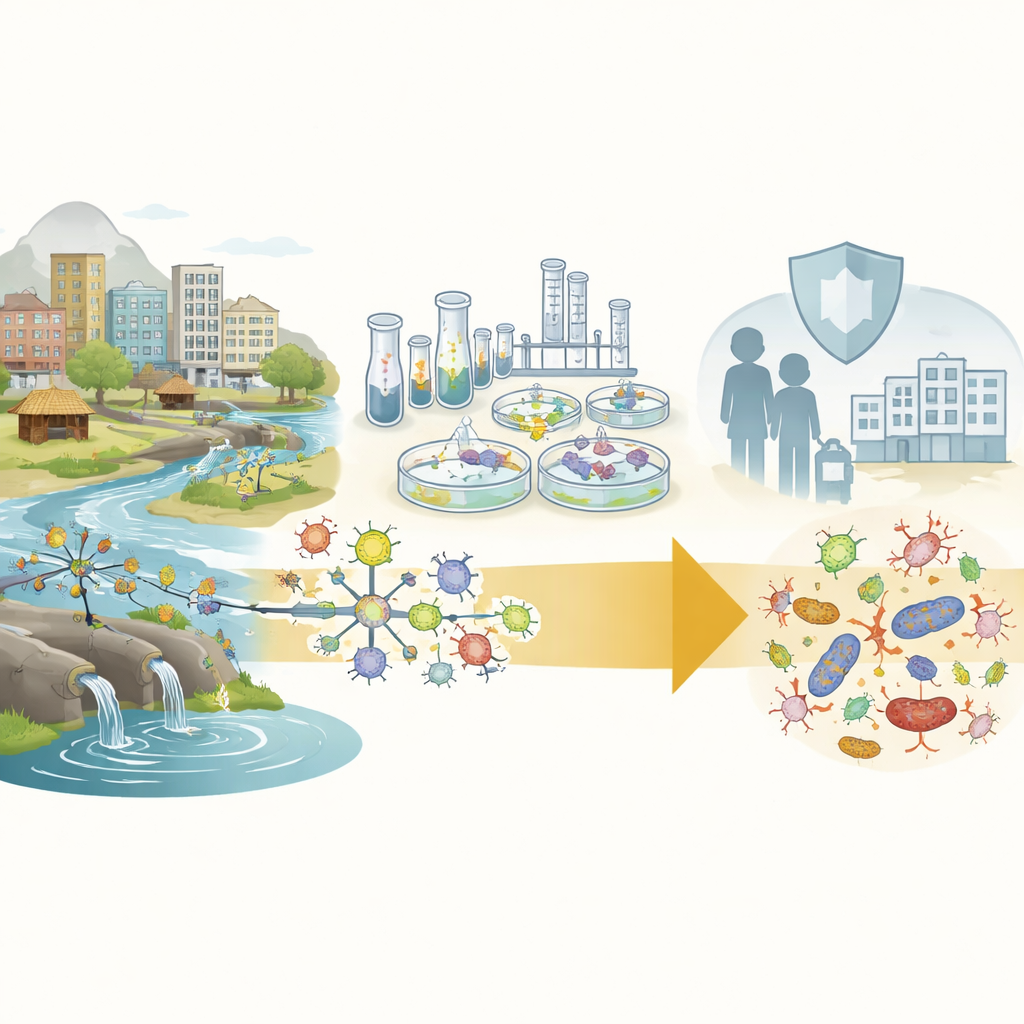
Buscando virus útiles en la ciudad
El equipo se centró en Addis Abeba, una ciudad de rápido crecimiento donde los hospitales abarrotados y el elevado uso de antibióticos crean condiciones ideales para las bacterias resistentes. En lugar de buscar nuevos fármacos en fábricas, los científicos recogieron 66 muestras de aguas residuales, desagües hospitalarios y suelos de cuatro hospitales principales y de ríos contaminados cercanos. Estos lugares están llenos de bacterias y de los fagos que las infectan. En el laboratorio, mezclaron cada muestra con diez cepas de Klebsiella particularmente difíciles de tratar, aisladas de pacientes. Las zonas claras que aparecían en las placas bacterianas señalaban que un fago presente en la muestra de agua había atacado y destruido con éxito a su hospedador.
Construyendo una biblioteca de “asesinos” bacterianos
A partir de 660 pruebas de este tipo, los investigadores aislaron 102 fagos distintos e impresionantes que podían matar Klebsiella multirresistente. La mayoría procedía de aguas residuales y desagües, lo que confirma que estos entornos son terrenos fértiles para la búsqueda. Cada fago se evaluó para determinar cuántos aislamientos clínicos distintos podía eliminar. Algunos eran selectivos, atacando a menos del 10% de las 46 cepas bacterianas probadas, mientras que otros eliminaron más del 60%. Un puñado incluso mostró capacidad para infectar especies estrechamente relacionadas, como otros tipos de Klebsiella, lo que sugiere que podrían ser útiles contra un conjunto más amplio de gérmenes hospitalarios. El equipo también midió la rapidez y eficiencia con que cada fago se multiplicaba, cuántas nuevas partículas fagales liberaba una célula infectada y cuán estables se mantenían a distintas temperaturas y niveles de acidez —condiciones a las que se enfrentarían en tratamientos reales—.
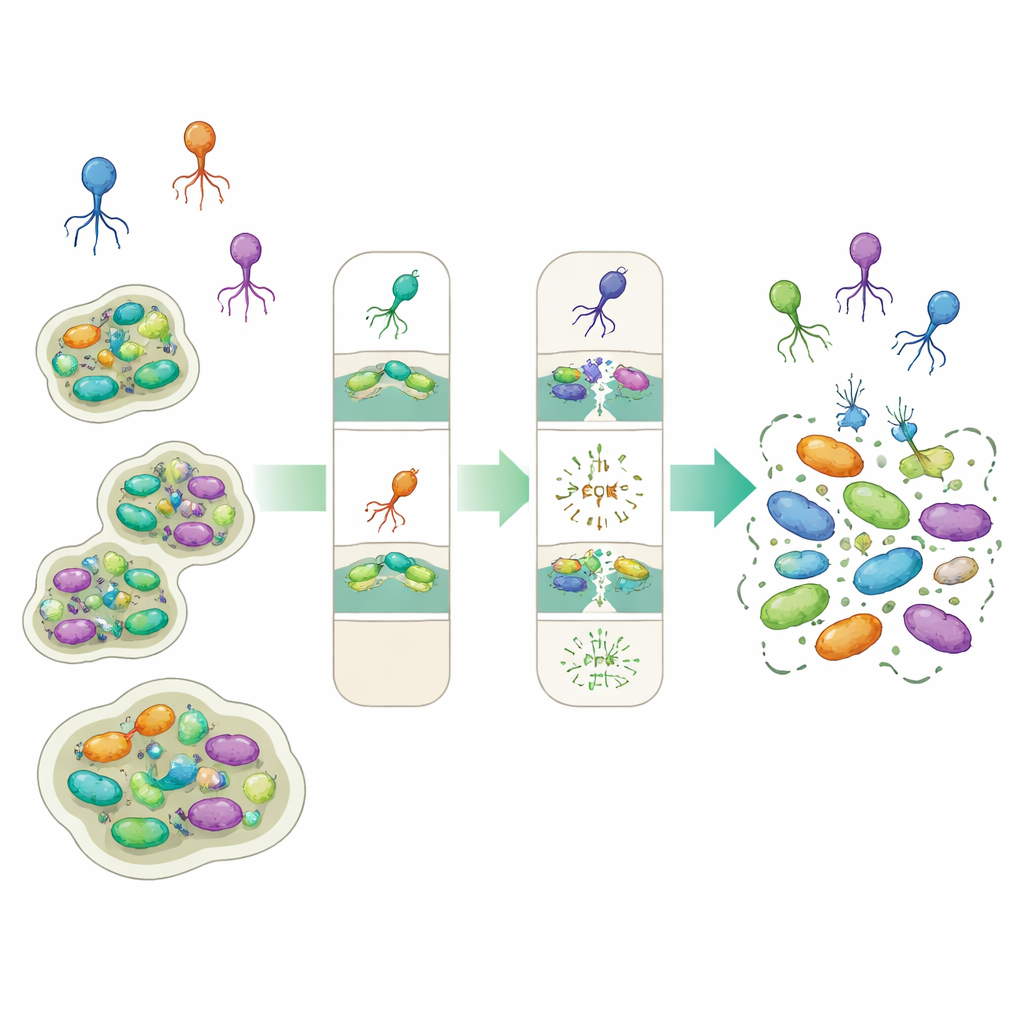
Diseñando un “cóctel” viral inteligente
Ningún fago individual pudo eliminar todas las cepas clínicas, por lo que los investigadores recurrieron a una estrategia de cóctel: combinar varios fagos para que al menos uno de ellos pueda atacar a cada bacteria concreta. Usando herramientas informáticas y sus datos de laboratorio, trataron el problema como un rompecabezas: encontrar el número mínimo de fagos que, en conjunto, cubrieran los 42 aislamientos de Klebsiella susceptibles en las pruebas. La solución fue sorprendentemente compacta: solo cuatro fagos cuidadosamente seleccionados formaron un cóctel mínimo que mató a todas las cepas objetivo. En experimentos de laboratorio, dosis más altas de estos fagos redujeron drásticamente el crecimiento bacteriano, mostrando un fuerte poder lítico incluso frente a aislamientos altamente resistentes.
Mirando dentro del árbol genealógico de los fagos
Para entender qué tipos de fagos habían encontrado, los científicos analizaron su material genético mediante pruebas de ADN dirigidas. La mayoría de los 60 fagos de mejor desempeño se agruparon en seis géneros conocidos de fagos virulentos que infectan Klebsiella. Un grupo llamado Taipeivirus fue el más común, mientras que otros eran más raros pero igualmente prometedores. En general, los fagos se mantuvieron activos en condiciones ligeramente ácidas a ligeramente alcalinas y a temperaturas similares a las del cuerpo humano hasta aproximadamente 50 °C, aunque el calor extremo o una acidez muy elevada redujeron su supervivencia. Estas características sugieren que muchos de los fagos podrían permanecer efectivos dentro del cuerpo humano y durante el almacenamiento si se manejan adecuadamente.
Del banco de laboratorio al paciente
En conjunto, el estudio ofrece un panorama alentador: las aguas sucias alrededor de Addis Abeba albergan un conjunto diverso y potente de fagos capaces de atacar Klebsiella multirresistente, y un cóctel cuidadosamente seleccionado de cuatro fagos puede cubrir una amplia gama de aislamientos clínicos en el laboratorio. Para el público general, el mensaje clave es que la naturaleza ya nos proporciona virus diminutos y muy específicos que podrían ayudarnos a contraatacar cuando los antibióticos dejan de funcionar. Antes de que estos fagos puedan usarse de forma rutinaria en hospitales, los científicos aún deben secuenciar completamente sus genomas, probarlos en animales y realizar ensayos clínicos para demostrar su seguridad y eficacia. Pero este trabajo sienta las bases cruciales para transformar fagos ambientales en tratamientos precisos y ecológicos contra infecciones bacterianas resistentes.
Cita: Abebe, A.A., Birhanu, A.G. & Tessema, T.S. Isolation and characterization of lytic bacteriophages with therapeutic potential against multidrug resistant Klebsiella pneumoniae from Ethiopia. Sci Rep 16, 8000 (2026). https://doi.org/10.1038/s41598-026-39153-8
Palabras clave: terapia con fagos, resistencia a los antibióticos, Klebsiella pneumoniae, cóctel de bacteriófagos, virología de aguas residuales