Clear Sky Science · es
La deficiencia de Dlgap2 interrumpe la homeostasis sináptica al promover la degradación de Itsn1 mediada por ubiquitina en un modelo con características autistas inducido por ácido valproico
Por qué importa un medicamento común y la conexión neuronal
El ácido valproico es un fármaco empleado desde hace tiempo para la epilepsia y los trastornos del ánimo, pero cuando se toma durante el embarazo se ha asociado a un mayor riesgo de autismo en los niños. Este estudio aborda una pregunta urgente para familias y médicos: ¿qué hace exactamente este medicamento al cableado en desarrollo del cerebro? Al rastrear cambios hasta moléculas concretas en las sinapsis —los puntos de comunicación entre neuronas— los investigadores descubren una nueva cadena de acontecimientos que puede ayudar a explicar conductas similares al autismo y orientar estrategias terapéuticas futuras. 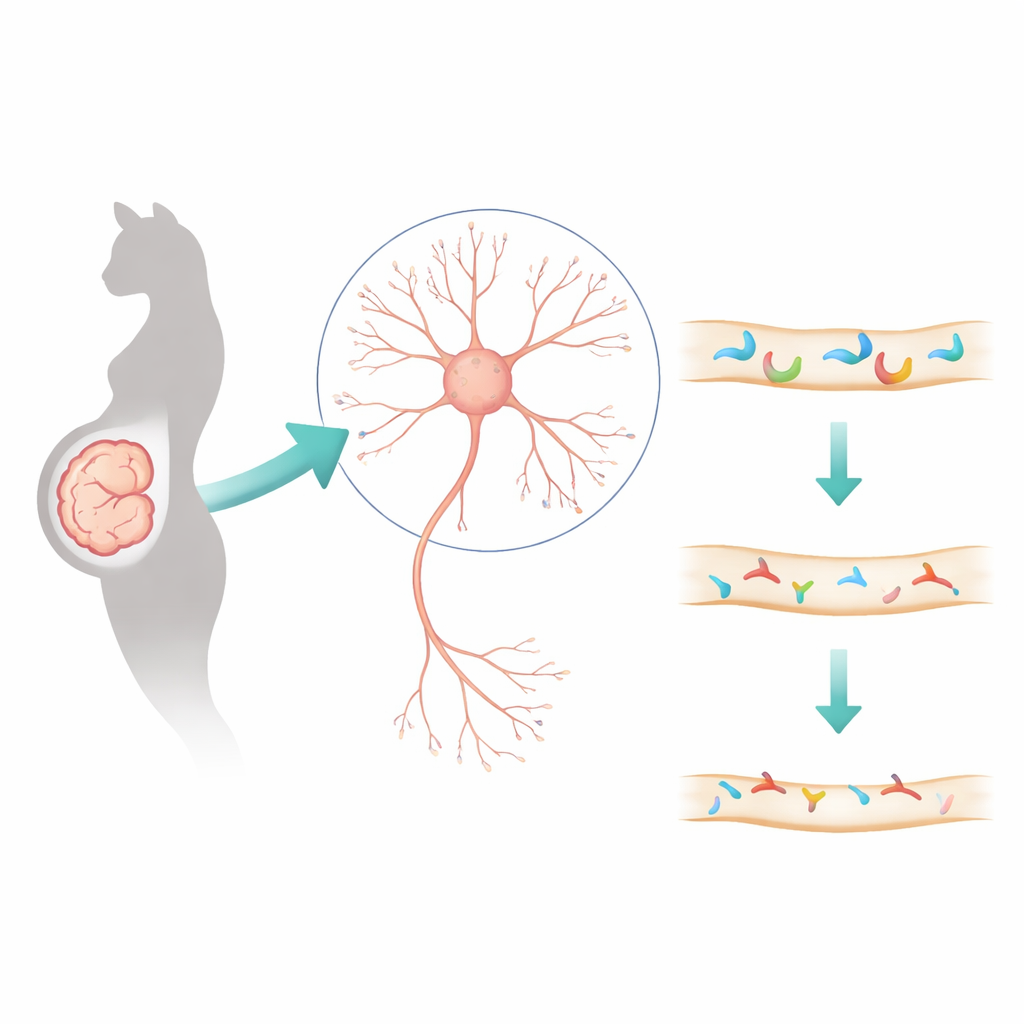
Buscando puntos vulnerables comunes entre especies
Para hallar pistas fiables, el equipo no se limitó a un solo modelo animal. Compararon cerebros o tejidos corticales derivados de organoides humanos, monos, ratas y ratones expuestos al ácido valproico antes del nacimiento. Mediante grandes sondeos de genes y proteínas, identificaron un pequeño conjunto de genes que cambiaron en todos estos sistemas y que estaban relacionados con las sinapsis y el aislamiento de fibras nerviosas. Entre ellos destacó uno: Dlgap2, una proteína andamio que ayuda a organizar el lado postsináptico de las sinapsis excitadoras. En ratones expuestos prenatalmente al ácido valproico, los niveles de Dlgap2 disminuyeron en la corteza y, más específicamente, dentro de pequeños compartimentos sinápticos, lo que sugiere que esta molécula estructural es una víctima clave de la exposición al fármaco.
De los cambios moleculares a las alteraciones del comportamiento
Los autores se preguntaron entonces si la pérdida de Dlgap2 por sí sola basta para perturbar la función cerebral. Emplearon virus que llevaban ARN de horquilla corta para reducir Dlgap2 en neuronas de ratón en cultivo y en ratones recién nacidos. En el cultivo, las neuronas con menos Dlgap2 desarrollaron ramas más cortas y presentaron menos puntos postsinápticos, señales de conexiones debilitadas. En animales vivos, la reducción dirigida de Dlgap2 en el cerebro produjo conductas similares al autismo: ratones jóvenes machos tuvieron dificultades para aprender la ubicación de una plataforma oculta en un laberinto acuático y mostraron menos interés por parejas sociales y por la novedad social en una prueba de tres cámaras. Estos cambios imitan los déficits de aprendizaje y sociales observados en animales expuestos al ácido valproico, lo que refuerza la idea de que la pérdida de Dlgap2 no es solo un efecto secundario sino un impulsor de las alteraciones conductuales.
Encontrando un socio vulnerable en la sinapsis
Para entender cómo la pérdida de Dlgap2 se propaga por la sinapsis, los investigadores examinaron más de cerca las proteínas ancladas en la densidad postsináptica, la densa almohadilla molecular que recibe señales químicas. Mediante proteómica, hallaron que reducir Dlgap2 alteraba la abundancia de cientos de proteínas sinápticas, en particular las implicadas en la organización de sinapsis y en el reciclado de vesículas por endocitosis. Una proteína, Intersectin‑1 (Itsn1), descendió de forma especialmente marcada. Trabajos bioquímicos posteriores mostraron que Dlgap2 e Itsn1 residen físicamente en los mismos complejos proteicos en fracciones enriquecidas en sinapsis y que ambos figuran entre genes vinculados al autismo. Esto apunta a una asociación reguladora focalizada entre las dos moléculas dentro del concurrido paisaje sináptico. 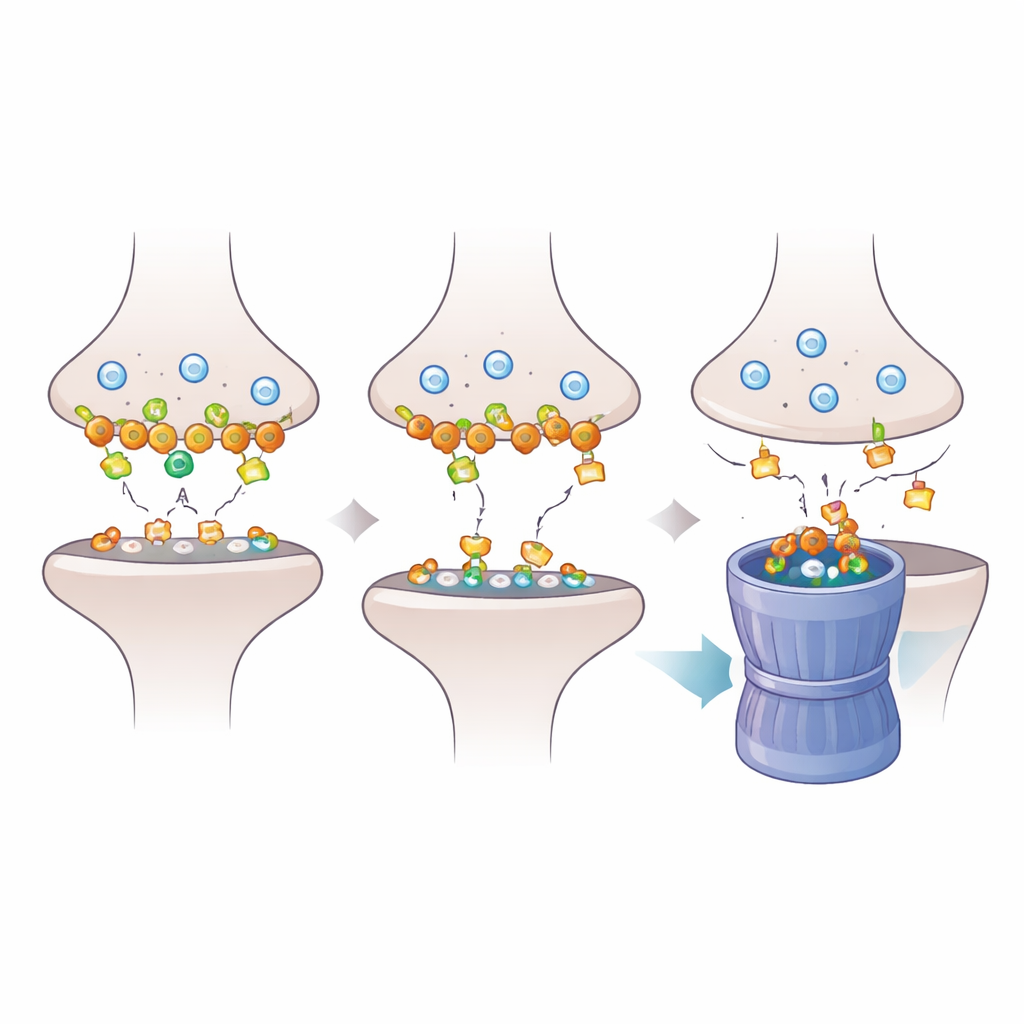
Sale a la luz una vía oculta de eliminación
El equipo preguntó a continuación por qué los niveles de Itsn1 caen cuando falta Dlgap2. Observaron que en los compartimentos sinápticos, la reducción de Dlgap2 desencadenó una forma de etiquetado proteico conocida como ubiquitinación ligada a K48, que marca proteínas para su degradación por el proteasoma, el “triturador” celular. Bloquear este sistema de eliminación con el fármaco MG132 evitó la pérdida de Itsn1, lo que indica que Dlgap2 protege normalmente a Itsn1 de ser etiquetada y destruida. Sin Dlgap2, Itsn1 es cada vez más etiquetada, dirigida al proteasoma y agotada en las sinapsis, socavando el reciclado endocítico y el equilibrio de la actividad sináptica. El trabajo sugiere que cambios sutiles en la velocidad de recambio de proteínas clave pueden desestabilizar las sinapsis durante el desarrollo cerebral.
Qué significa esto para el autismo y futuras terapias
En conjunto, el estudio propone una idea sencilla pero potente para el público general: la exposición prenatal al ácido valproico puede debilitar una proteína estructural “armazón” (Dlgap2) en las sinapsis. Cuando se pierde ese armazón, su proteína asociada (Itsn1) queda sobreexpuesta al sistema de eliminación celular, lo que conduce a un reciclado defectuoso de componentes sinápticos y, en última instancia, a circuitos mal conectados y conductas de tipo autista en ratones. Aunque muchos genes y factores ambientales contribuyen al autismo, este eje Dlgap2–Itsn1 ofrece una cadena molecular concreta desde la exposición prenatal al fármaco hasta la alteración de la función cerebral. A largo plazo, las estrategias que preserven esta asociación o que ajusten finamente la maquinaria de eliminación de proteínas en las sinapsis podrían ayudar a proteger los cerebros en desarrollo frente a formas similares de perturbación.
Cita: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Palabras clave: ácido valproico y embarazo, proteínas andamio sinápticas, mecanismos del espectro autista, vía del proteasoma y ubiquitina, modelos murinos de autismo