Clear Sky Science · es
El casr en pez cebra modula la estructura y función cardíaca
Por qué importan los corazones de los peces para la salud humana
Nuestros corazones dependen del calcio, un mineral sencillo, para latir correctamente. Cuando las señales de calcio fallan, el resultado puede ser insuficiencia cardiaca u otras enfermedades graves. Este estudio utiliza diminutos peces cebra—peces de agua dulce transparentes usados con frecuencia en laboratorio—para explorar cómo un interruptor que detecta calcio en las células moldea la fuerza y la supervivencia cardíaca. Al desactivar un único gen que ayuda a las células a detectar el calcio, los investigadores descubrieron una cadena de problemas en el bombeo del corazón, la forma del cuerpo e incluso en la vejiga natatoria llena de aire del pez. Su trabajo también muestra que el trasfondo genético más amplio de un animal puede suavizar o empeorar dramáticamente el impacto de una mutación dañina, una lección con claras resonancias en la medicina humana.
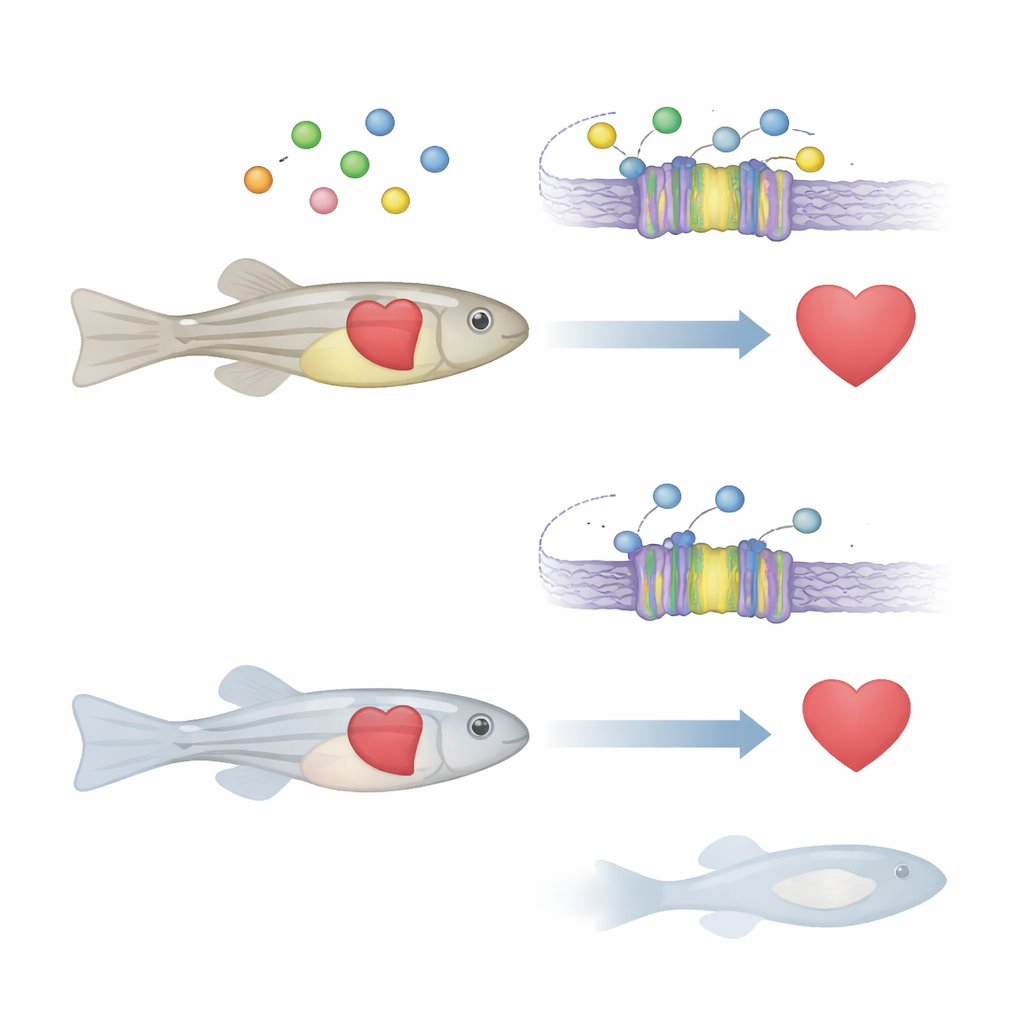
Un “termostato” celular para el calcio
El calcio dentro y fuera de las células actúa como una señal universal que controla el movimiento muscular, la liberación de hormonas e incluso qué genes se activan. Muchos órganos dependen de una proteína llamada receptor sensor de calcio, que funciona como un termostato para los niveles de calcio. Cuando el calcio extracelular cambia, este receptor ajusta la liberación hormonal y otros procesos para restaurar el equilibrio. En las personas, los defectos en este receptor ya se asocian a trastornos óseos y minerales, y se sospecha que participan en enfermedades cardíacas y algunos cánceres. Sin embargo, cómo exactamente este sensor de calcio influye en el desarrollo y la función cardíaca en un animal entero había permanecido poco claro.
Qué sucede cuando el sensor de calcio se apaga
El equipo se centró en la versión del gen en pez cebra, llamada casr, que está fuertemente conservada con su homólogo humano. Usando herramientas modernas de edición genética, crearon peces cebra en los que ambas copias de casr fueron desactivadas. Al principio, los peces jóvenes parecían casi normales. Pero a los cinco días después de la fertilización, muchos mutantes no lograron inflar su vejiga natatoria, un pequeño órgano lleno de gas que controla la flotabilidad. Estos peces se hundían en el fondo, nadaban mal, pronto desarrollaron curvatura espinal y todos murieron a las dos semanas de edad. Estos signos externos apuntaban a problemas internos graves que afectaban a más de un sistema de órganos.
Un corazón más débil, más pequeño y más lento
El video a alta velocidad y el análisis de imágenes del latido cardíaco revelaron cuán profundamente afectaba la ausencia del sensor de calcio al rendimiento cardíaco. En larvas de pez cebra normales, el ventrículo cardíaco se llena y se vacía con un patrón rítmico y vigoroso. En los mutantes, el ventrículo era notablemente más pequeño durante el llenado, el corazón latía más despacio y cada latido expulsaba menos sangre. Las medidas de cuánto se acorta el músculo cardíaco y de cuánto cambia el área de la cámara de bombeo en cada latido se redujeron, mostrando una contracción debilitada. El gasto cardíaco global—el volumen de sangre movido por minuto—cayó drásticamente. A nivel de genes, cientos de transcripciones cambiaron, y las redes clave que controlan el manejo del calcio y la maquinaria de la contracción muscular se redujeron, vinculando la edición genética tanto con el fallo molecular como con el mecánico del corazón.
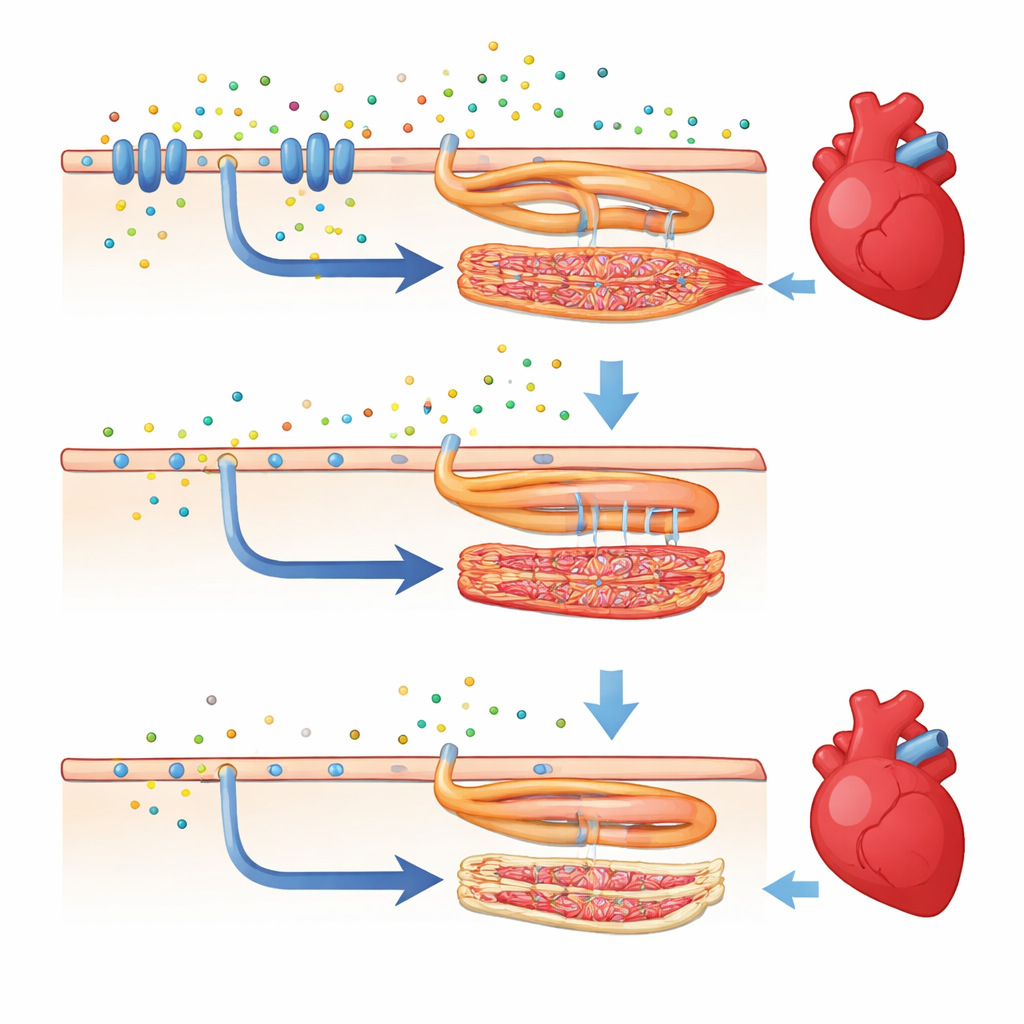
Cómo los genes de fondo pueden rescatar un corazón enfermo
Sorprendentemente, la misma mutación en casr se comportó de forma muy diferente en otra cepa común de pez cebra, conocida como TL (Tupfel long-fin). Cuando la eliminación del gen se introdujo en este nuevo trasfondo genético, los peces pudieron inflar sus vejigas natatorias, sobrevivir hasta la adultez y mostraron un bombeo cardíaco mucho mejor. Sus corazones seguían algo comprometidos—la frecuencia cardíaca permanecía por debajo de lo normal—pero las medidas de la fuerza de contracción ventricular y de la cantidad de sangre bombeada por minuto casi igualaron a las de los peces sanos. En estos animales rescatados, muchos de los genes vinculados a la señalización del calcio y a la contracción del músculo cardíaco regresaron a niveles intermedios, más altos que en la línea enferma original. Esto revela que otros genes repartidos por el genoma pueden amortiguar o intensificar el impacto de un cambio dañino.
Señales que moldean corazones y la flotabilidad
Más allá del corazón, la pérdida del sensor de calcio también perturbó sistemas de control del crecimiento importantes en el embrión. Los genes de las vías de señalización Wnt y Hedgehog—arquitectos bien conocidos de la formación de órganos—estaban reprimidos en los mutantes. Estos cambios probablemente contribuyen al fracaso en la inflación de la vejiga natatoria, lo que a su vez puede empeorar la supervivencia al dificultar que el pez se alimente y se mueva eficientemente. Los marcadores de diferenciación de las células del músculo cardíaco también se redujeron, y los ventrículos eran más pequeños, lo que sugiere que el sensor de calcio ayuda a guiar cómo crecen y maduran las células del músculo cardíaco.
Qué significa esto para entender el riesgo de enfermedad
En conjunto, este trabajo muestra que el receptor sensor de calcio es un guardián crucial tanto de la función cardíaca como del desarrollo adecuado de órganos en el pez cebra. Cuando se pierde este sensor, las señales de calcio flaquean, el músculo cardíaco se contrae débilmente, la vejiga natatoria falla y los animales mueren jóvenes. Sin embargo, el rescate dramático en una cepa genética diferente subraya un mensaje clave: el resto del genoma puede modificar fuertemente cuán peligrosa es realmente una mutación dada. Para la salud humana, esto enfatiza por qué personas que portan variantes génicas riesgosas similares pueden experimentar resultados de enfermedad muy distintos, y por qué entender tanto los genes centrales de la enfermedad como su trasfondo genético es esencial para predecir y tratar las afecciones cardíacas.
Cita: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Palabras clave: señalización del calcio, desarrollo cardíaco, modelo de pez cebra, trasfondo genético, función cardíaca