Clear Sky Science · es
La transmisión de fuerzas de tracción a través de un hidrogel de matriz bioactiva promueve la migración colectiva epitelial mediada por integrinas
Cómo las células tiran juntas para sanar
Cuando te cortas la piel o dañas un órgano, láminas de células deben moverse de forma coordinada para cerrar la herida. Este estudio plantea una pregunta aparentemente simple: cuando las células se desplazan en grupo, ¿solo se tiran unas a otras o también "se comunican" a través del material blando que hay debajo? Al recrear en el laboratorio un entorno gelatinoso realista, los autores muestran que las células pueden transmitir fuerzas mecánicas a través de esa matriz blanda para guiar el movimiento colectivo, revelando una capa oculta de comunicación que puede ser crucial para la cicatrización, la reparación tisular e incluso la diseminación del cáncer.
Un suelo blando que transmite fuerza
En nuestros cuerpos, muchas células se asientan sobre un andamiaje blando y rico en proteínas en lugar de sobre algo rígido como vidrio o plástico. Para imitar esto, los investigadores cultivaron células epiteliales renales como una capa continua sobre un hidrogel bioactivo formado por Matrigel y colágeno, dos componentes comunes del tejido natural. Después crearon una pequeña zona vacía en el centro del gel, como una diminuta herida, y observaron cómo la lámina celular marchaba hacia el interior para llenar el vacío. Para rastrear la actividad de una vía de señalización clave dentro de las células, usaron un biosensor fluorescente que informa sobre la actividad de ERK, una proteína que a menudo responde a señales mecánicas. Esta disposición les permitió ver, en tiempo real, cómo las fuerzas mecánicas en el gel blando se relacionaban tanto con el movimiento celular como con la señalización interna. 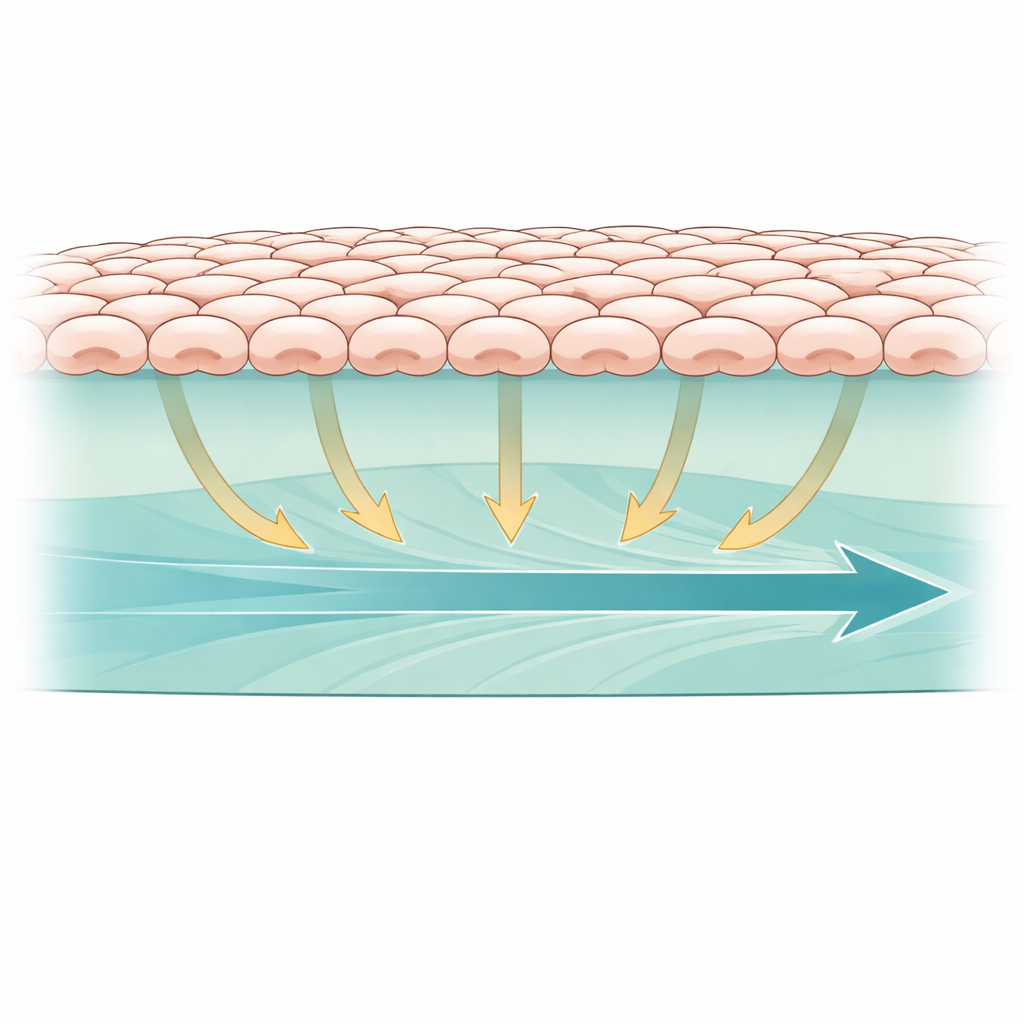
Viendo moverse el suelo bajo las células
Para comprobar si el gel realmente soportaba y transmitía fuerza, el equipo mezcló pequeñas cuentas magnéticas en el material y siguió su movimiento durante la migración celular. En el gel normal que contenía tanto Matrigel como colágeno, las cuentas se desplazaron lentamente hacia adelante en la misma dirección que la lámina celular que avanzaba, lo que indica que las células se agarraban y arrastraban la matriz bajo ellas. En geles compuestos solo por Matrigel, las cuentas se movían más despacio, lo que sugiere una transmisión de fuerza más débil. Cuando el gel se entrecruzó químicamente con glutaraldehído para endurecer y "bloquear" la red, las cuentas apenas se desplazaron. Bajo estas condiciones bloqueadas, las células seguían adhiriéndose pero su avance colectivo se ralentizó drásticamente, y la señal de ERK se volvió más débil y menos concentrada en el borde líder, lo que vincula una mayor tracción sobre la matriz con un movimiento grupal más rápido y dirigido.
Motores internos y compuertas iónicas impulsan el movimiento
Los autores investigaron a continuación qué dentro de las células genera estas fuerzas de tracción y cómo se detecta esa actividad. Usaron fármacos para bloquear la contracción mediada por miosina, el mismo tipo de maquinaria molecular que impulsa el músculo. Cuando se inhibió la contracción, la actividad de ERK disminuyó y la lámina celular avanzó más despacio, coherente con la idea de que el tirón interno es necesario para transmitir tensión a la matriz. También interfirieron con varios tipos de canales de calcio en la membrana celular y con el depósito interno de calcio. Bloquear estas vías iónicas atenuó la actividad de ERK y ralentizó la migración colectiva, apuntando a una cadena de eventos en la que el tirón mecánico sobre la matriz se convierte en señales de calcio y ERK que ayudan a mantener al grupo moviéndose unido.
Guiar la dirección mediante agarres superficiales
Un hallazgo especialmente llamativo provino de apuntar a las integrinas, las moléculas de superficie que actúan como pequeños anclajes que conectan las células con su entorno. Cuando los investigadores bloquearon un subtipo mayoritario de integrina, la lámina dejó de avanzar como un frente coherente, aunque las células individuales aún podían moverse localmente a una velocidad casi normal. Al mismo tiempo, el movimiento de las cuentas en el gel casi se detuvo, demostrando que las integrinas son esenciales para transmitir la fuerza desde las células en contracción hacia la matriz. En contraste, bloquear canales mecanosensibles relacionados con Piezo1, que ayudan a las células a detectar presión física, redujo tanto el ritmo de migración como la tracción observada en el gel. En conjunto, estos resultados trazan un panorama en el que la contracción genera fuerza, las integrinas la transmiten a la matriz, y los canales mecanosensibles y la señalización ERK interpretan esa fuerza para coordinar la dirección y eficiencia del movimiento colectivo. 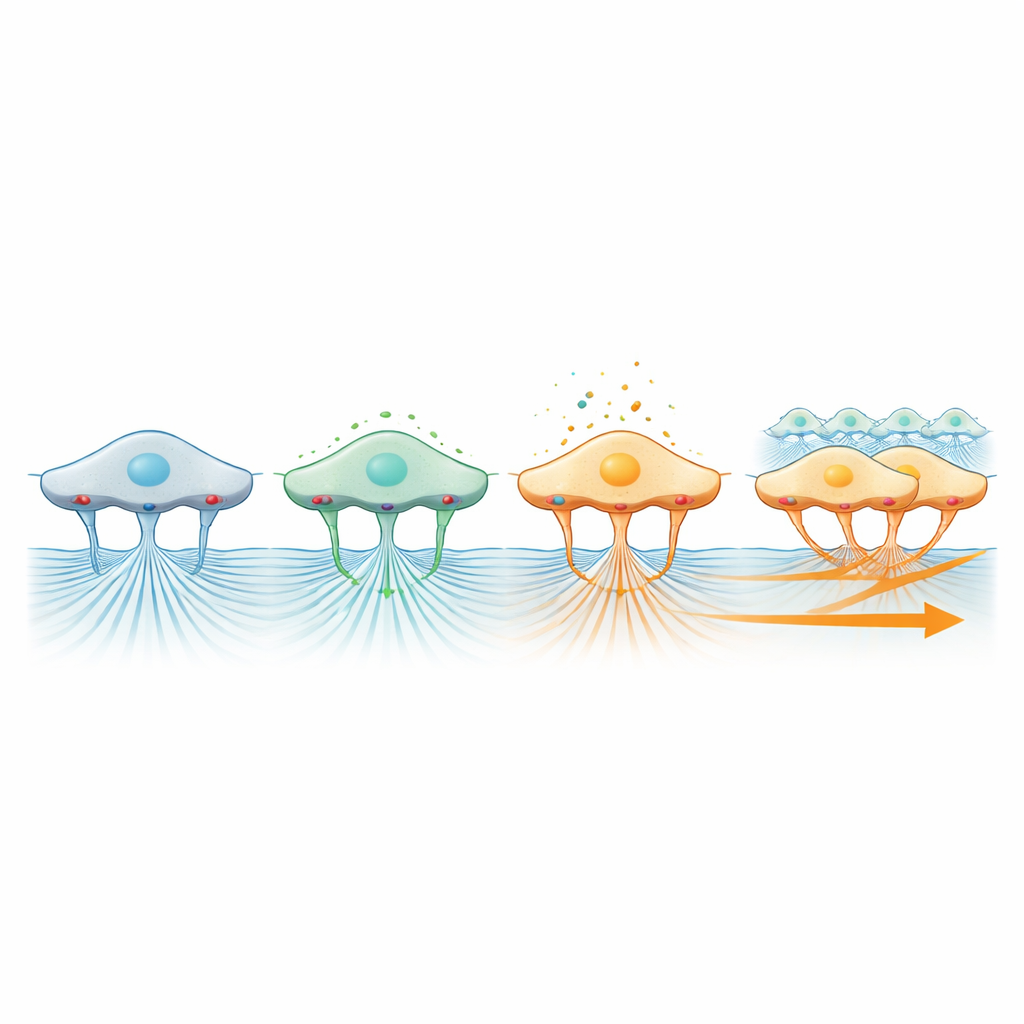
Por qué esto importa para la curación y la enfermedad
En pocas palabras, este trabajo muestra que las láminas celulares no solo se tiran entre sí; también tiran del material blando que hay debajo y a través de él, usándolo como una especie de línea telefónica mecánica. Las contracciones de la capa celular envían tensión a través de la matriz, y esa tensión, percibida mediante integrinas y canales iónicos y leída por la actividad de ERK, ayuda al grupo a moverse con rapidez y en una dirección unificada. Cuando la matriz se bloquea químicamente para impedir la propagación de fuerzas, o cuando se bloquean agarres y sensores superficiales clave, la marcha colectiva falla. Estos hallazgos profundizan nuestra comprensión de cómo se cierran las heridas, cómo los tejidos mantienen su estructura y cómo grupos celulares invasivos, como los del cáncer y la fibrosis, podrían explotar vías mecánicas en su entorno para diseminarse.
Cita: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
Palabras clave: migración colectiva de células, señalización mecánica, matriz extracelular, integrina, cicatrización