Clear Sky Science · es
Identificación in silico de antagonistas inhalables de pequeñas moléculas contra IL-33/ST2 para endotipos de asma grave tipo 2 alta
Por qué esto importa para la respiración
Para millones de personas con asma grave, incluso los inhaladores modernos y las inyecciones avanzadas pueden dejarles sin aliento y en riesgo de ataques peligrosos. Este estudio explora si fármacos familiares, tipo comprimido, podrían rediseñarse para funcionar como tratamientos inhalados que bloqueen una de las señales “de alarma” ascendentes en los pulmones. Usando únicamente simulaciones por ordenador, los investigadores buscaron pequeñas moléculas que pudieran encajar en un receptor clave implicado en el asma grave impulsada por alergias, sentando las bases para futuras pruebas en laboratorio en lugar de ofrecer un medicamento listo para usar.
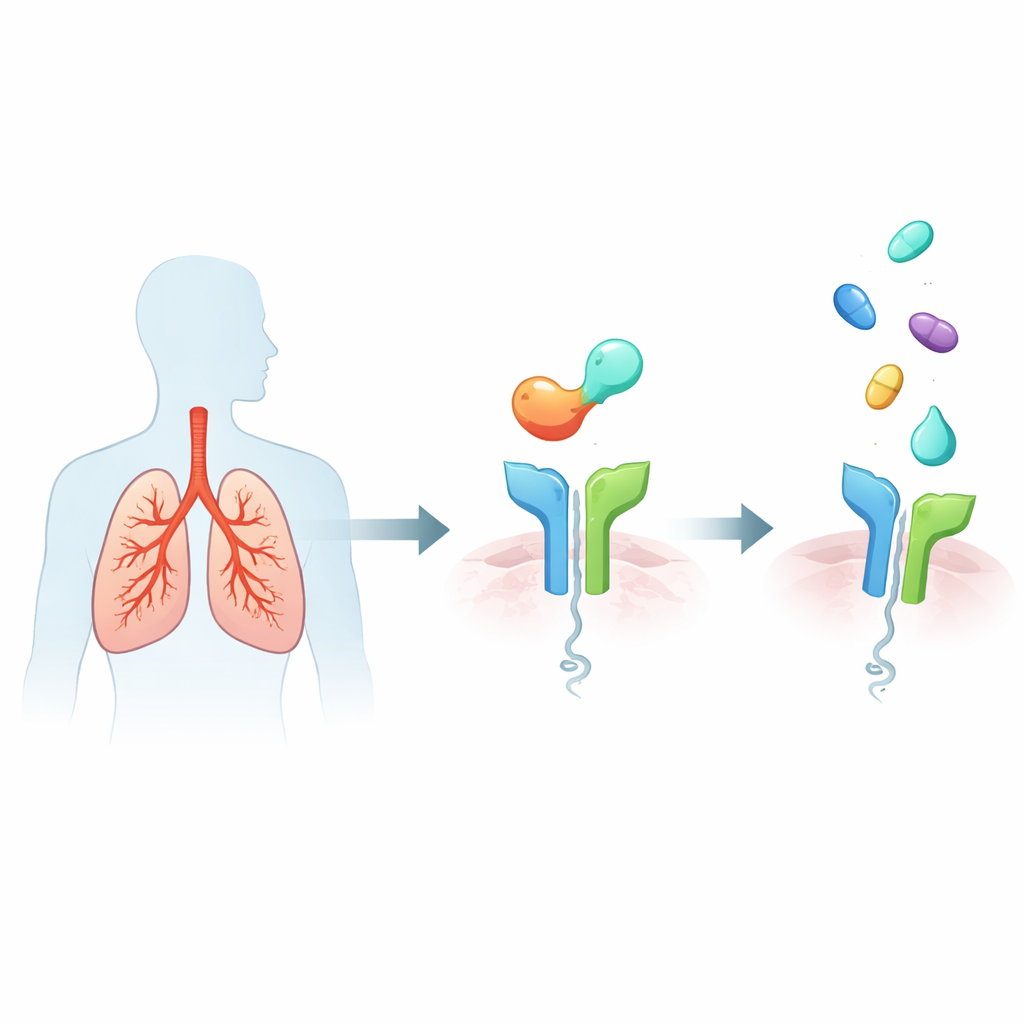
El sistema de alarma dentro de los pulmones asmáticos
El asma grave tipo 2 alta se caracteriza por una respuesta inmune hiperactiva que llena las vías respiratorias de moco y células inflamatorias, estrecha los tubos respiratorios y con el tiempo daña la estructura pulmonar. Un desencadenante importante es una proteína llamada IL-33, liberada por las células estresadas del epitelio aéreo. IL-33 se une a un receptor llamado ST2 en diversas células inmunitarias, que entonces liberan moléculas mensajeras potentes que impulsan rasgos distintivos del asma, como sibilancias, exacerbaciones y remodelado crónico de las vías aéreas. Dado que una mayor actividad IL-33/ST2 se asocia con peores síntomas y ataques más frecuentes, ST2 ha emergido como un objetivo ascendente atractivo: bloquear ST2 podría silenciar muchas de las señales inflamatorias aguas abajo a la vez.
De los anticuerpos a fármacos de uso cotidiano
Varias terapias actuales para el asma grave usan anticuerpos inyectables que eliminan proteínas inflamatorias en la sangre o bloquean sus receptores. Aunque son eficaces para algunos, estos fármacos biológicos son caros, deben administrarse por inyección y se centran principalmente en señales más lejos en la vía. En contraste, los fármacos de pequeñas moléculas—más parecidos a comprimidos o inhaladores tradicionales—podrían fabricarse a escala, almacenarse con facilidad y potencialmente entregarse directamente en los pulmones. El desafío es que ST2 se une a IL-33 a través de una amplia interfaz proteína–proteína, lo que resulta más difícil de interrumpir para pequeñas moléculas que un bolsillo profundo y bien definido en una enzima. Por ello, los autores recurrieron a datos estructurales de alta resolución del complejo ST2–IL-33 y a herramientas modernas in silico para ver si algún fármaco antiinflamatorio conocido podría, inesperadamente, encajar en parte de esta interfaz.
buscando la superficie del receptor por ordenador
Empleando la estructura cristalina humana de ST2 unida a IL-33, el equipo primero retiró IL-33 para exponer la superficie de unión del receptor y utilizó un programa de detección de bolsillos para identificar la región más prometedora en la que una pequeña molécula pudiera alojarse. Luego seleccionaron diez pequeñas moléculas clínicamente relevantes ya usadas en asma o enfermedades inmunes relacionadas—como los bloqueadores de leucotrienos Montelukast y Zafirlukast, parientes inmunomoduladores de la talidomida y inhibidores de JAK—más una molécula previamente reportada dirigida a ST2 como referencia. Con software de acoplamiento virtual, cada compuesto se posicionó miles de veces sobre la superficie de ST2, y las poses mejor ajustadas se puntuaron según la afinidad de unión predicha. Zafirlukast emergió como el andamiaje mejor clasificado, superando ligeramente a Montelukast y al comparador conocido dirigido a ST2.
Afinando una molécula líder en pantalla
Dado que Zafirlukast mostró el equilibrio más prometedor entre unión predicha y comportamiento farmacológico, los autores usaron una herramienta de diseño guiada por IA para crear una versión modificada de esta molécula. El objetivo fue conservar su unión a ST2 mejorando al mismo tiempo su perfil de seguridad predicho. El análogo rediseñado presentó una puntuación de acoplamiento muy similar y se predijo que sería menos tóxico in silico. Mapas detallados de contactos sugirieron que tanto el compuesto parental como el modificado tocan varios de los mismos aminoácidos de ST2 que normalmente contactan IL-33, lo que insinúa que ocupan partes funcionalmente importantes de la interfaz. Simulaciones extendidas de dinámica molecular—medio microsegundo de movimiento virtual en agua y sal—mostraron que el receptor y el ligando permanecieron flexibles, con la pequeña molécula muestreando distintas posiciones a lo largo de la superficie en lugar de bloquearse rígidamente. Cálculos de energías de interacción a lo largo del tiempo apuntaron a una asociación significativa pero dinámica, coherente con una molécula que explora una superficie proteína–proteína relativamente plana.
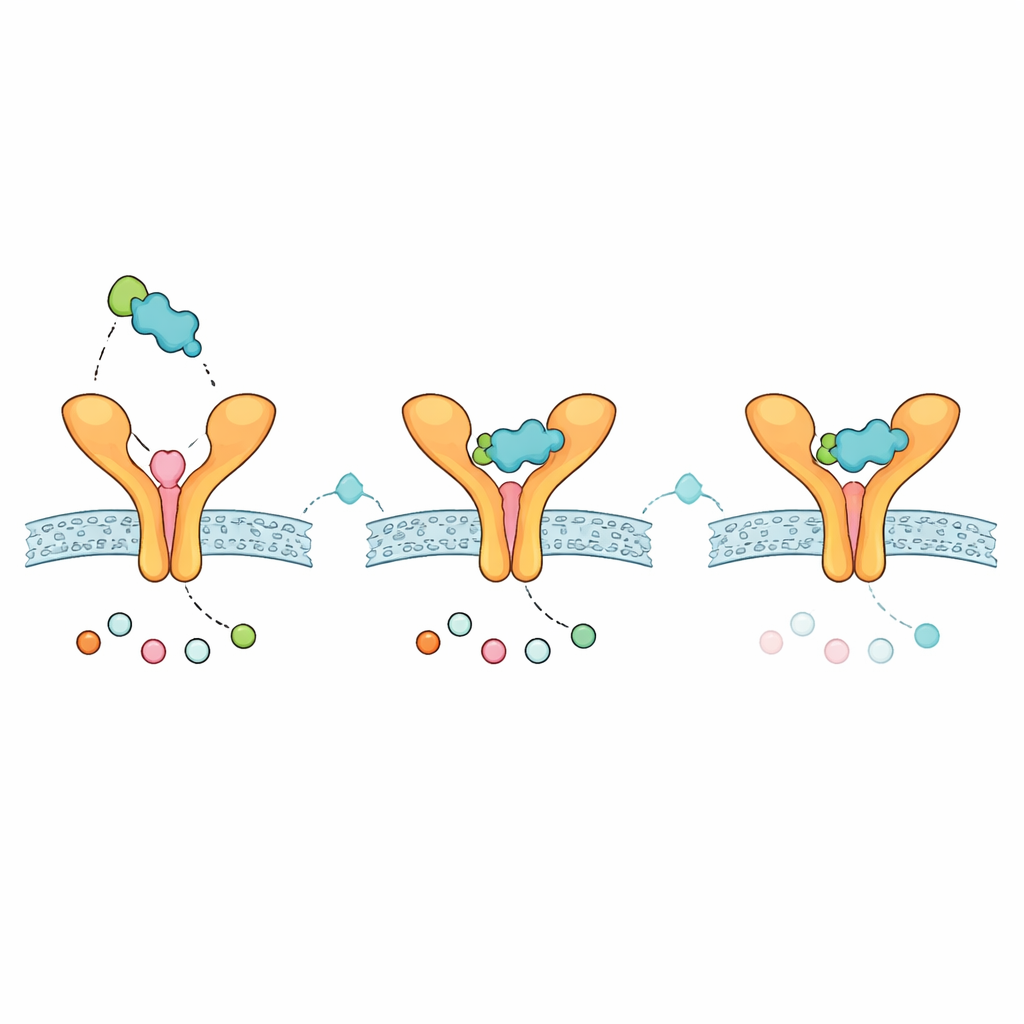
Pistas sobre cómo podría comportarse un futuro inhalador
Para explorar si el Zafirlukast modificado podría funcionar plausiblemente como medicamento, el equipo realizó controles computacionales estándar de absorción, distribución, metabolismo, excreción y toxicidad. El análogo cumplió las reglas comunes de parecido a fármaco oral, mostró tamaño y lipofilia moderados y se predijo que no penetraría en el cerebro—características que pueden ser favorables para un tratamiento centrado en el pulmón con efectos secundarios sistémicos limitados. Las estimaciones de solubilidad variaron según el modelo, lo que implica que sería necesaria una formulación cuidadosa, especialmente para vías no orales como la inhalación. Además, se predijo que el compuesto interactuaría con ciertas enzimas hepáticas, lo que sugiere que las posibles interacciones farmacológicas deberían considerarse si alguna vez se usara junto a otros medicamentos.
Lo que este trabajo realmente muestra
En lugar de entregar un nuevo fármaco para el asma, este estudio demuestra una estrategia computacional paso a paso para encontrar y refinar pequeñas moléculas que puedan interferir con el sistema de alarma IL-33/ST2 en la superficie de las células aéreas. Destaca a Zafirlukast y a un pariente optimizado por IA como puntos de partida plausibles para experimentos de laboratorio, mostrando que pueden ocupar partes clave de la interfaz ST2 y presentar propiedades previsibles de seguridad y semejanza farmacológica aceptables. Sin embargo, toda la evidencia es virtual: el trabajo no prueba que estas moléculas bloqueen la unión de IL-33 a ST2, atenúen la señalización inflamatoria o ayuden a los pacientes a respirar mejor. Esas respuestas requerirán pruebas bioquímicas, estudios celulares, modelos animales y, finalmente, ensayos clínicos. Por ahora, el estudio ofrece una hoja de ruta computacional y una lista corta de andamiajes candidatos para científicos que buscan convertir el propio interruptor de alarma del asma en un objetivo farmacológico inhalable y práctico.
Cita: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Palabras clave: asma grave, vía IL-33 ST2, antagonistas de pequeñas moléculas, diseño de fármacos in silico, terapéuticos inhalados