Clear Sky Science · es
El modelado estructural revela la base molecular de la nueva actividad de CYP153A6 hacia derivados del tolueno
Delegar trabajos químicos difíciles a la naturaleza
Químicos e industria dependen de reacciones que incorporan oxígeno en enlaces carbono–hidrógeno resistentes, por ejemplo para limpiar contaminantes o para sintetizar ingredientes de fármacos y fragancias. Hacer esto de manera limpia, sin productos químicos agresivos ni residuos de metales pesados, es difícil. Este estudio examina un catalizador natural, una enzima llamada CYP153A6 de una bacteria del suelo, y plantea una pregunta sencilla con grandes implicaciones: ¿se puede orientar esta enzima para que seleccione y "mejore" compuestos semejantes al tolueno—componentes comunes de combustibles y disolventes—convirtiéndolos en productos más útiles y respetuosos con el medio ambiente?
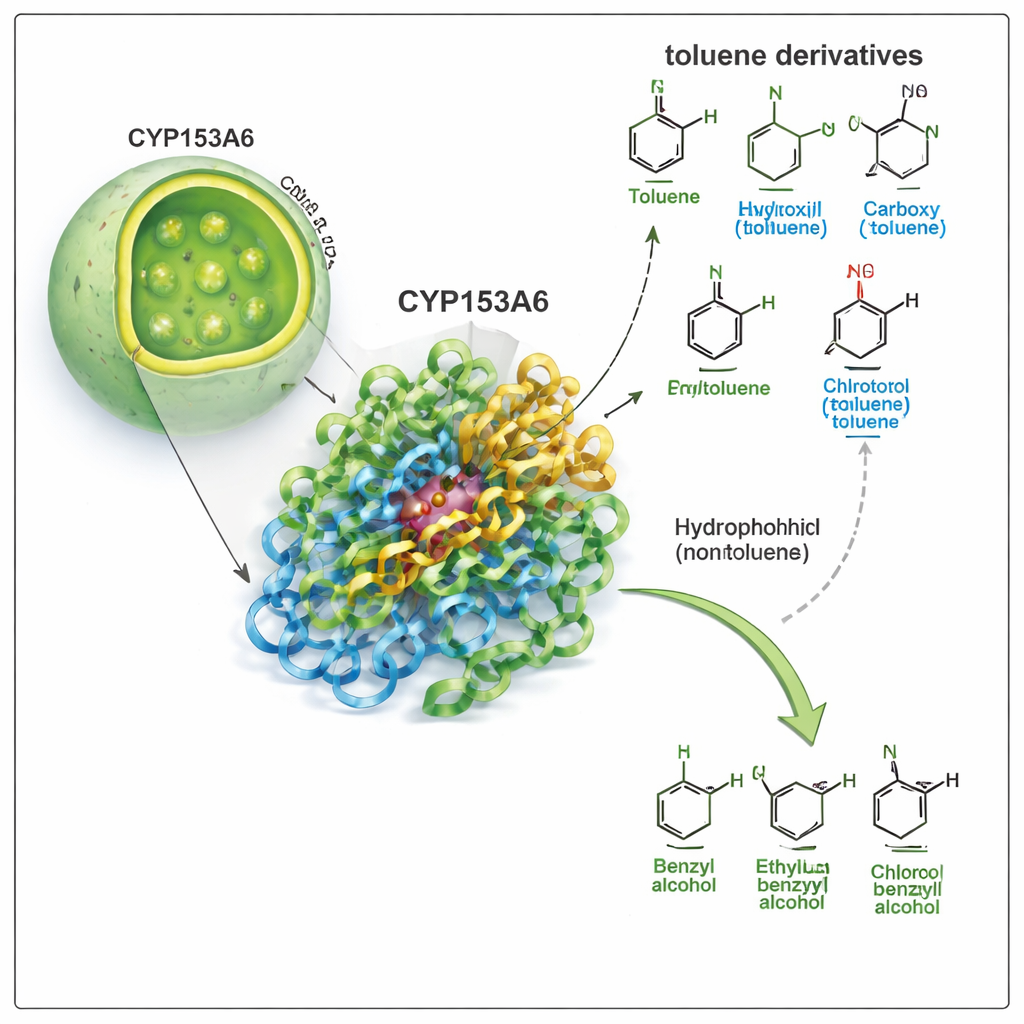
Una enzima que elige un único punto
CYP153A6 pertenece a la amplia familia de los citocromos P450, los versátiles especialistas naturales en oxidorreducción. A diferencia de muchos catalizadores industriales, esta enzima actúa en agua, a temperatura moderada, y elige posiciones muy específicas en la molécula. Trabajos previos mostraron que CYP153A6 introduce oxígeno en los extremos de cadenas hidrocarbonadas simples y en ciertos compuestos aromáticos de origen vegetal. Aquí, los autores se preguntan si también puede atacar la posición “benílica”, la pequeña cadena lateral unida a un anillo bencénico, en tolueno y compuestos relacionados. Esa transformación convierte derivados del tolueno en alcoholes bencílicos, bloques de construcción valiosos para farmacéuticos, sabores y productos químicos finos.
Probar qué moléculas prefiere la enzima
El equipo realizó primero experimentos de biotransformación usando células de E. coli modificadas que producen CYP153A6, tanto como células completas como extractos celulares. Expusieron la enzima a un panel de derivados del tolueno, variando el grupo unido al anillo aromático (por ejemplo metilo, cloro, metoxi, hidroxilo o nitro) y su posición (para, meta u orto). La enzima funcionó muy bien con compuestos apolares o apenas polares, como p-cimeno, p-xileno, p-metil-anisole y p-clorotolueno, convirtiendo de forma consistente el grupo metílico benílico en un alcohol bencílico. Sorprendentemente, ignoró por completo moléculas más polares como p-cresol, p-metil bencil alcohol y p-nitrotolueno, pese a su similitud estructural. Este patrón sugiere que el bolsillo de la enzima es fuertemente hidrófobo y desfavorece grupos polares.
Construir un mapa 3D de la máquina molecular
Dado que la estructura tridimensional de CYP153A6 no se había resuelto experimentalmente, los investigadores construyeron un modelo por ordenador de alta calidad usando un P450 estrechamente relacionado cuya estructura sí se conoce. Validaron el modelo comprobando su geometría y ejecutando largas simulaciones de dinámica molecular para ver si la proteína permanecía estable con el tiempo, lo cual ocurrió. Las simulaciones revelaron un sitio activo enterrado conectado con el exterior por túneles estrechos a través de los cuales entran los sustratos y salen los productos. Estos túneles están conformados y regulados por bucles flexibles en la superficie de la proteína, lo que ayuda a explicar cómo la enzima puede guiar moléculas hidrófobas hasta el centro reactivo del hemo al tiempo que permite la salida de agua y de los productos oxidados.
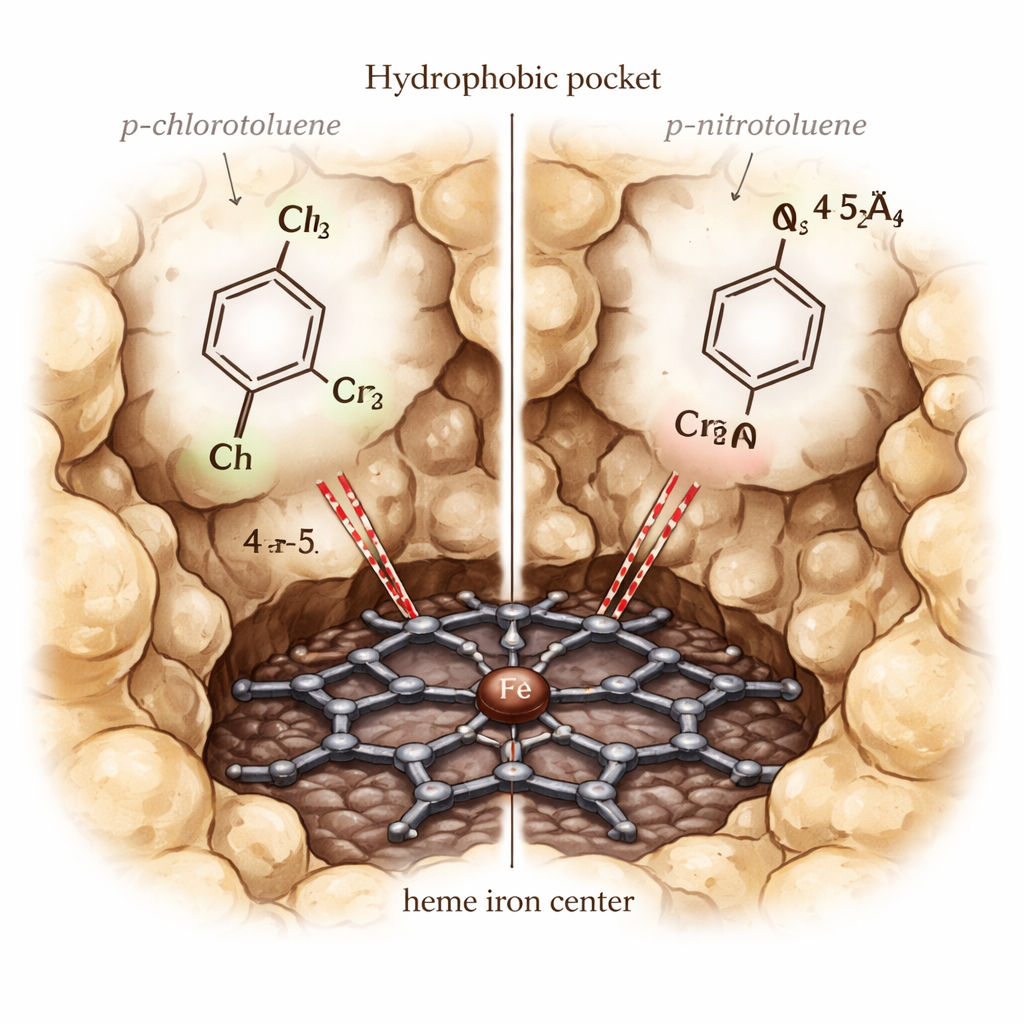
Observar cómo las moléculas encajan, se mueven y reaccionan
Con el modelo disponible, los autores simularon cómo se unen distintos derivados del tolueno dentro de CYP153A6. Usaron un enfoque llamado acoplamiento por conjuntos (ensemble docking), probando muchas formas proteicas sutilmente diferentes y varios estados electrónicos del hierro del hemo, para identificar qué configuraciones distinguían mejor a los verdaderos sustratos de los no sustratos. El escenario ganador empleó el hierro en su estado férrico de reposo y sin moléculas de agua adicionales en el bolsillo, y favoreció correctamente a los sustratos conocidos. Simulaciones de seguimiento rastrearon, cuadro por cuadro, cómo se posicionaba cada molécula respecto al hemo. Buenos sustratos como p-cimeno y p-xileno permanecieron cerca del hierro con su grupo metílico benílico orientado hacia él, y sus energías de unión previstas eran claramente favorables. Los malos sustratos tendían a alejarse, adoptar orientaciones incómodas o interactuar desfavorablemente con las cadenas laterales mayoritariamente oleosas que revisten el bolsillo.
Por qué un parecido reacciona y otro no
Surgió un rompecabezas: p-clorotolueno es oxidado eficientemente por CYP153A6, mientras que p-nitrotolueno no lo es, aunque ambos encajan en el bolsillo y se unen con fuerza similar en las simulaciones. Para resolver esto, los autores realizaron cálculos más detallados de mecánica cuántica/mecánica molecular (QM/MM) sobre el estado altamente reactivo “Compuesto I” de la enzima. Estos cálculos mostraron que el grupo nitro atrae tanta densidad electrónica desde el carbono benílico que este se vuelve muy difícil de oxidar, pese a estar geométricamente lo bastante cerca. En contraste, el grupo cloro permite una mejor comunicación electrónica entre el hemo y el sustrato, reflejada en una mayor densidad de espín en el anillo aromático y en el grupo metilo, y en una alineación más reactiva para el paso crítico de abstracción de hidrógeno.
Qué significa esto para una química más limpia
En términos cotidianos, CYP153A6 actúa como un pequeño guante aceitoso que sujeta ciertos compuestos de tipo combustible en la posición adecuada para que se añada oxígeno en un punto específico—convirtiéndolos en productos más solubles en agua, más útiles y, en última instancia, más degradables. El estudio muestra que la enzima prefiere sustituyentes no polares y que tanto la forma como el flujo electrónico determinan si un derivado del tolueno será transformado. Al aclarar cómo CYP153A6 reconoce y activa estas moléculas, el trabajo traza un plan para diseñar versiones mejoradas que podrían ayudar a limpiar contaminantes aromáticos o a fabricar productos químicos complejos de manera más sostenible.
Cita: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Palabras clave: biocatálisis, citocromo P450, hidroxilación de tolueno, ingeniería de enzimas, química verde