Clear Sky Science · es
Biofactoría transplastómica para la producción de α‑lactoalbúmina humana funcional para aplicaciones nutricionales y terapéuticas
Convertir plantas en fábricas de proteínas de la leche
Las dietas modernas dependen en gran medida de las proteínas de la leche, pero la cría de vacas a escala global acarrea costes ambientales y cuestiones éticas. Este estudio explora una forma muy distinta de producir una proteína clave de la leche humana: enseñando a las hojas de plantas a fabricarla. El trabajo demuestra que plantas de tabaco pueden reprogramarse para manufacturar α‑lactoalbúmina humana, una proteína importante para la nutrición infantil y con potenciales propiedades anticancerígenas, abriendo una vía hacia ingredientes para fórmulas infantiles sin origen animal y nuevos componentes alimentarios con actividad antitumoral.
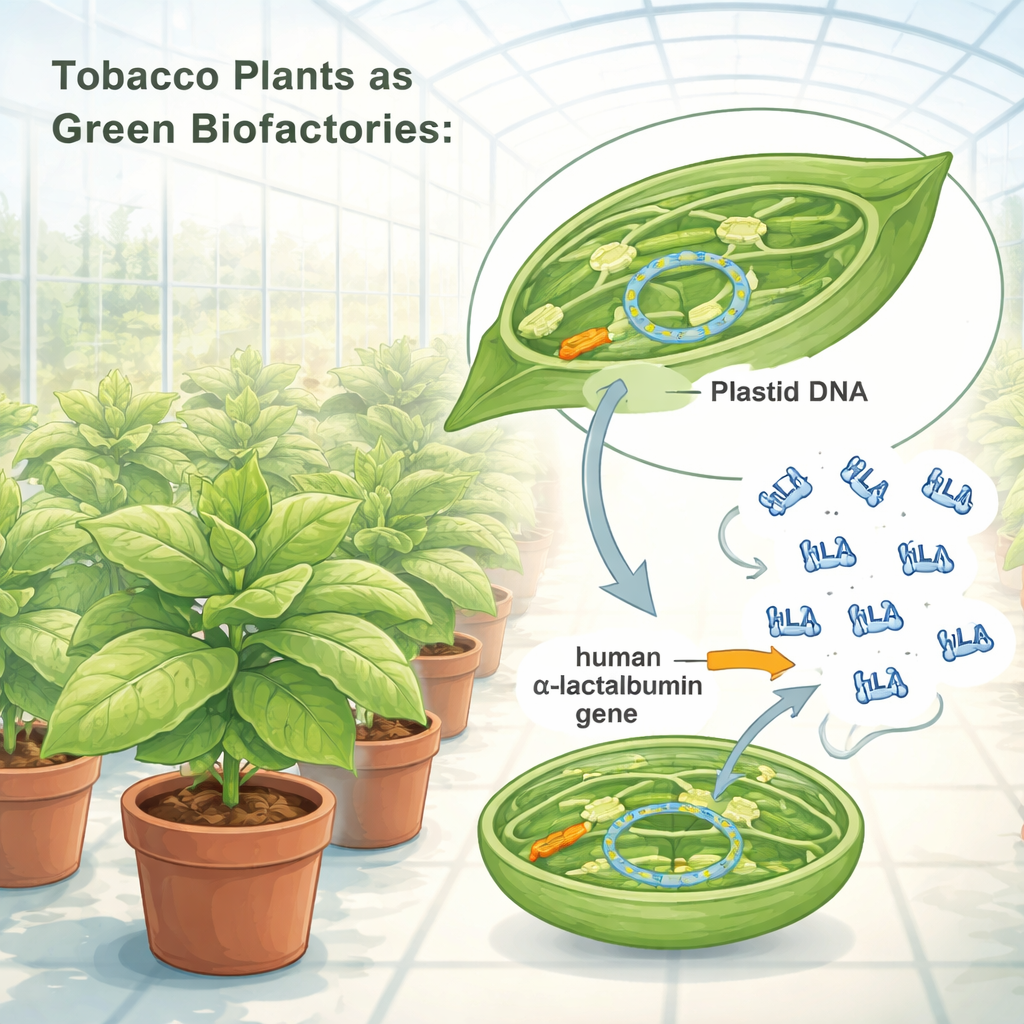
Por qué importa esta proteína de la leche
La leche materna humana es más que alimento; es un cóctel afinado de proteínas, grasas y azúcares que cambia según las necesidades del lactante. Una de sus proteínas más importantes es la α‑lactoalbúmina, que ayuda a sintetizar la lactosa, el azúcar principal de la leche y una fuente crítica de energía para los bebés. La α‑lactoalbúmina es rica en aminoácidos esenciales, incluido el triptófano, precursor de la serotonina, el neurotransmisor asociado al bienestar, y se ha relacionado con mayor resiliencia al estrés y posible protección frente a ciertos cánceres. Por ser fácil de digerir, de sabor suave y estable en un amplio rango de acidez, se usa ampliamente en fórmulas infantiles y bebidas nutricionales—y la demanda está en aumento.
El problema de la lechería tradicional
Depender de las vacas para suministrar proteínas lácteas tiene inconvenientes. El ganado genera una parte considerable de las emisiones globales de gases de efecto invernadero, y las grandes explotaciones lecheras requieren enormes cantidades de tierra, agua y pienso. Además, la gestión de las granjas puede introducir preocupaciones sobre hormonas, antibióticos y patógenos en la cadena de la leche. Estas presiones han impulsado el interés por enfoques de «agricultura celular», donde las proteínas lácteas las producen microbios o células cultivadas en lugar de animales. Sin embargo, muchos de estos sistemas siguen siendo caros, difíciles de escalar o generan proteínas que no son exactamente idénticas a las humanas. Las plantas, y en especial sus cloroplastos foliares—las pequeñas fábricas verdes que impulsan la fotosíntesis—ofrecen una plataforma alternativa prometedora.
Reprogramar cloroplastos como biofactorías
Los investigadores rediseñaron las instrucciones genéticas de la α‑lactoalbúmina humana para que los cloroplastos del tabaco pudieran leerlas de forma eficiente. Insertaron este gen optimizado en el ADN del cloroplasto, usando un «casete genético» construido con potentes elementos reguladores vegetales que actúan como interruptores de encendido‑apagado. Mediante un método de bombardeo de partículas, introdujeron este casete en las células foliares del tabaco y luego seleccionaron plantones cuyos cloroplastos habían adoptado completamente el nuevo gen. Pruebas genéticas confirmaron que todas las copias del ADN de cloroplasto en estas plantas llevaban ahora el plano para la proteína humana. Las plantas modificadas crecieron normalmente en condiciones de invernadero, produciendo semillas y sin mostrar penalizaciones visibles en tamaño, forma o fertilidad, lo que sugiere que la carga extra de proteína no dañó la salud vegetal.
Demostrar que la proteína producida en planta funciona
A continuación, el equipo preguntó si la α‑lactoalbúmina producida en planta se comportaba como la proteína humana auténtica. Extrajeron proteínas solubles de las hojas, purificaron la α‑lactoalbúmina y examinaron su estructura mediante una técnica que informa sobre el plegamiento proteico. La «huella» espectral de la proteína derivada de la planta se solapó casi por completo con la de la α‑lactoalbúmina humana comercial, indicando un plegamiento similar. Funcionalmente, la proteína vegetal activó la enzima sintetizadora de lactosa casi tan bien como la versión nativa, impulsando la formación de lactosa a aproximadamente el 93 % de la tasa de la proteína estándar. De forma notable, la α‑lactoalbúmina se acumuló hasta alrededor del 23 % de toda la proteína soluble en las hojas—uno de los niveles más altos reportados para proteínas humanas producidas en cloroplastos vegetales—lo que sugiere que este sistema puede ofrecer rendimientos relevantes a escala industrial.
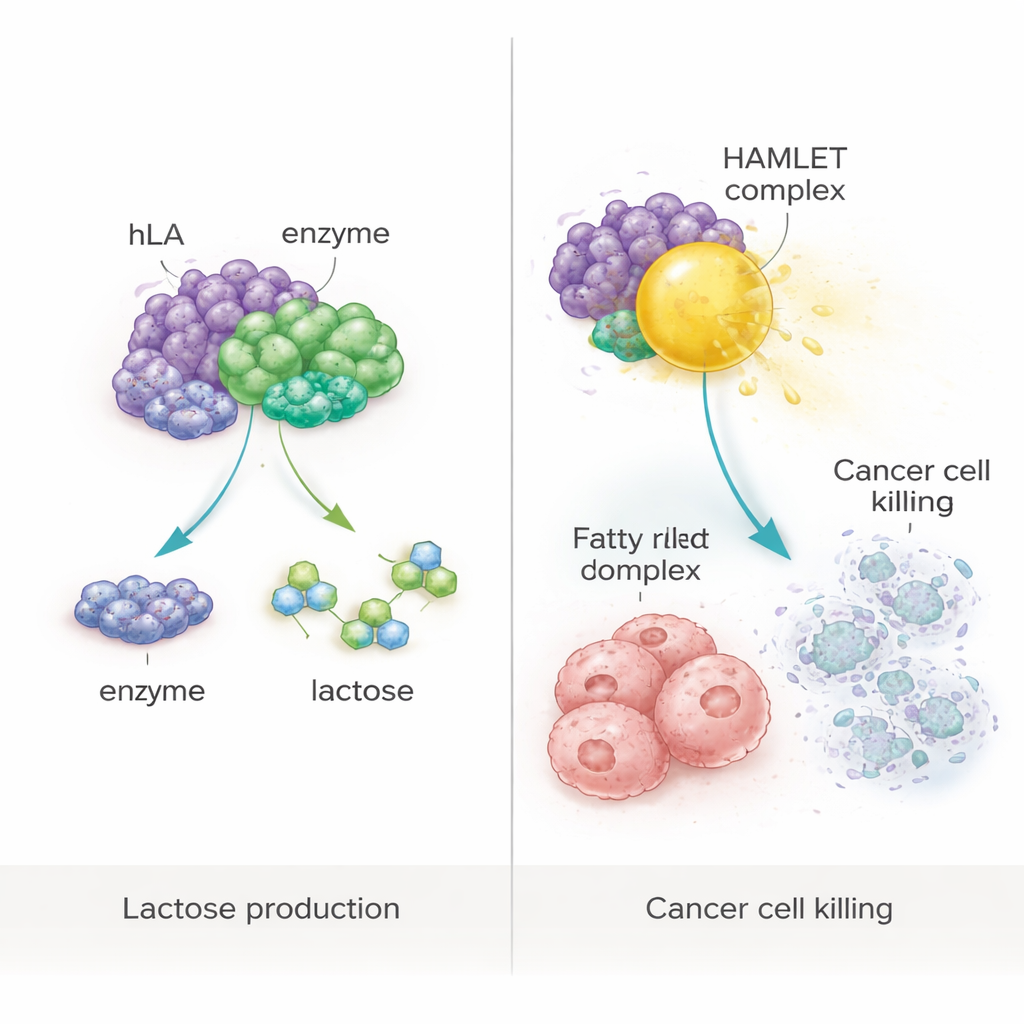
De la nutrición a complejos anticáncer
El estudio también probó una idea más ambiciosa: usar la proteína producida en planta como bloque de construcción para un complejo anticáncer conocido como HAMLET, que se forma cuando la α‑lactoalbúmina se une estrechamente al ácido oleico, un ácido graso común. Al calentar suavemente la proteína purificada de la planta con ácido oleico bajo condiciones controladas, los investigadores crearon un complejo similar a HAMLET. Cuando se aplicó a células humanas de cáncer colorrectal (WiDr) y de mama (MCF‑7) en cultivo, este complejo redujo drásticamente la supervivencia celular a menos del 10 %. Análisis posteriores mostraron que la mayoría de las células afectadas estaban entrando en apoptosis, una forma de muerte celular programada en lugar de una ruptura descontrolada. Es importante señalar que ni la proteína sola, ni el ácido graso solo, ni extractos de plantas no modificadas desencadenaron muerte celular significativa, lo que confirma que el efecto citotóxico dependía del complejo específico.
Qué podría significar para futuros alimentos y medicinas
En conjunto, el trabajo muestra que los cloroplastos de las plantas pueden producir de forma fiable grandes cantidades de una proteína de la leche humana que es tanto nutricionalmente relevante como terapéuticamente activa. Para un público no especializado, esto significa que en el futuro las fórmulas infantiles, los alimentos funcionales o los suplementos podrían fabricarse con proteínas cultivadas en hojas en lugar de extraerse de vacas, reduciendo el impacto ambiental y adaptándose más estrechamente a la biología humana. Al mismo tiempo, la misma proteína derivada de plantas puede convertirse en el laboratorio en un complejo anticáncer dirigido, apuntando a vías basadas en plantas para bioterapéuticos asequibles. Aunque se necesita más investigación para confirmar la seguridad y el rendimiento en animales y personas—y para transferir esta tecnología a cultivos comestibles—el estudio ofrece un vistazo convincente de las plantas multiplicando su papel como mini‑fábricas para la próxima generación de nutrición y medicina.
Cita: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Palabras clave: proteínas lácteas producidas en plantas, biofactoría de cloroplastos, alfa‑lactoalbúmina humana, alternativas lácteas sostenibles, terapia contra el cáncer HAMLET