Clear Sky Science · es
La integrina αv contribuye a la regulación de la rigidez de las células musculares lisas vasculares
Por qué importa la “elasticidad” de las arterias
A medida que envejecemos o desarrollamos hipertensión, nuestras arterias grandes van perdiendo gradualmente su elasticidad natural y se vuelven más rígidas. Este cambio obliga al corazón a trabajar más y aumenta el riesgo de infartos, accidentes cerebrovasculares y otros problemas cardiovasculares. Los científicos hace tiempo que saben que los materiales que componen las paredes arteriales—proteínas como la elastina y el colágeno—influyen en la rigidez. Este estudio plantea una pregunta más sutil: ¿pueden las propias células musculares dentro de las paredes arteriales volverse más rígidas, y ayuda una pequeña familia de receptores de superficie llamada integrina αv a mantener esas células, y por tanto nuestras arterias, más flexibles?
Las células musculares que moldean el flujo sanguíneo
Las arterias grandes no son solo tubos pasivos. Su capa media está repleta de células musculares lisas vasculares, que pueden contraerse y relajarse para ajustar con precisión el flujo y la presión sanguínea. Estas células están ancladas a un andamiaje circundante conocido como matriz extracelular. Los investigadores se centraron en un grupo de moléculas de anclaje, la integrina αv, que atraviesa la superficie celular y enlaza físicamente el esqueleto interno de la célula con ese andamiaje externo. Trabajos previos sugerían que la integrina αv participaba en la cicatrización y remodelado vascular, pero no quedaba claro si también controlaba la rigidez de las propias células musculares, sobre todo bajo el estrés de hormonas como la angiotensina II, que elevan la presión arterial y promueven la fibrosis.
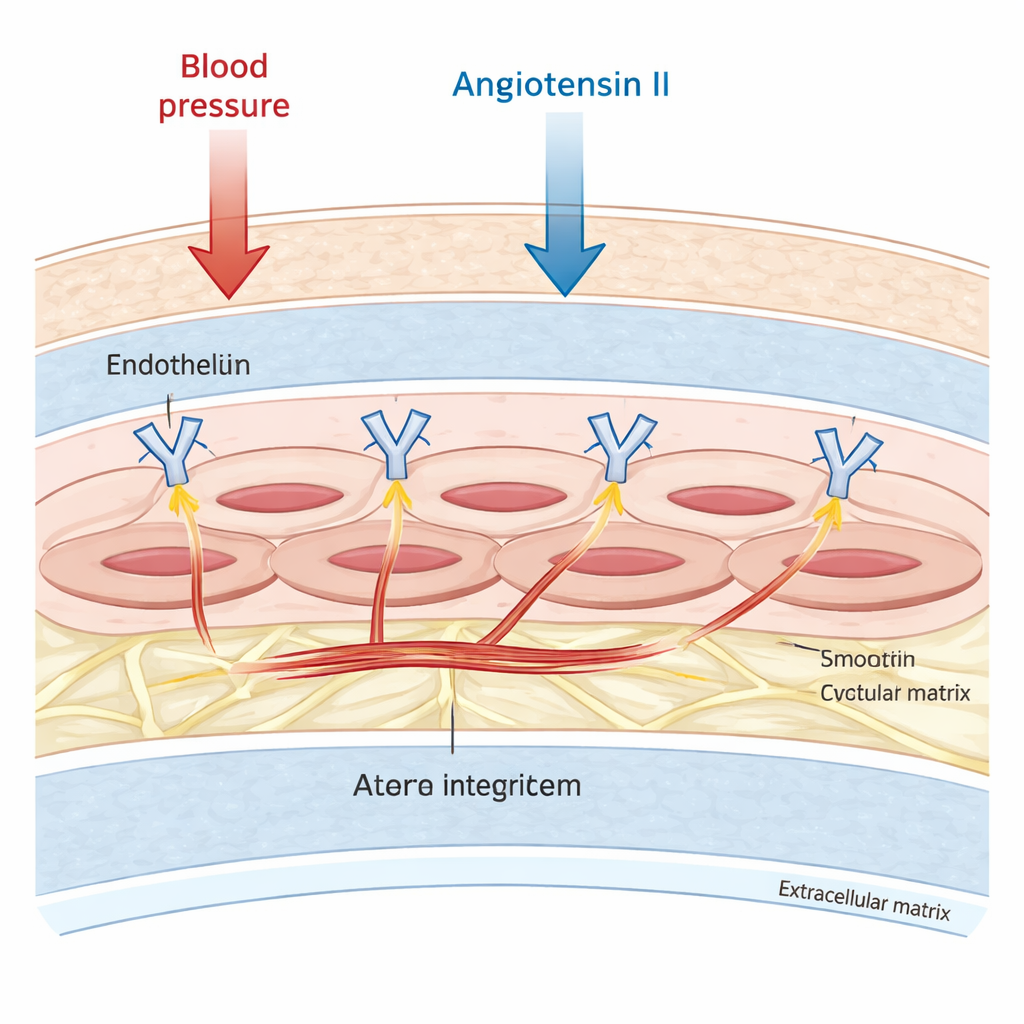
Midiendo la rigidez una célula a la vez
Para abordar esto, el equipo usó células musculares lisas de ratón cultivadas en laboratorio y ratones diseñados para carecer de integrina αv específicamente en sus células musculares vasculares. Midieron la rigidez celular con microscopía de fuerza atómica, una técnica en la que una punta ultra‑fina indenta suavemente la superficie celular y registra la fuerza necesaria. Las células sin integrina αv eran más del doble de rígidas que las células de control en condiciones tranquilas. Al exponerse a angiotensina II durante dos días, estas células deficientes aumentaron su rigidez aproximadamente tres veces más, mientras que las células normales apenas cambiaron. Dado que sus mediciones usaron indentaciones muy superficiales, los autores construyeron un modelo informático detallado de una célula muscular lisa y simularon indentaciones más profundas. Las simulaciones mostraron que las pruebas superficiales enfatizan la contribución de la capa externa y la región cortical de la célula, y todavía encajaban dentro del rango observado en las células mutantes rígidas, lo que apoya los hallazgos biológicos.
Un esqueleto interno remodelado
El siguiente paso fue mirar dentro de las células. Usando tintes fluorescentes y microscopía, los investigadores examinaron la actina, un filamento clave que forma el andamiaje interno de la célula. Las células musculares de control mostraron una red de actina relativamente difusa, incluso tras el tratamiento con angiotensina II. En cambio, las células sin integrina αv formaron gruesas fibras de tensión que cruzaban la célula y, después de la exposición hormonal, una banda intensa de actina justo debajo de la membrana celular, conocida como actina cortical. Una medida cuantitativa de cuánto actina se acumulaba cerca del borde celular confirmó que esta capa cortical estaba fuertemente enriquecida solo en las células deficientes en integrina. Estas células también desarrollaron estructuras de adhesión inusualmente largas donde se agarran a la matriz circundante, coherente con una transición hacia adhesiones fibrilares más tensionales que pueden bloquear a la célula en un estado rígido.
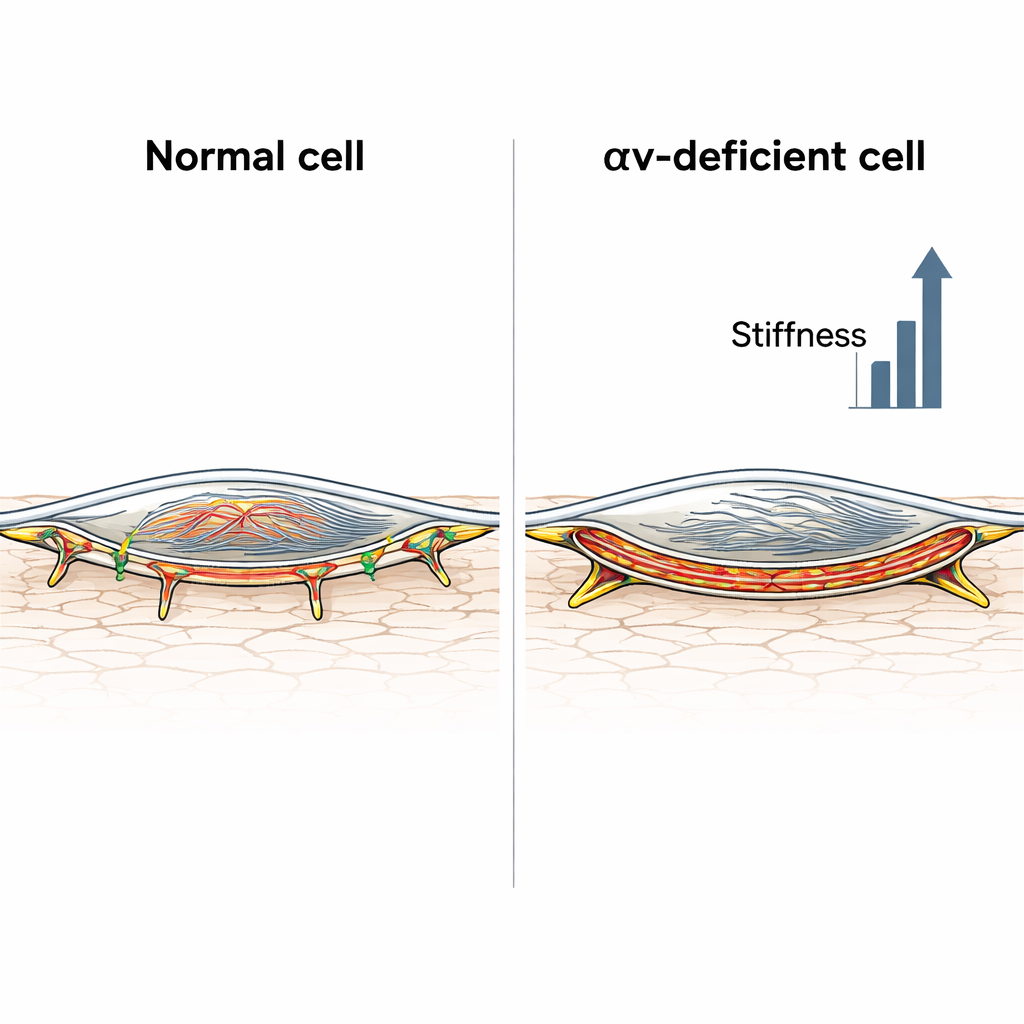
Cuando la pared parece igual pero se comporta de forma distinta
Puesto que las arterias son más que sus células musculares, los científicos también midieron las propiedades mecánicas de las arterias carótidas en ratones vivos, con y sin integrina αv en sus células musculares vasculares, y con o sin infusión crónica de angiotensina II. Sorprendentemente, la presión arterial general y la rigidez de la pared—evaluadas a partir de curvas presión‑diámetro basadas en ultrasonido—fueron similares en ambas cepas de ratón, tanto en reposo como tras el tratamiento hormonal. Sin embargo, la composición microscópica de la pared difería. Bajo angiotensina II, los ratones de control mostraron menos elastina y más colágeno, signos clásicos de una matriz más rígida, mientras que los ratones deficientes en integrina presentaron cambios relativos menores en el colágeno pero células musculares mucho más rígidas. En otras palabras, en ratones normales la matriz fue la principal responsable del endurecimiento; en los ratones sin integrina, las propias células musculares se volvieron tan rígidas que en la práctica compensaron sus alteraciones matrixales más modestas.
Qué significa esto para las arterias que envejecen
Para un público general, el mensaje clave es que la rigidez arterial no se debe solo a fibras elásticas desgastadas; también depende de cómo las células musculares en la pared organizan sus pequeños cables internos. La integrina αv ayuda normalmente a evitar que estas células se vuelvan demasiado rígidas cuando son desafiadas por hormonas como la angiotensina II. Cuando se pierde este control, las células reorganizan su andamiaje de actina—especialmente en la corteza justo bajo la membrana—y se bloquean en un estado más rígido que puede impulsar el endurecimiento arterial incluso sin cambios dramáticos en el material circundante. Esta idea apunta a nuevas estrategias terapéuticas: fármacos que aflojen o reorganizen con suavidad la red de actina cortical, o que modulen la señalización ligada a integrinas, podrían algún día complementar las terapias antihipertensivas para restaurar más directamente el “resorte” de las arterias envejecidas.
Cita: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Palabras clave: rigidez arterial, células musculares lisas vasculares, integrina alfa v, citoesqueleto de actina, angiotensina II