Clear Sky Science · es
Diseño, síntesis y evaluación antitumoral de nuevas espiroindenopiridotriazinapiranas funcionalizadas
Por qué importan los nuevos medicamentos contra el cáncer
Los tratamientos contra el cáncer han salvado muchas vidas, pero con frecuencia presentan dos grandes problemas: los tumores pueden dejar de responder a los fármacos y los tejidos sanos pueden resultar dañados junto con las células cancerosas. Este estudio explora una nueva familia de pequeñas moléculas diseñadas con cuidado para golpear con fuerza a las células tumorales mientras perjudican menos a las células normales. Al construir estos compuestos de forma inteligente y eficiente y evaluarlos en células agresivas de cáncer de mama y de páncreas, los investigadores buscan señales tempranas de futuros medicamentos más seguros y selectivos.
Construir mejores formas para fármacos
El núcleo de este trabajo es una forma química tridimensional especial llamada andamiaje espiro. Puede imaginarse como dos sistemas de anillos unidos en un único punto de pivote, lo que hace que la molécula sea rígida, compacta y más “concreta” que una cadena flexible. Muchos fármacos modernos usan este tipo de arquitectura porque les ayuda a encajar con precisión en los complejos huecos de proteínas dentro de nuestras células. En este proyecto, el equipo diseñó nuevas moléculas espiro que combinan varios tipos de anillos conocidos por estudios previos por su potencial anticancerígeno, todos fusionados en una estructura estrechamente organizada.
Una receta simple para moléculas complejas
Desde el punto de vista químico, estos compuestos espiro serían normalmente difíciles y lentos de sintetizar. En su lugar, los investigadores emplearon una estrategia multicomponente en una sola fase: se mezclan tres bloques de construcción simples y, en las condiciones adecuadas, se ensamblan por sí mismos en la estructura objetivo intricada. Tras probar distintos disolventes y temperaturas, las mejores condiciones resultaron ser etanol común a calentamiento suave, sin ningún catalizador añadido. Este enfoque produjo una pequeña biblioteca de moléculas relacionadas con elevados rendimientos, que luego analizaron en detalle con técnicas estándar para confirmar que las estructuras previstas se habían formado realmente.
Poniendo a prueba los nuevos compuestos
Una vez establecida la química, el enfoque se desplazó a la biología. El equipo expuso dos líneas celulares cancerosas difíciles de tratar —pancreáticas (Panc1) y de mama triple negativa (MDA‑MB‑231)— a las nuevas moléculas, junto con células normales derivadas de la piel como control de seguridad. Utilizando una prueba colorimétrica que mide cuántas células permanecen vivas tras el tratamiento, encontraron que tres compuestos, etiquetados 9d, 9e y especialmente 9f, destacaron por sus efectos mucho más potentes en la inhibición del crecimiento que los demás. Sorprendentemente, todos estos compuestos mostraron poco impacto sobre las células normales a las mismas concentraciones, lo que sugiere un grado de selectividad que con frecuencia falta en las quimioterapias actuales.
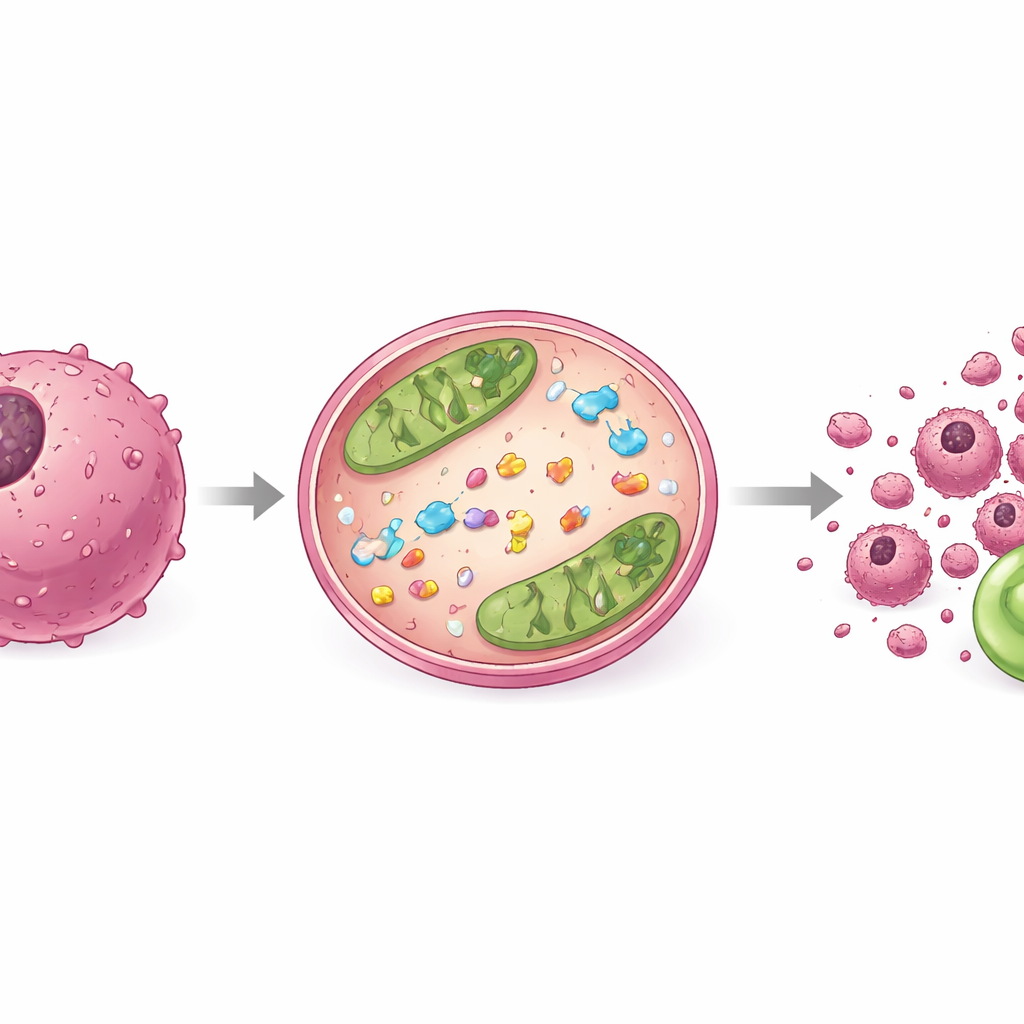
Cómo responden las células y por qué la estructura importa
Para ver qué ocurría dentro de las células cancerosas, los investigadores tiñeron su ADN y las examinaron con microscopía de fluorescencia. Las células tratadas con el compuesto más potente, 9f, mostraron núcleos encogidos y fragmentados —marcadores clásicos de muerte celular programada más que de simple envenenamiento. Experimentos adicionales examinaron dos proteínas guardianas clave que controlan este interruptor de muerte celular: una que evita la muerte y otra que la promueve. El tratamiento con 9f desplazó este equilibrio hacia la autodestrucción en las células tumorales, coherente con un impulso dirigido hacia la apoptosis. Al comparar los distintos miembros de la familia de compuestos, el equipo también observó que pequeños cambios alrededor del núcleo espiro tenían grandes efectos sobre la potencia, subrayando cómo tanto la atracción electrónica como la colocación tridimensional de los sustituyentes pueden ajustar la actividad anticancerígena.
Qué podría significar esto para futuros tratamientos
En términos sencillos, el estudio ofrece una vía práctica para sintetizar una nueva clase de moléculas rígidas y tridimensionales que pueden frenar con fuerza el crecimiento de ciertas células cancerosas mientras preservan a las normales en pruebas de laboratorio. Un candidato, 9f, fue tan eficaz como un fármaco de quimioterapia estándar frente a las líneas celulares probadas y pareció matarlas activando su programa de autodestrucción. Estos resultados son preliminares y se limitan a células cultivadas en placas: faltan estudios en animales, datos sobre la farmacocinética en el organismo y seguridad a largo plazo. Aun así, el trabajo muestra cómo el diseño molecular inteligente y métodos sintéticos eficientes pueden combinarse para generar candidatos prometedores para futuros medicamentos contra el cáncer.
Cita: Safari, F., Bayat, M., Hosseini, H. et al. Design, synthesis, and antitumor evaluation of new functionalized spiroindenopyridotriazinepyrans. Sci Rep 16, 7917 (2026). https://doi.org/10.1038/s41598-026-38946-1
Palabras clave: terapia contra el cáncer, diseño de fármacos, moléculas espirocíclicas, apoptosis, síntesis multicomponente