Clear Sky Science · es
Las A2-pancortinas interactúan con Bcl-xL y WAVE1 para promover los sitios de contacto mitocondria-RE (MERCs) y exacerbar la elevación del calcio mitocondrial para mediar la muerte celular en el ictus
Por qué importan los pequeños enlaces cerebrales en el ictus neonatal
El ictus suele considerarse una enfermedad de adultos, pero cuando afecta a recién nacidos puede dañar silenciosamente el cerebro en desarrollo y causar problemas de por vida. Este estudio examina lo que ocurre en el interior de las neuronas durante esa crisis. Los autores se centran en una familia poco conocida de proteínas llamadas pancortinas y muestran cómo dos variantes del desarrollo actúan como “potenciadores” peligrosos, estrechando las conexiones entre estructuras celulares clave y provocando una avalancha de calcio que puede empujar a las neuronas jóvenes hacia la muerte.
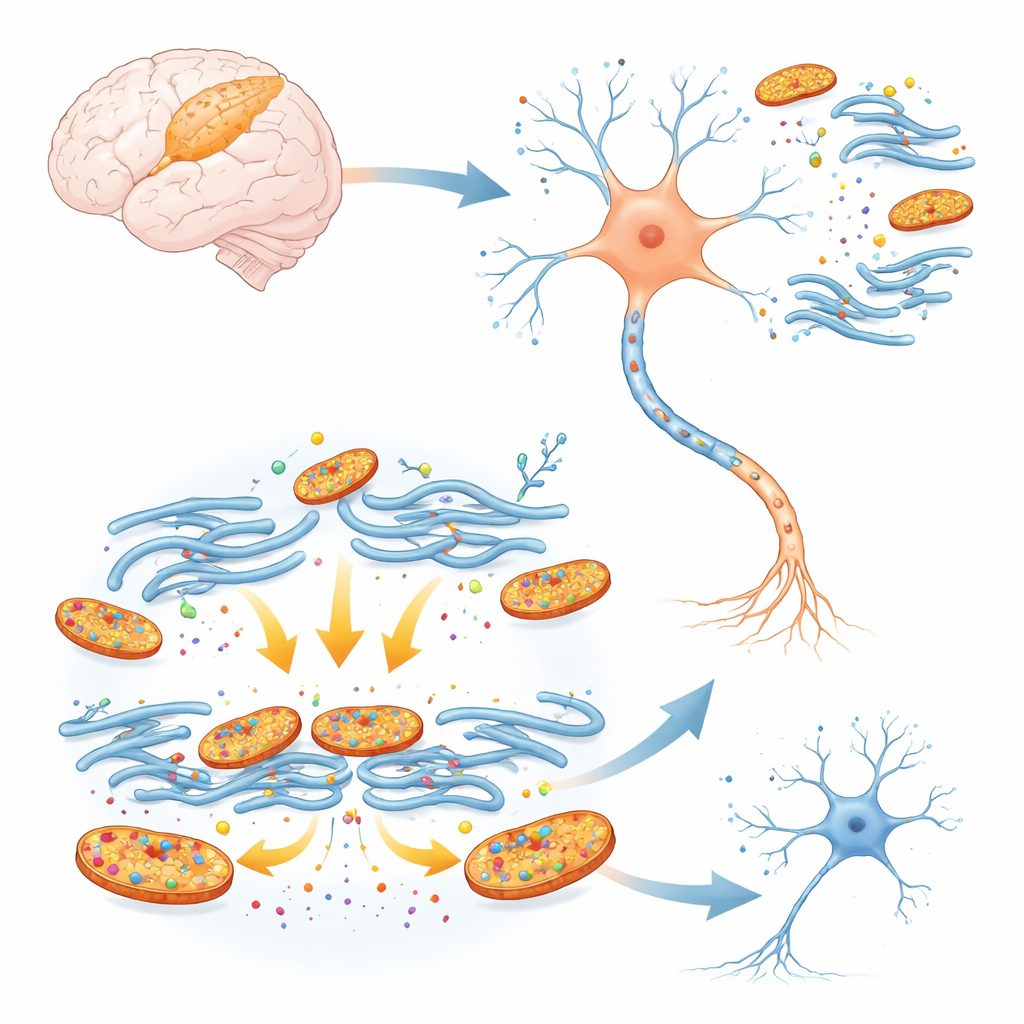
Culpables ocultos en el cerebro neonatal
Las pancortinas son proteínas tipo andamiaje que ayudan a dar forma al cerebro en crecimiento. Dos formas, denominadas A2-pancortinas, son abundantes durante el desarrollo temprano y luego desaparecen en gran medida a medida que el cerebro madura. Dado que los cerebros de los recién nacidos son especialmente vulnerables a la pérdida de oxígeno, los investigadores se preguntaron si estas proteínas propias de la primera etapa de la vida podrían empeorar el daño cuando el flujo sanguíneo hacia la corteza se interrumpe brevemente, como sucede en el ictus neonatal. En neuronas corticales de ratón cultivadas, utilizaron herramientas genéticas para reducir todos los niveles de pancortina y luego expusieron las células a una carencia de oxígeno y glucosa que imita el ictus. Las neuronas con niveles reducidos de pancortina sobrevivieron con mucha más probabilidad, lo que sugiere que estas proteínas, en lugar de proteger a las células jóvenes, contribuyen a su daño bajo estrés.
De modelos de ictus en ratón a tejido cerebral protegido
Para comprobar si este papel perjudicial también se observa en un cerebro vivo, el equipo diseñó ratones que carecen específicamente de las formas A2-pancortinas del desarrollo. Ratones jóvenes de dos semanas con el gen anulado y sus compañeros normales fueron sometidos al bloqueo de una arteria cerebral mayor, un modelo estándar de ictus isquémico. Tras un día, ambos grupos mostraron lesiones en regiones profundas del cerebro, pero la corteza de los ratones sin A2-pancortinas tenía aproximadamente la mitad del daño que la de los animales normales. De manera notable, este efecto protector desapareció en ratones de cinco semanas, cuando predominan las variantes adultas de pancortina. Estos resultados dependientes de la edad apuntan a las A2-pancortinas como factores clave pro-muerte en la corteza neonatal, vinculando un programa de desarrollo con la vulnerabilidad al ictus.
Zonas de contacto peligrosas dentro de las neuronas
Dentro de las células, las mitocondrias productoras de energía se sitúan cerca del retículo endoplásmico (RE), una red membranosa plegada que almacena calcio. Donde las dos membranas quedan en contacto estrecho, los llamados sitios de contacto mitocondria–RE actúan como túneles microscópicos por los que puede pasar el calcio. Una transferencia moderada respalda la producción de energía, pero el exceso puede sobrecargar las mitocondrias y desencadenar la muerte celular. Los investigadores hallaron que las A2-pancortinas, junto con dos socias —Bcl-xL y WAVE1—, se ensamblan en un complejo de tres partes que se localiza en estos sitios de contacto. Cuando forzaron a las células a producir A2-pancortinas adicionales junto con estas socias, mitocondrias y RE se aproximaron con más frecuencia y mayor firmeza, según informó un sensor fluorescente dividido especializado. Una proteína de unión llamada GRP75 se incorporó a este complejo, ayudando a estabilizar las zonas de contacto.
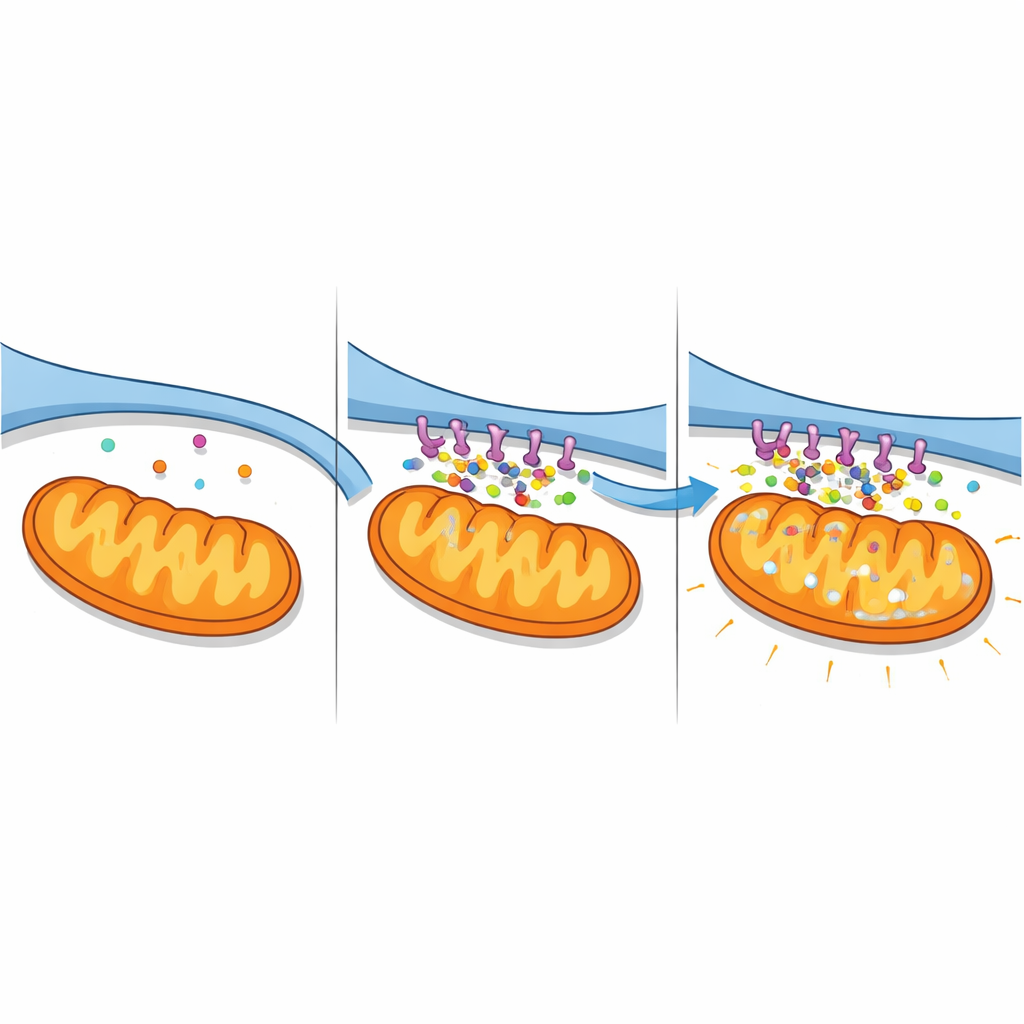
Avalanchas de calcio y centrales eléctricas fallidas
El reforzamiento de los contactos tuvo consecuencias importantes para el equilibrio del calcio. Usando indicadores fluorescentes que informan por separado del calcio en el citosol, el RE y las mitocondrias, los autores observaron los cambios a lo largo del tiempo. Las células que expresaban el complejo A2-pancortina mostraron un aumento sostenido de calcio dentro de las mitocondrias y en el fluido circundante, junto con una caída en las reservas del RE, una firma de transferencia masiva desde el RE hacia las mitocondrias. Bloquear un canal clave de liberación de calcio en la superficie del RE (IP3R) evitó en gran medida estos cambios, confirmando que el complejo amplifica una vía específica del RE a la mitocondria. En células neuronales expuestas a la privación de oxígeno y glucosa típica del ictus, la reducción de pancortinas tuvo el efecto opuesto: la sobrecarga de calcio se atenuó y las reservas del RE se conservaron mejor. En conjunto, estos hallazgos revelan a las A2-pancortinas como organizadoras de una “autopista” de calcio que se vuelve letal bajo estrés isquémico.
Qué significa esto para proteger los cerebros neonatales
Para el público general, la conclusión es que este trabajo identifica un nuevo interruptor molecular que contribuye a decidir si las neuronas jóvenes viven o mueren tras un ictus. Al apretar las uniones microscópicas entre las membranas que almacenan calcio y las centrales energéticas celulares, las A2-pancortinas provocan que las mitocondrias se asfixien por el exceso de calcio y fallen. Eliminar estas proteínas en ratones jóvenes suaviza el impacto del ictus experimental, lo que sugiere que fármacos o terapias génicas dirigidas a interrumpir los complejos A2-pancortina —o a aflojar los sitios de contacto que refuerzan— podrían algún día reducir la lesión cerebral en recién nacidos afectados. Aunque tales tratamientos sigan siendo prospectos futuros, el estudio traza una vía clara y comprobable desde proteínas del desarrollo hasta la sobrecarga de calcio y la pérdida neuronal en el ictus neonatal.
Cita: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Palabras clave: ictus neonatal, sitios de contacto mitocondria-RE, sobrecarga de calcio, proteínas pancortina, muerte neuronal