Clear Sky Science · es
Un nuevo eje regulador C/EBPα–miR-335-5p–PRKAA2 impulsa la acumulación de lípidos hepáticos en MASLD
Por qué importa la enfermedad del hígado graso
Mucha gente que prácticamente no bebe alcohol desarrolla aun así un «hígado graso», una condición actualmente denominada enfermedad hepática esteatótica asociada a la disfunción metabólica (MASLD). Está estrechamente vinculada con la obesidad y la diabetes tipo 2 y puede progresar silenciosamente hacia la cicatrización hepática, la cirrosis e incluso el cáncer de hígado. Este estudio plantea una pregunta simple pero crucial: ¿qué sucede dentro de las células hepáticas que las hace almacenar tanto grasa, y podemos encontrar un interruptor molecular que pueda apagarse para proteger el hígado?
Una reacción en cadena oculta en las células hepáticas
Los investigadores se centraron en una reacción en cadena molecular que conecta la dieta y el metabolismo con la acumulación de grasa en el hígado. Estudiaron ratones alimentados con una dieta alta en grasas y células hepáticas en cultivo expuestas a ácidos grasos para imitar la MASLD. En estos modelos, los animales aumentaron de peso, sus lípidos en sangre se elevaron y sus hígados se llenaron de gotículas oleosas, reproduciendo rasgos clave del hígado graso humano. Dentro de estos hígados esteatósicos, el equipo observó que un regulador genético particular, un factor de transcripción llamado C/EBPα, y una pequeña molécula de ARN, miR‑335‑5p, estaban ambos aumentados, mientras que una subunidad de enzima protectora denominada PRKAA2, parte del conocido sensor de energía AMPK, estaba reducida.
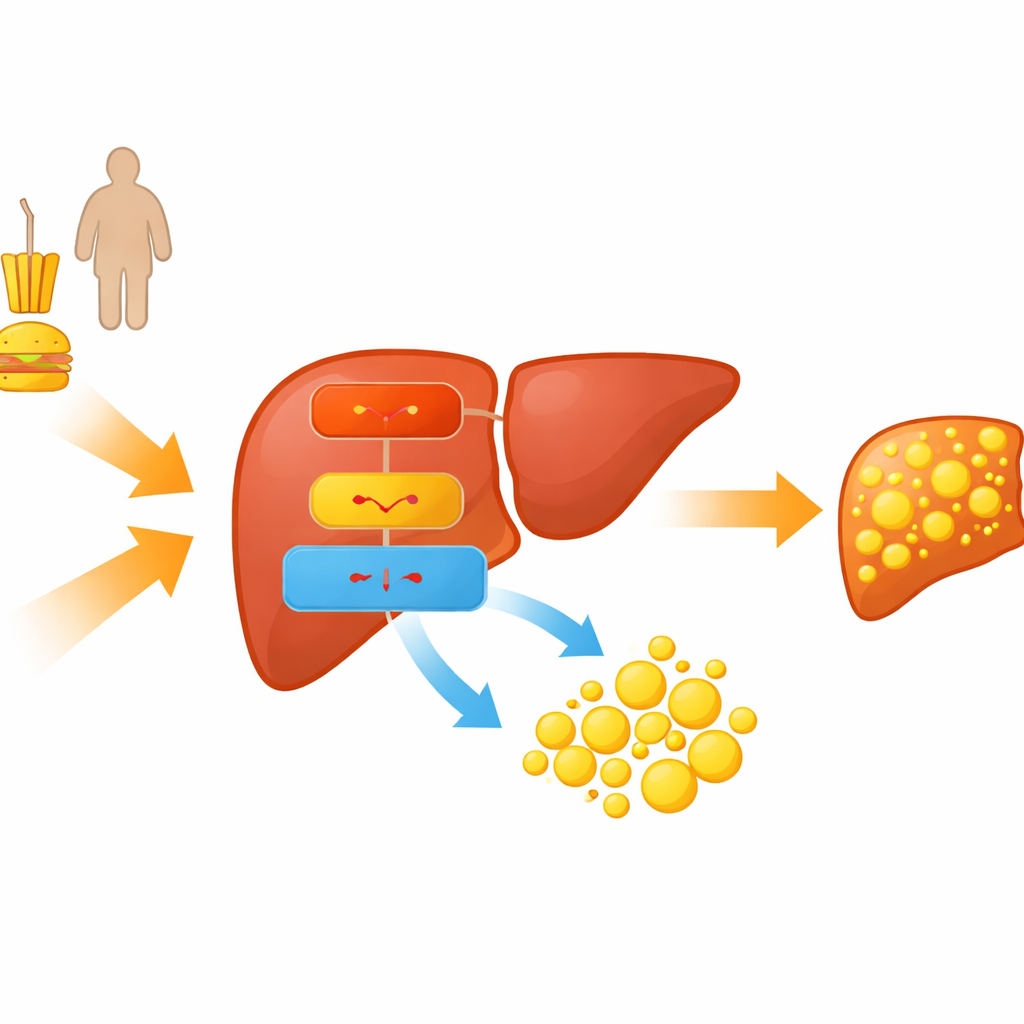
Cómo un pequeño ARN inclina la balanza hacia la grasa
Las pequeñas moléculas de ARN llamadas microARN actúan como atenuadores moleculares, reprimiendo genes específicos. El equipo demostró que miR‑335‑5p se une directamente al mensajero que codifica PRKAA2 e impide que las células produzcan esta proteína. PRKAA2 ayuda a ensamblar el complejo AMPK, que normalmente detecta bajo nivel energético y responde frenando la producción de grasa y fomentando su quema. Cuando los niveles de miR‑335‑5p se elevaron artificialmente en células hepáticas, los niveles de PRKAA2 cayeron, la actividad de AMPK disminuyó y las proteínas que construyen grasa aumentaron, conduciendo a cúmulos visibles de gotículas lipídicas. Cuando se bloqueó miR‑335‑5p, ocurrió lo contrario: PRKAA2 y la actividad de AMPK aumentaron y la acumulación de grasa disminuyó.
El interruptor maestro que inicia la cascada
¿Qué enciende miR‑335‑5p en primer lugar? Al escanear la secuencia de ADN que controla este microARN, los científicos predijeron varios posibles interruptores maestros y se centraron en C/EBPα, ya conocido por influir en el manejo de grasas y azúcares. Confirmaron que C/EBPα se une directamente a la región de control de miR‑335‑5p y aumenta su actividad. Incrementar C/EBPα en células hepáticas elevó los niveles de miR‑335‑5p, redujo PRKAA2, debilitó la señalización de AMPK y favoreció la acumulación de grasa. Silenciar C/EBPα tuvo el efecto inverso, reforzando el freno sensor de energía de la célula y reduciendo los lípidos. Experimentos de rescate, en los que se bloqueó miR‑335‑5p o se restauró PRKAA2, mostraron que gran parte del efecto promotor de grasa de C/EBPα fluye a través de esta única cadena.
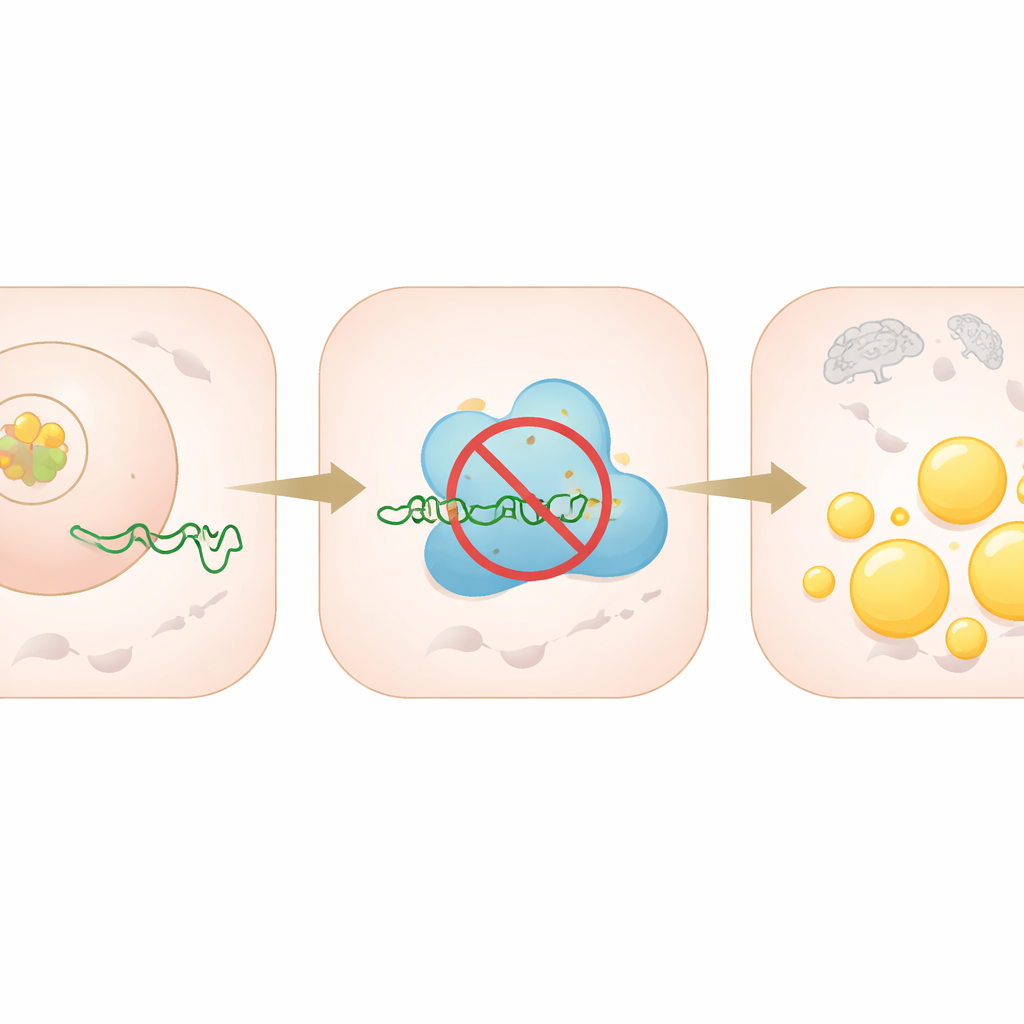
De platos de cultivo a ratones vivos
Para comprobar si esta vía importa en animales vivos, los investigadores usaron virus modificados para entregar herramientas genéticas directamente a los hígados de ratones alimentados con dieta alta en grasas. Una herramienta redujo los niveles de C/EBPα; otra eliminó el exceso de miR‑335‑5p. En ambos casos, los hígados de los animales contenían menos grasa, su apariencia microscópica mejoró y PRKAA2 y la actividad de AMPK se recuperaron, mientras que las proteínas que impulsan la síntesis de grasa disminuyeron. Estos resultados in vivo concordaron con los hallazgos en cultivos celulares y subrayaron que la cadena C/EBPα–miR‑335‑5p–PRKAA2 no es solo una curiosidad de laboratorio, sino un potente impulsor del hígado graso en un organismo vivo.
Qué significa esto para tratamientos futuros
En términos sencillos, el estudio revela un relevo molecular de tres pasos que hace que las células hepáticas acaparen grasa: C/EBPα activa miR‑335‑5p, que a su vez apaga PRKAA2 y debilita AMPK, el freno energético de la célula. Con ese freno desactivado, la maquinaria de construcción de grasa funciona sin control y el hígado se llena de lípidos. Interrumpir cualquiera de los eslabones de este relevo —atenuar C/EBPα, bloquear miR‑335‑5p o potenciar PRKAA2/AMPK— redujo la grasa en los hígados de los ratones. Aunque queda mucho trabajo antes de que tales estrategias puedan usarse de forma segura en personas, esta vía ofrece un objetivo claro y comprobable para fármacos futuros destinados a frenar o revertir la MASLD.
Cita: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
Palabras clave: enfermedad del hígado graso, microARN, AMPK, metabolismo de lípidos, enfermedad metabólica