Clear Sky Science · es
Microbiota intestinal y perfiles de vías metabólicas en pacientes con trasplante de corazón infectados y no infectados antes y después de la cirugía
Por qué importa tu intestino después de recibir un nuevo corazón
El trasplante de corazón puede dar a las personas con insuficiencia cardíaca grave una segunda oportunidad de vida, pero las infecciones en las semanas posteriores a la cirugía siguen siendo una amenaza importante. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿cómo cambia la comunidad microbiana que vive en nuestros intestinos—la microbiota intestinal—alrededor del trasplante de corazón, y pueden esos cambios ayudar a explicar quién desarrolla infecciones y quién no?
El diminuto ecosistema dentro de los pacientes trasplantados
Nuestros intestinos albergan billones de bacterias que ayudan a digerir los alimentos, entrenan el sistema inmunitario y mantienen a raya a los gérmenes invasores. La cirugía, los potentes fármacos inmunosupresores y los antibióticos de amplio espectro pueden alterar este frágil ecosistema. Para seguir lo que ocurre en pacientes con trasplante de corazón, investigadores en China siguieron a 20 adultos que recibieron corazones donados. Recogieron muestras de heces aproximadamente una semana antes de la cirugía y de nuevo 30 días después, y luego usaron secuenciación de ADN para catalogar qué bacterias estaban presentes y herramientas informáticas para predecir qué podrían estar haciendo metabólicamente esos microbios.
Cuatro grupos de pacientes, cuatro patrones microbianos
El equipo dividió a los pacientes en cuatro grupos: con y sin infección antes de la cirugía, y con y sin infección en el primer mes después del procedimiento. Antes del trasplante, la diversidad y la estructura general de la microbiota intestinal parecían sorprendentemente similares tanto si los pacientes ya tenían una infección como si no. Las personas sin infecciones previas a la cirugía estaban mayoritariamente colonizadas por un género conocido llamado Bacteroides, a menudo vinculado con la estabilidad del intestino. En contraste, los pacientes infectados mostraron una mezcla que incluía al potencialmente dañino Enterococcus casseliflavus junto a bacterias consideradas benignas, como Limosilactobacillus y Weissella cibaria, lo que sugiere una comunidad intestinal en un equilibrio frágil y cambiante.
Después de la cirugía: una bifurcación en el camino microbiano
Treinta días después de la operación, la microbiota de los pacientes que evitaron la infección formó un patrón reconocible, mientras que la de quienes desarrollaron infecciones fue muy distinta. Los pacientes no infectados mostraron comunidades microbianas más ricas y uniformes, con muchos miembros de un género llamado Blautia y bacterias relacionadas que producen butirato, un ácido graso de cadena corta conocido por nutrir las células intestinales y apoyar la estabilidad inmunitaria. Sus ecosistemas intestinales parecían diversos y equilibrados. En los pacientes que sufrieron infecciones, en cambio, la diversidad disminuyó y la comunidad estuvo dominada por Enterococcus faecium, una bacteria resistente frecuentemente asociada a infecciones hospitalarias y conocida por su resistencia a antibióticos. Los análisis estadísticos mostraron que los microbios del grupo infectado se agruparon por separado del resto, señalando un caso claro de alteración microbiana posquirúrgica, o disbiosis.
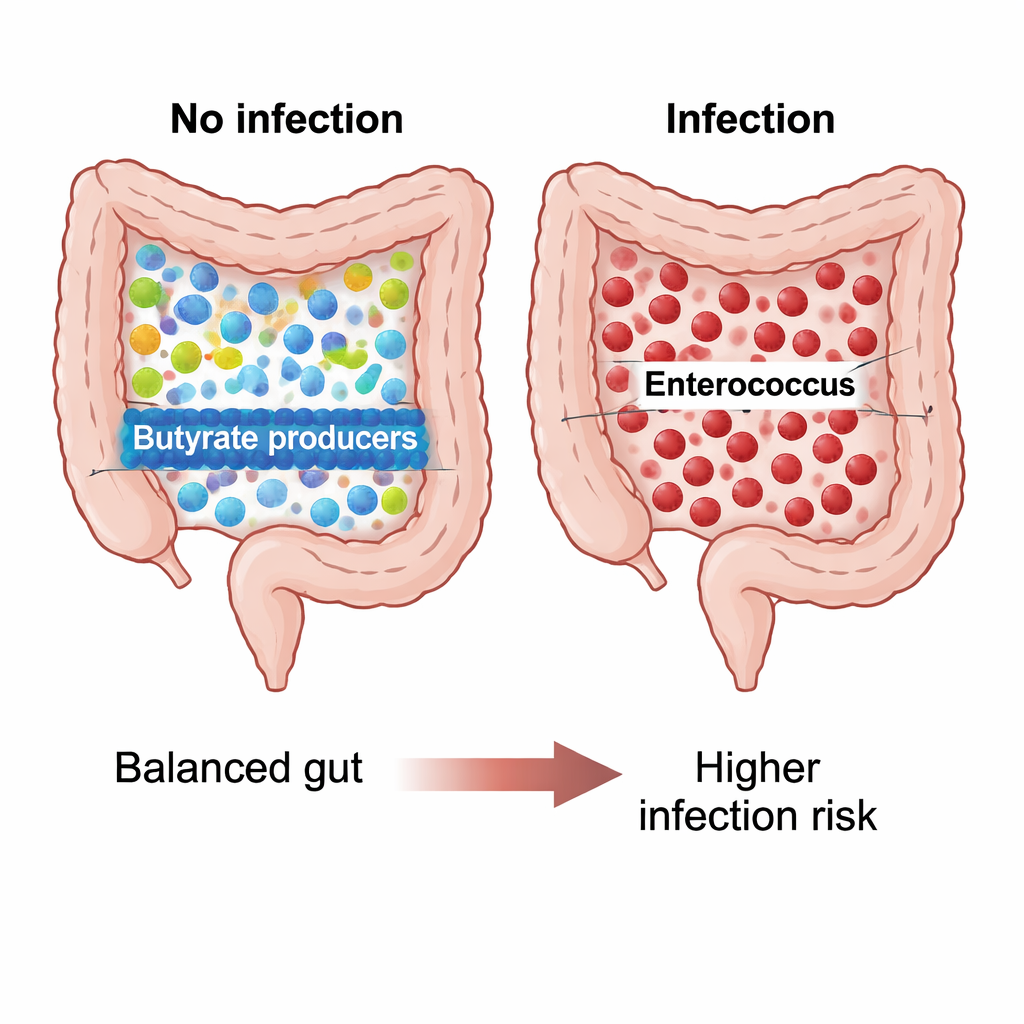
Química microbiana vinculada a protección o riesgo
Los investigadores también preguntaron qué tipos de funciones químicas podrían realizar estos microbios. Usando software predictivo, hallaron que en el grupo posoperatorio no infectado, Blautia se asoció a vías que descomponen un compuesto llamado L-1,2-propanodiol, un intermedio en la fermentación de fibra que finalmente alimenta la producción de ácidos grasos beneficiosos como el propionato. En los pacientes infectados, este potencial metabólico predicho fue marcadamente menor, coherente con una comunidad intestinal menos capaz de producir moléculas protectoras. Antes de la cirugía, Enterococcus casseliflavus en pacientes infectados se relacionó con rutas de fermentación inusuales que pueden reflejar un entorno microbiano estresado y con alta demanda energética, aunque esto requiere confirmación directa en laboratorio.
Qué significa esto para pacientes y equipos de cuidados
Para las personas que afrontan un trasplante de corazón, estos hallazgos sugieren que el intestino no es solo un espectador; puede ayudar a moldear el riesgo de infecciones peligrosas. El estudio apunta a un cambio dinámico desde el predominio de Bacteroides antes de la cirugía hacia una enriquecimiento protector por Blautia o una sobrecrecimiento perjudicial de Enterococcus después, dependiendo de cómo transcurra el periodo temprano de recuperación. El estrés relacionado con la infección y el uso intensivo de antibióticos parecen empujar la comunidad intestinal hacia el estado de baja diversidad dominado por Enterococcus observado en los pacientes infectados. Los autores proponen una estrategia de “doble objetivo”: favorecer la recuperación de bacterias productoras de butirato—quizá mediante la dieta o probióticos seleccionados con cuidado—mientras se monitorizan de cerca los niveles de Enterococcus. Aunque hacen falta estudios más amplios y prolongados, este trabajo abre la puerta a un cuidado de trasplantes futuro en el que ajustar la microbiota intestinal sea parte habitual de la protección de los pacientes contra infecciones potencialmente mortales.
Cita: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Palabras clave: trasplante de corazón, microbiota intestinal, infección postoperatoria, antibióticos, bacterias productoras de butirato