Clear Sky Science · es
Expresión alterada del eje CD26/ADA en la inflamación mediada por el sistema inmune en la mononucleosis infecciosa
Por qué importa este virus infantil
Muchos padres conocen la mononucleosis infecciosa, a menudo llamada “mono”, como una enfermedad mala pero por lo general temporal, caracterizada por fiebre, dolor de garganta y ganglios inflamados. Sin embargo, en un pequeño número de niños la infección puede volverse grave y dañar órganos como el hígado. Este estudio examina en detalle cómo reaccionan los sistemas inmunitarios de los niños ante el virus de Epstein–Barr, la causa principal de la mono, y se centra en una pareja de diminutos colaboradores en la superficie celular—CD26 y una enzima llamada ADA—que podrían ayudar a explicar por qué algunas respuestas inmunitarias se vuelven peligrosamente intensas.
Los defensores del cuerpo en sobreactivación
Cuando el virus de Epstein–Barr entra en el organismo, infecta principalmente ciertos glóbulos blancos y desencadena una reacción inmune fuerte. En este estudio, los médicos compararon sangre de 30 niños con mono aguda con la de 30 niños sanos. Encontraron que los niños enfermos tenían muchas más células blancas en general, especialmente un subconjunto llamado células T CD8 que se especializan en matar células infectadas. Al mismo tiempo, otro grupo importante de células helpers, las T CD4, estaba relativamente reducido, de modo que el equilibrio habitual entre células de “ataque” y de “apoyo” se invirtió. Los niveles de proteínas que combaten la infección en la sangre, incluidos varios mensajeros que aumentan o disminuyen la inflamación, también fueron más altos, lo que muestra que el sistema inmune estaba completamente activado.
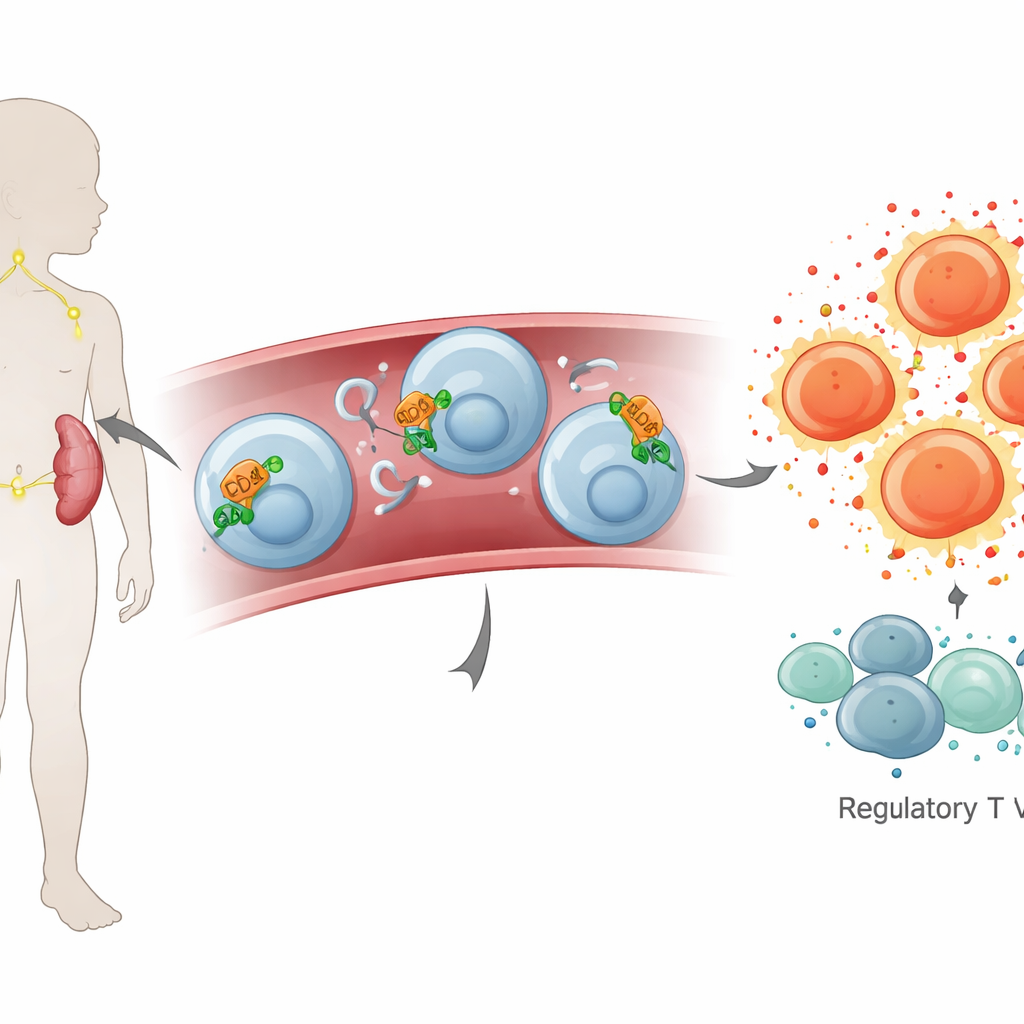
Una mirada cercana a un diminuto interruptor de control
Los investigadores se centraron entonces en CD26 y ADA, dos moléculas que se sitúan en la encrucijada entre la activación celular y la señalización química fuera de las células. Mediante pruebas genéticas en las células sanguíneas, hallaron que los niños con mono mostraban niveles más altos de instrucciones para CD26 y ADA (ARNm), lo que sugiere que las células inmunitarias se estaban preparando para producir más de estas proteínas. Los análisis de sangre confirmaron que la actividad de ADA en sí misma era mayor. Curiosamente, la cantidad circulante de proteína CD26 en el plasma no difería mucho entre niños enfermos y sanos, lo que insinúa que en la mono esta molécula puede permanecer principalmente unida a las superficies celulares en lugar de flotar libremente.
Desplazamiento del equilibrio entre ataque y contención
Para entender cómo funcionaba este interruptor en distintos tipos de células inmunitarias, el equipo utilizó citometría de flujo, un método que cuenta y caracteriza las células una por una. En las células T CD8, las que se expanden de forma dramática durante la mono, CD26 era más frecuente, tanto si las células portaban como si no otro marcador llamado CD39, vinculado a un potente sistema químico de freno. Este patrón sugiere que en estas células “asesinas”, CD26 podría ayudar a superar señales químicas locales que normalmente amortiguarían su actividad, apoyando un ataque enérgico contra las células infectadas por el virus. Al mismo tiempo, entre las células T CD4 que habitualmente ayudan a coordinar las respuestas inmunitarias, el panorama fue más mixto. Las células que expresaban tanto CD4 como CD39—con frecuencia asociadas a roles reguladores y calmantes—eran relativamente más frecuentes, lo que puede ayudar a explicar los altos niveles de señales calmantes como la citocina IL-10.
Cuando la regulación se debilita
No obstante, dentro de la población de CD4 que carece de CD39 y que suele estar compuesta por células helpers activas, la fracción de células que mostraban CD26 fue en realidad menor en los niños con mono que en los compañeros sanos. Esta pérdida de CD26 en las células helpers puede reducir su capacidad de proliferar y coordinar respuestas equilibradas, incluso cuando las células CD8 se ven empujadas hacia una mayor actividad. El estudio también mostró que la cantidad de CD26 en plasma se correlacionaba con los niveles de ADA y con el interferón-gamma, una señal inflamatoria potente, y se relacionaba inversamente con la proporción de células T CD4 y con la relación CD4/CD8. En conjunto, estos patrones señalan al “eje” CD26/ADA como estrechamente vinculado a la intensidad con que responde el sistema inmune durante la infección.
Qué significa para los niños enfermos
Para las familias y los clínicos, estos hallazgos ofrecen una imagen más clara de por qué un virus común puede a veces conducir a una enfermedad preocupante. En la mono aguda, los sistemas inmunitarios de los niños parecen apoyarse fuertemente en células T CD8 armadas con actividad adicional del eje CD26–ADA, impulsando una respuesta antiviral intensa que corre el riesgo de excederse y dañar tejidos. Al mismo tiempo, ciertas células helpers y regulatorias pierden o reconfiguran sus patrones de CD26, debilitando potencialmente los frenos que normalmente mantienen la inflamación bajo control. Aunque se necesita más trabajo—especialmente en casos muy graves—este estudio sugiere que medir y, eventualmente, modular el eje CD26/ADA podría algún día ayudar a los médicos a valorar la gravedad de la enfermedad o a diseñar tratamientos que calmen los fuegos inmunitarios dañinos sin apagar por completo las defensas del cuerpo.
Cita: Shi, T., Shi, W., Tian, J. et al. Altered expression of the CD26/ADA axis in immune-mediated inflammation of infectious mononucleosis. Sci Rep 16, 9316 (2026). https://doi.org/10.1038/s41598-026-38891-z
Palabras clave: mononucleosis infecciosa, virus de Epstein-Barr, células T, regulación inmune, vía de la adenosina