Clear Sky Science · es
Evaluando la relación evolutiva de la proteína vinculante a la caja TATA (TBP) con diversos patrones de plegamiento de dominios proteicos usando máquinas de vectores de soporte (SVM)
Cómo una proteína «interruptor» del ADN se conecta con muchas otras
La proteína vinculante a la caja TATA, o TBP, es un pilar del funcionamiento celular: ayuda a activar genes al sujetar el ADN en numerosos promotores. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿existen otras proteínas, con funciones muy distintas, que compartan silenciosamente la forma subyacente de la TBP? Combinando comparación de estructuras 3D, análisis de secuencias y herramientas modernas de aprendizaje automático, los autores trazan vínculos familiares ocultos entre la TBP y proteínas implicadas en el metabolismo, la química de los neurotransmisores e incluso vías relacionadas con el cáncer.
Una proteína clave en el control génico
La TBP se sitúa en la puerta de entrada de la expresión génica en organismos que van desde la levadura hasta los humanos. Reconoce una corta secuencia de ADN llamada caja TATA y dobla el ADN para ayudar a ensamblar la gran maquinaria de transcripción que copia genes en ARN. Dado que este paso es tan central, el plegamiento —la disposición tridimensional— del núcleo de la TBP está altamente conservado a lo largo de la evolución. Los autores se centran en una estructura de TBP bien estudiada conocida como 1tba y la usan como sonda para buscar otras proteínas que puedan compartir su plano arquitectónico, incluso si sus secuencias de aminoácidos y tareas habituales parecen muy diferentes a primera vista.
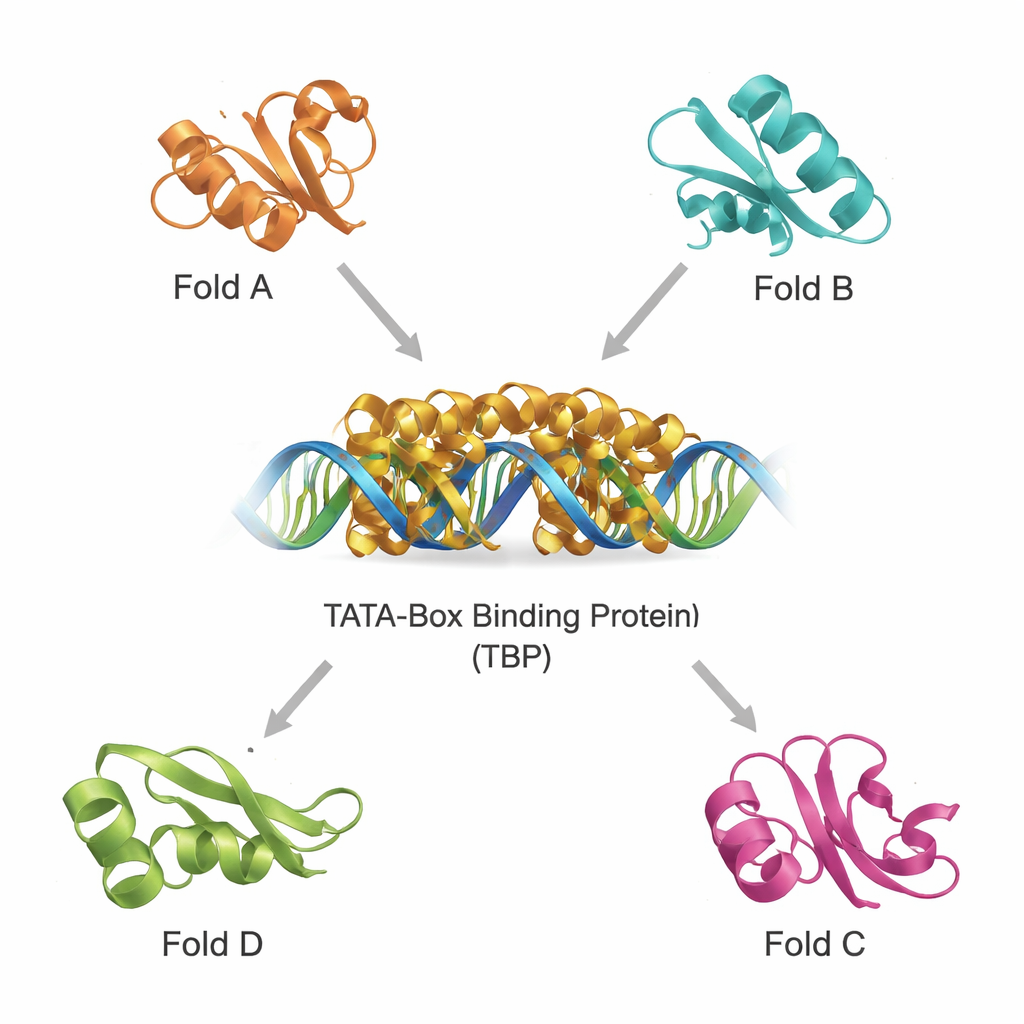
Encontrando primos estructurales en un universo proteico abarrotado
Las bases de datos modernas contienen cientos de miles de estructuras proteicas, lo que permite rastrear parientes lejanos por forma 3D en lugar de por secuencia. Usando dos herramientas poderosas, DALI y TOP‑search, el equipo extrajo primero proteínas cuyos plegamientos se parecían al de la TBP. Luego clasificaron estos candidatos con un catálogo evolutivo de dominios y los redujeron a un pequeño conjunto de ejemplos estructuralmente similares pero funcionalmente diversos. Entre ellos figuran una enzima que sintetiza glutamina importante en el metabolismo, un dominio presente en varias enzimas que manejan ARN de transferencia (tRNA), una enzima con un característico plegamiento tipo “hot‑dog” implicada en la química de ácidos grasos, y proteínas que ayudan a producir tetrahidrobiopterina, una molécula crucial para la función cerebral. Superponer sus estructuras sobre la TBP mostró que, pese a sus distintos roles, comparten motivos centrales reconocibles.
Enseñar a las máquinas a reconocer familias proteicas ocultas
Para ir más allá de la inspección caso por caso, los autores construyeron modelos de aprendizaje automático que pudieran señalar automáticamente plegamientos tipo TBP. Reunieron grandes conjuntos de secuencias proteicas conocidas por pertenecer a la TBP o a cada uno de los plegamientos relacionados, junto con un amplio conjunto de “fondo” de proteínas no relacionadas. Cada proteína se convirtió en resúmenes numéricos simples: la frecuencia de aparición de cada aminoácido y la frecuencia de cada par posible de aminoácidos en la secuencia. Estos perfiles alimentaron máquinas de vectores de soporte (SVM) y modelos de bosques aleatorios, que aprendieron a separar un tipo de plegamiento de todos los demás. Usando validación cruzada rigurosa, los modelos alcanzaron una precisión muy alta—frecuentemente por encima del 95 por ciento—incluso cuando se entrenaron solo con partes de las secuencias correspondientes a regiones conservadas.
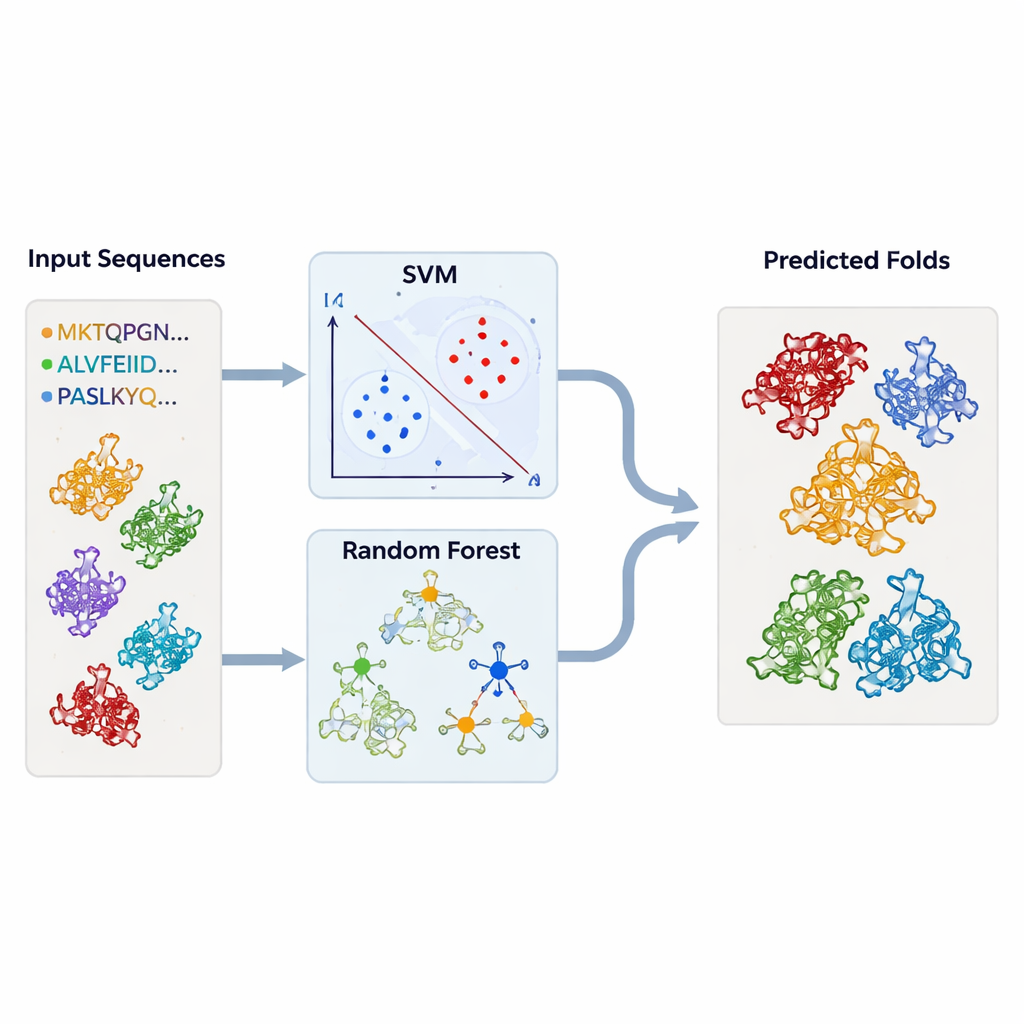
Probar los modelos en miles de estructuras desconocidas
Armado con estos clasificadores entrenados, el equipo regresó a las bases de datos estructurales. Ejecutaron miles de cadenas proteicas—recuperadas de DALI y TOP‑search—a través de sus modelos para ver cuáles presentaban las señales estadísticas de plegamientos tipo TBP o relacionados. Los enfoques SVM y de bosque aleatorio coincidieron en gran medida y seleccionaron muchos candidatos que las herramientas estructurales también habían marcado como similares. En algunos casos, enzimas con actividades aparentemente no relacionadas se agruparon con fuerza junto a la TBP o entre sí, reforzando la idea de que la evolución puede reutilizar el mismo marco subyacente para múltiples roles bioquímicos distintos.
Por qué importan estas conexiones ocultas
El estudio concluye que la TBP comparte una profunda ascendencia estructural con varias familias de enzimas, incluidas proteínas similares a la glutamina sintetasa y dominios de edición de enzimas procesadoras de tRNA. Incluso cuando las secuencias han cambiado y las funciones se han diversificado, estas proteínas conservan motivos arquitectónicos comunes, lo que sugiere descendencia de un ancestro compartido. Para un lector no especialista, el mensaje clave es que la naturaleza tiende a reciclar diseños exitosos: un plegamiento puede adaptarse repetidamente para resolver problemas muy diferentes, desde activar genes hasta ajustar el metabolismo y la química cerebral. Al combinar la comparación de estructuras 3D con aprendizaje automático, los autores ofrecen una caja de herramientas práctica para descubrir tales relaciones, ayudando a los biólogos a predecir qué pueden hacer proteínas no caracterizadas y orientando a desarrolladores de fármacos hacia nuevos objetivos guiados por la evolución en vías relevantes para la enfermedad.
Cita: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
Palabras clave: proteína vinculante a la caja TATA, evolución de proteínas, aprendizaje automático, estructura de proteínas, máquina de vectores de soporte