Clear Sky Science · es
Estudio piloto aleatorizado de camrelizumab con o sin células asesinas inducidas por citocinas autólogas en carcinoma de células claras refractario de riñón
Nuevas esperanzas para un cáncer de riñón de difícil tratamiento
Para las personas con cáncer de riñón avanzado que ha dejado de responder a los fármacos estándar, las opciones de tratamiento son limitadas y alarmantemente escasas. Este estudio explora una forma prometedora de potenciar las defensas del propio cuerpo al combinar un fármaco inmunoterapéutico moderno con una infusión personalizada de células inmunitarias activadas, ofreciendo un indicio de cómo podría ser la atención futura para estos pacientes.
Por qué este cáncer es tan difícil
El carcinoma renal de células claras es el tipo más común de cáncer de riñón. Muchos pacientes ahora viven más tiempo gracias a fármacos que cortan el suministro de sangre al tumor y a los inhibidores de puntos de control inmunitarios que ayudan al sistema inmunitario a reconocer el cáncer. Sin embargo, algunos tumores finalmente encuentran formas de eludir estos tratamientos y seguir creciendo. En esa fase, los médicos necesitan con urgencia opciones que puedan estimular aún más al sistema inmunitario, sin provocar efectos secundarios inaceptables.
Usar las propias células del paciente como refuerzo
En este ensayo, los investigadores probaron si combinar el fármaco de punto de control camrelizumab con las propias células “entrenadas” del paciente podría mejorar los resultados. El camrelizumab actúa bloqueando un freno molecular llamado PD‑1, que los tumores usan para desactivar a las células T atacantes. El tratamiento añadido, denominado terapia con células asesinas inducidas por citocinas (CIK), se fabrica recogiendo la sangre del paciente, cultivando y activando ciertos glóbulos blancos en el laboratorio y luego reinfundiendo estas células energizadas en el torrente sanguíneo. La idea es que camrelizumab suelte los frenos mientras las células CIK actúan como tropas frescas, penetrando en el tumor y ayudando a convertir un ambiente “frío” y supresor en uno “caliente” y listo para atacar. 
Qué encontró el pequeño ensayo
El estudio reclutó a 21 personas con carcinoma renal de células claras avanzado cuya enfermedad había empeorado a pesar de tratamientos previos. Los pacientes se asignaron al azar para recibir camrelizumab solo o camrelizumab más infusiones repetidas de células CIK. Debido a que el estudio se detuvo antes de tiempo —solo se pudo inscribir a aproximadamente un tercio de los participantes planeados—, sus resultados se consideran exploratorios más que definitivos. Aun así, las cifras fueron alentadoras: más de la mitad de los pacientes que recibieron la combinación vieron disminuir sus tumores de forma significativa, frente a alrededor de cuatro de cada diez en el grupo que recibió solo el fármaco. Un hombre del grupo de combinación presentó desaparición de todas las señales de cáncer activo en exploraciones especializadas y se mantuvo con vida y con buena calidad de vida mucho después de que su tratamiento tuviera que suspenderse por una inflamación pulmonar.
Señales de un control más prolongado, con matices
Cuando los investigadores examinaron cuánto tiempo permaneció controlado el cáncer y cuánto vivieron los pacientes, quienes recibieron camrelizumab y células CIK parecieron hacerlo mejor. De media, las personas del grupo combinado pasaron más de dos años antes de que su enfermedad empeorara de forma evidente, frente a menos de un año para quienes recibieron solo camrelizumab. La supervivencia global también pareció algo mejor en el grupo combinado, pero el estudio fue demasiado pequeño para afirmar con certeza que estas diferencias no se debieran al azar. Los efectos secundarios observados —como pequeños crecimientos de vasos sanguíneos en la piel, alteraciones tiroideas, fatiga e inflamación pulmonar rara— fueron en su mayoría leves a moderados y coherentes con lo que ya se conoce sobre camrelizumab; añadir células CIK no aumentó de forma notable los riesgos del tratamiento. 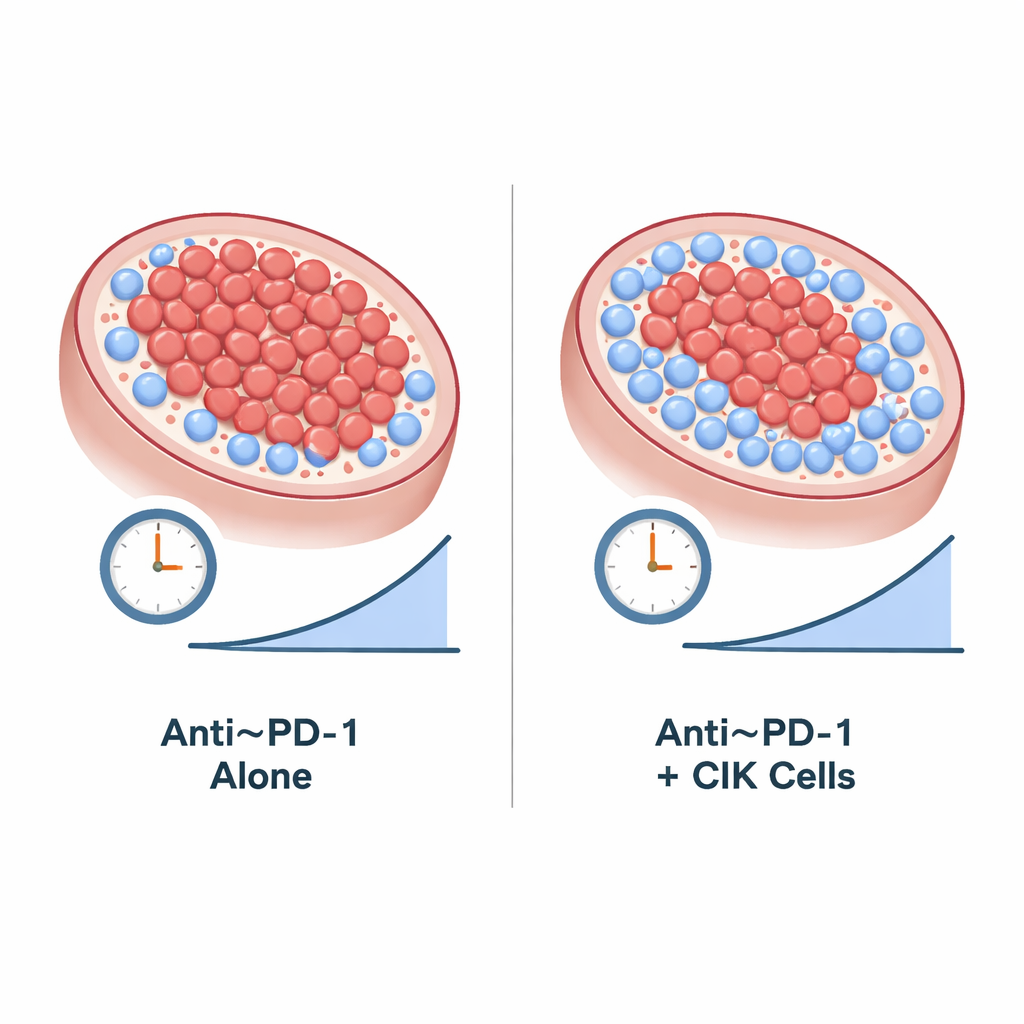
Pistas desde el sistema inmunitario
El equipo también tomó muestras de sangre de algunos pacientes para buscar señales tempranas de quién podría beneficiarse más de este enfoque. Se centraron en las células T CD8, una clase clave de células inmunitarias “asesinas”, y midieron cuántas mostraban el marcador PD‑1 antes del tratamiento. Los pacientes cuyas células asesinas comenzaron con niveles más altos de PD‑1 tendieron a responder mejor, y la proporción de células PD‑1 positivas generalmente disminuyó tras el inicio de la terapia —patrones que pueden reflejar la reactivación de células inmunitarias agotadas. Dado que solo se analizaron un número reducido de pacientes, estas pistas deben confirmarse en estudios más amplios y detallados.
Qué significa esto para los pacientes
Por ahora, este enfoque combinado debe considerarse una estrategia experimental más que un nuevo estándar de atención. El ensayo fue demasiado pequeño para demostrar que añadir células CIK al camrelizumab prolonga realmente la vida, y los tratamientos de primera línea actuales para el cáncer de riñón ya combinan fármacos inmunitarios con pastillas que atacan los vasos sanguíneos. Aun así, el estudio muestra que recolectar, expandir y reinfundir las propias células inmunitarias de los pacientes junto con un inhibidor de puntos de control es factible, parece seguro y puede ofrecer un beneficio adicional para quienes su enfermedad ha resistido otras opciones. Harán falta ensayos más grandes y cuidadosamente diseñados para determinar si esta inmunoterapia de “doble impulso” puede convertirse en un arma fiable contra el cáncer renal avanzado.
Cita: Li, S., Qin, J., Sun, Q. et al. Randomized pilot study of camrelizumab with or without autologous cytokine-induced killer cells in refractory clear cell renal cell carcinoma. Sci Rep 16, 7768 (2026). https://doi.org/10.1038/s41598-026-38881-1
Palabras clave: cáncer de riñón, inmunoterapia, inhibidor de puntos de control, terapia celular, camrelizumab