Clear Sky Science · es
Mediciones de densidad de masa a nivel celular mediante centrifugación en gradiente de microcanal
Por qué importa pesar células diminutas
Cada célula viva es más que una bolsa de moléculas; su peso y compactación cuentan una historia sobre su estado de salud. Cambios sutiles en cuán densamente empaquetada está una célula pueden indicar si está creciendo, muriendo, combatiendo una infección o volviéndose cancerosa. Sin embargo, a pesar de este potencial, medir la densidad de masa de miles de células individuales ha seguido siendo lento, técnicamente exigente y costoso. Este artículo presenta una forma nueva y mucho más simple de “pesar” células individuales según cómo flotan o se hunden en un líquido controlado dentro de un canal de vidrio del grosor de un cabello girado en una centrífuga.
Una nueva vuelta a un truco antiguo de laboratorio
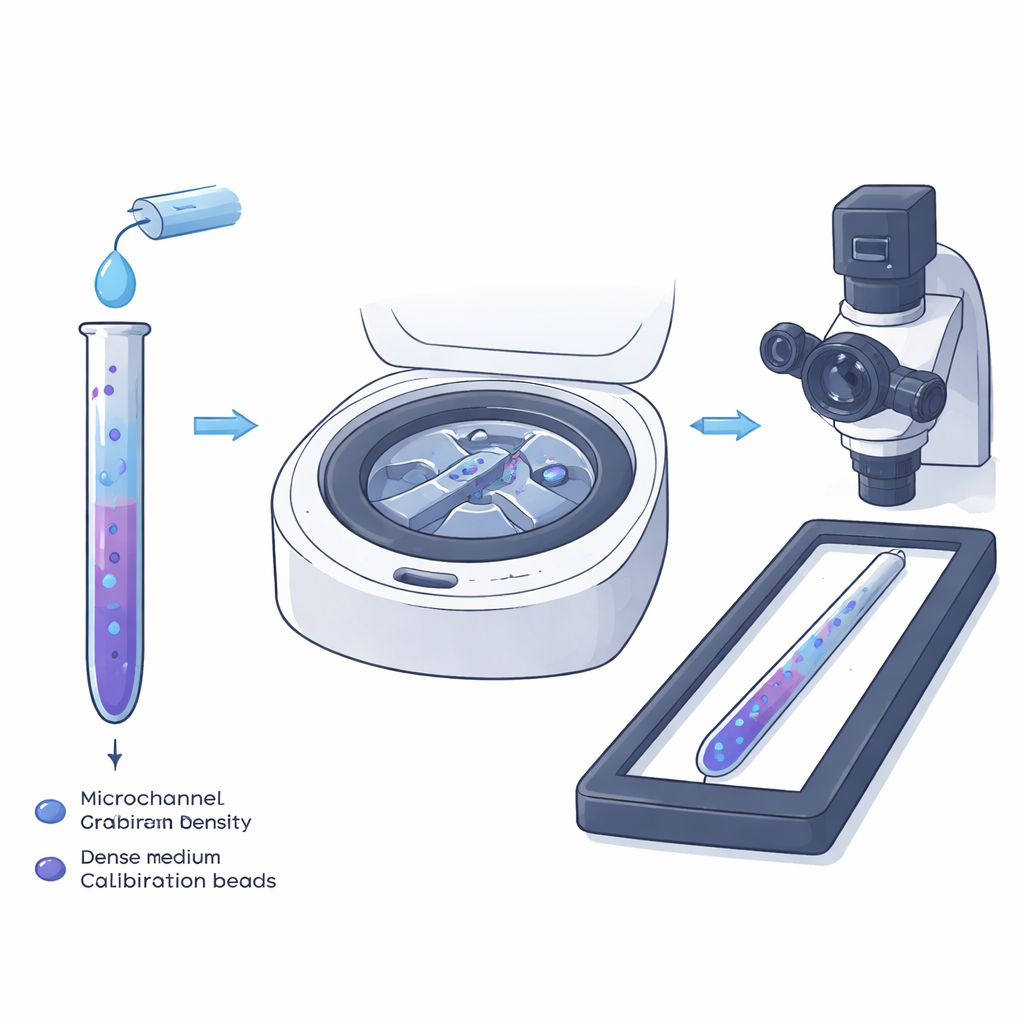
La centrifugación en gradiente de densidad tradicional se ha usado durante mucho tiempo en tubos de ensayo para separar mezclas de células: al girar, las células se sitúan en el punto del líquido estratificado donde su propia densidad coincide con la del fluido circundante. Los autores miniaturizan esta idea en un microcanal estrecho para que se puedan medir directamente bajo un microscopio células individuales, no solo capas. Primero llenan el canal con un líquido ligero que contiene las células y luego con un líquido más pesado que contiene pequeñas partículas de plástico cuyas densidades se conocen con precisión. Cuando estos dos líquidos se encuentran y fluyen en el diminuto canal, forman de manera natural un gradiente de densidad suave y unidimensional a lo largo de su longitud.
Crear una pendiente suave de densidad
Dentro de canales tan finos, el fluido se mueve lenta y suavemente, sin turbulencias. En estas condiciones, el perfil parabólico de flujo mezcla los líquidos ligero y pesado lo justo para crear una transición gradual, en lugar de un límite abrupto, entre ellos. El equipo estudió este proceso tanto experimentalmente, usando un tinte fluorescente, como mediante simulaciones por ordenador. Encontraron que puede formarse en segundos un gradiente de densidad casi lineal que se extiende varios milímetros. La altura del canal resultó crucial: canales poco profundos mantienen el gradiente estable y evitan el vaivén impulsado por la gravedad del líquido más pesado, que difuminaría la relación entre posición y densidad e introduciría errores en las mediciones finales de las células.
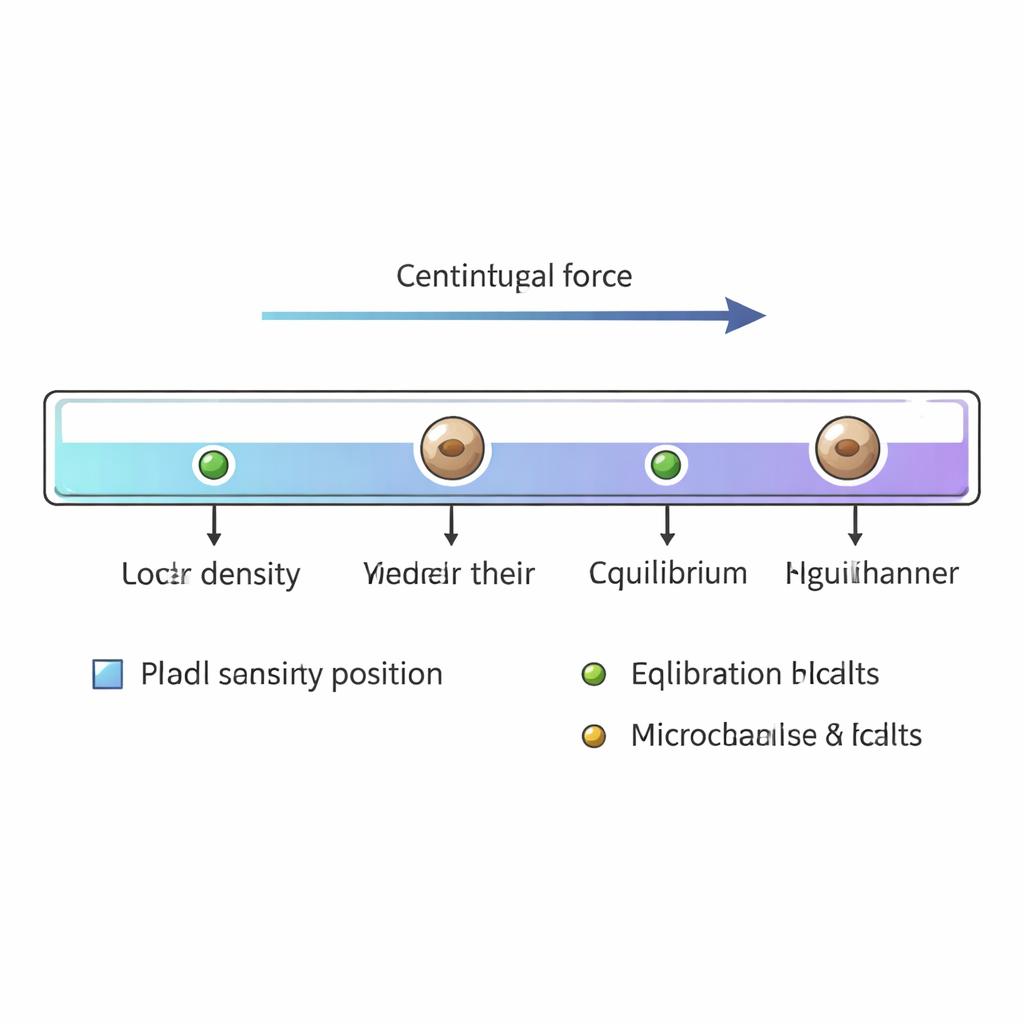
Hacer girar las células hasta su punto de equilibrio
Una vez llenado el canal, se sellan sus extremos y se coloca en una pequeña centrífuga. Al girar a unas 12.000 revoluciones por minuto, las células y las perlas de calibración se desplazan a lo largo del canal hasta que la fuerza hacia fuera debida al giro queda exactamente equilibrada por la flotabilidad correspondiente a su densidad particular. Con diámetros mayores de aproximadamente tres micrómetros, las células de levadura alcanzan este equilibrio en menos de 20 segundos. Tras aproximadamente minuto y medio de centrifugado, se retira el canal y se escanea con un microscopio estándar. Los investigadores registran las posiciones de miles de células de levadura individuales y de las perlas de referencia, y luego convierten cada posición a lo largo del gradiente en un valor de densidad de masa usando las densidades conocidas de las perlas como puntos de anclaje.
Leer la salud celular a partir de pequeñas diferencias
Con este enfoque, los autores midieron las densidades de más de 20.000 células de levadura en múltiples canales. La incertidumbre típica de la medición para una sola célula fue de alrededor de 3,3 kilogramos por metro cúbico, lo bastante pequeña como para resolver diferencias biológicas reales, que en sus muestras fueron aproximadamente el doble. A lo largo de varias horas, observaron que la población principal de levaduras mantenía una densidad estable, mientras que aparecía de forma gradual una segunda población, más densa y ligeramente más pequeña. Este grupo más denso probablemente consistía en células muertas o dañadas que habían absorbido el fluido más pesado, volviéndolas más compactas. Los valores medidos concordaron bien con resultados obtenidos por técnicas mucho más complejas y lentas, como resonadores de microcanal suspendido, métodos ópticos y levitación magnética.
De prototipo de laboratorio a biomarcador práctico
El estudio muestra que una simple combinación de microcanales de vidrio, centrífugas comerciales y microscopios estándar puede ofrecer mediciones de densidad por célula única de alto rendimiento a velocidades de aproximadamente 16.000 células por hora. Aunque aún no es lo bastante sensible para detectar los cambios más diminutos inducidos por fármacos, ya es lo bastante potente para distinguir distintos tipos celulares o vivas de muertas según su grado de compactación. Al hacer que el “pesaje” preciso de células sea más accesible y asequible, este método de gradiente en microcanal podría ayudar a convertir la densidad de masa celular en un biomarcador de rutina para monitorizar enfermedades, evaluar terapias y explorar cómo las células regulan su composición interna.
Cita: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Palabras clave: densidad de célula individual, microfluidos, centrifugación, levaduras, biomarcadores celulares