Clear Sky Science · es
Bifidobacterium breve promueve el crecimiento y altera los lípidos en Trichomonas vaginalis de forma transitoria mediante la reprogramación transcriptómica
Por qué importan los microbios vaginales diminutos
La vagina humana alberga una comunidad activa de microbios que, en silencio, ayudan a mantener a raya las infecciones. Entre estos habitantes hay bacterias amistosas como Bifidobacterium breve y un parásito indeseado llamado Trichomonas vaginalis, responsable de la infección de transmisión sexual no viral más común del mundo. Este estudio plantea una pregunta sorprendentemente simple pero importante: cuando estos dos microbios se encuentran, ¿las bacterias “buenas” nos protegen o, sin querer, favorecen al parásito?
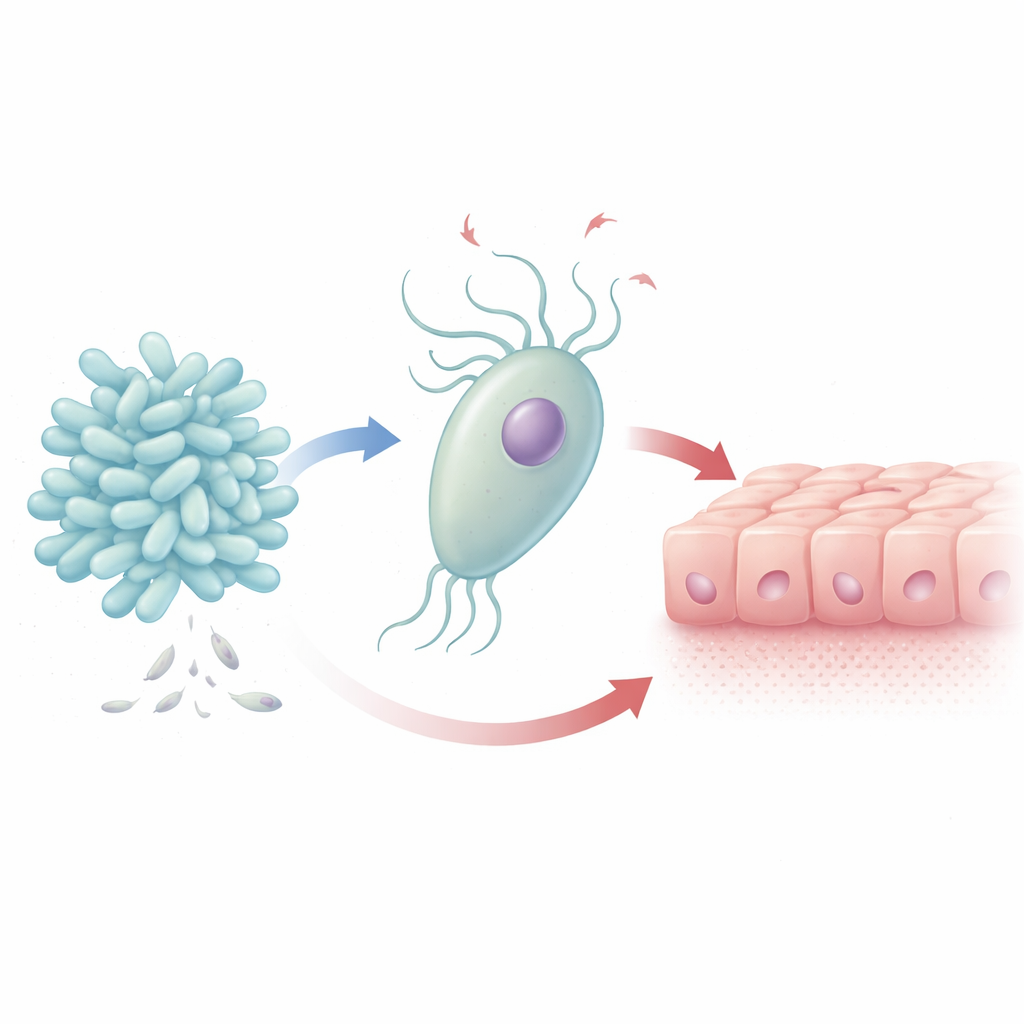
Un equilibrio delicado en el vecindario vaginal
Las mujeres con ecosistemas vaginales saludables suelen tener comunidades dominadas por bacterias protectoras que producen ácido láctico y ayudan a mantener un pH bajo, lo que desalienta a los invasores. B. breve es una de esas especies beneficiosas, mientras que T. vaginalis es un protozoo flagelado vinculado no solo con molestias e inflamación, sino también con mayor riesgo de VIH e infecciones persistentes por el papilomavirus humano. Estudios clínicos han observado que las mujeres infectadas con T. vaginalis suelen tener menos B. breve, lo que sugiere que el sobrecrecimiento del parásito va de la mano con cambios en el equilibrio microbiano normal. Los autores se propusieron entender si B. breve combate al parásito, lo ignora o, de forma inesperada, lo favorece.
Cuando las bacterias “buenas” se encuentran con un parásito
En placas de laboratorio, los investigadores cultivaron B. breve junto con T. vaginalis bajo condiciones anóxicas que imitan el ambiente vaginal. En apenas cuatro horas, el número del parásito aumentó alrededor de un 20 %, mientras que la población bacteriana cayó en más de una cuarta parte. Al microscopio, B. breve se agrupó de forma compacta alrededor de la superficie de T. vaginalis, lo que sugiere contacto físico directo entre ambos. Cuando el parásito expuesto a B. breve se añadió posteriormente a células cervicales humanas (células HeLa), las células hospedadoras no mostraron protección adicional: no hubo reducción en la capacidad del parásito para dañar la capa celular.
Probando la protección del hospedador y la inflamación
El equipo exploró entonces dos escenarios realistas: qué ocurre si B. breve se establece en las células vaginales antes de que llegue el parásito, y qué pasa si ambos llegan a las células al mismo tiempo. En ambos casos, B. breve no consiguió proteger a las células epiteliales del daño causado por T. vaginalis. Las medidas de cobertura y morfología celular permanecieron esencialmente sin cambios tanto si B. breve estaba presente como si no. Al medir señales inflamatorias, especialmente las citocinas IL-6 e IL-8, encontraron que B. breve a veces incluso amplificaba estas respuestas tempranas. En lugar de calmar la inflamación, la exposición simultánea o previa a B. breve tendió a producir picos breves en estas señales, lo que puede ser un arma de doble filo: apoyar la defensa inmune pero también, potencialmente, favorecer la supervivencia del parásito.
Reconfiguración del parásito desde el interior
Para entender cómo cambia el parásito en presencia de B. breve, los investigadores analizaron qué genes se activaban o silenciaban en T. vaginalis y qué ocurría con sus moléculas relacionadas con las grasas. Encontraron que genes implicados en la replicación del ADN, el empaquetamiento de los cromosomas y la generación de energía se activaron, coherente con un crecimiento acelerado del parásito. De forma importante, genes y rutas vinculados al uso de ácidos grasos—especialmente el manejo de grasas de cadena larga y ácidos grasos de cadena corta como el propionato—se activaron con fuerza. Mediciones químicas detalladas revelaron que muchos ácidos grasos dentro del parásito disminuyeron después del cocultivo, lo que sugiere que T. vaginalis estaba consumiendo estas grasas como combustible y material de construcción. En conjunto, los datos apuntan a una breve “reprogramación” metabólica en la que el contacto con B. breve empuja al parásito a consumir más lípidos y a dividirse más rápidamente.
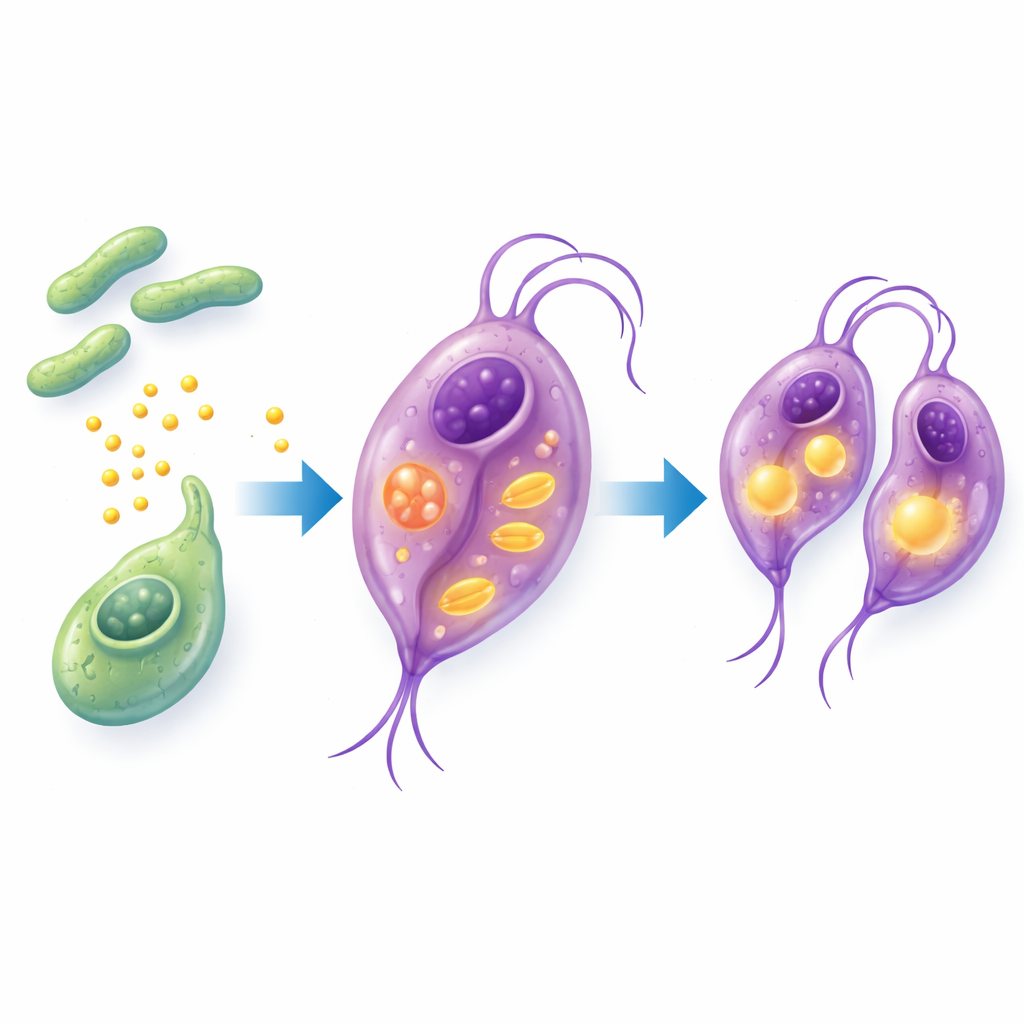
Qué significa esto para la salud vaginal
En términos generales, el estudio muestra que B. breve, a pesar de su reputación como aliado probiótico, no actúa como un guardián simple frente a T. vaginalis. A corto plazo, estas bacterias aparentemente se adhieren al parásito, estimulan su crecimiento y modifican su uso de lípidos, sin proteger directamente a las células humanas del daño. A más largo plazo, B. breve puede seguir contribuyendo al mantenimiento del equilibrio microbiano general, pero no contrarresta directamente a este patógeno en particular. Para pacientes y clínicos, este trabajo subraya que no todas las bacterias “buenas” son protectoras en todo contexto y que la composición y el momento de llegada de los microbios en la vagina pueden indicar cuándo las condiciones favorecen el sobrecrecimiento del parásito, ofreciendo potencialmente nuevos marcadores de alerta temprana o dianas para terapias basadas en el microbioma.
Cita: Chen, PY., Yeh, YM., Chen, CH. et al. Bifidobacterium breve promotes growth and lipid alteration in Trichomonas vaginalis transiently through transcriptomic reprogramming. Sci Rep 16, 8997 (2026). https://doi.org/10.1038/s41598-026-38866-0
Palabras clave: microbioma vaginal, Trichomonas vaginalis, Bifidobacterium breve, metabolismo de ácidos grasos, interacción probiótico–parásito