Clear Sky Science · es
Dinámica conformacional y análisis de energía libre de unión revelan un inhibidor flavonoide estable de la polimerasa NS5 del virus del dengue
Por qué un virus transmitido por mosquitos necesita la ayuda de las plantas
La fiebre del dengue se ha disparado en todo el mundo en los últimos años, enfermando a millones y matando a miles. Aun así, seguimos sin disponer de una pastilla antiviral ampliamente eficaz y asequible para tratar a las personas una vez infectadas. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿pueden los compuestos naturales de las plantas convertirse en precisas "llaves" moleculares que bloqueen una de las máquinas más importantes del virus del dengue?
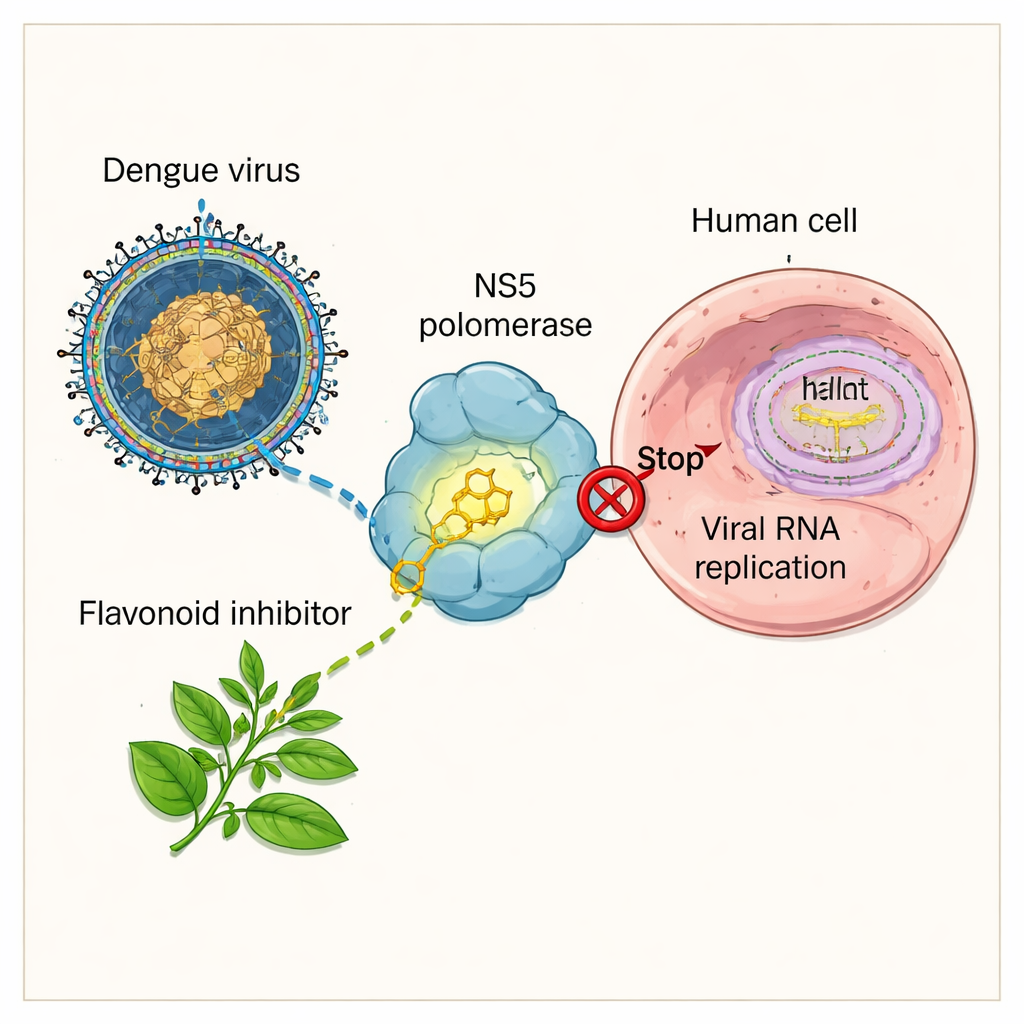
El motor viral que los científicos intentan apagar
El virus del dengue sobrevive copiando su material genético dentro de nuestras células. Para ello depende de una proteína clave llamada NS5, que actúa como un diminuto motor copiador del ARN del virus. Si NS5 deja de funcionar, el virus no puede producir nuevos genomas y la infección se detiene. Por eso los desarrolladores de fármacos consideran a NS5—especialmente su región de copia de ARN, conocida como ARN polimerasa dependiente de ARN—como un objetivo principal para nuevos medicamentos. Varios compuestos sintéticos y extractos vegetales ya han demostrado que NS5 puede ser bloqueada, pero muchos de estos primeros candidatos o bien se unen débilmente, son inestables o plantean dudas sobre seguridad y su comportamiento en el organismo.
Buscar en las plantas agujas químicas prometedoras en un pajar
Los investigadores se centraron en los flavonoides, una gran familia de compuestos vegetales presentes en alimentos como bayas, té y hierbas, conocida desde hace tiempo por sus efectos antivirales y antiinflamatorios. A partir de una base de datos seleccionada de compuestos secundarios vegetales, extrajeron 326 flavonoides y prepararon modelos tridimensionales tanto de la enzima NS5 del virus como de cada molécula candidata. Mediante un acoplamiento computacional escalonado, preguntaron: ¿qué formas encajan mejor en una región específica de "puerta trasera" de NS5 llamada bolsillo N—un sitio alostérico que puede apagar la enzima cuando se ocupa y que tiende a mutar menos que el sitio activo principal?
En cada etapa de este cribado virtual, se descartaron los compuestos que encajaban mal o que parecían poco probables de comportarse como fármacos reales en el cuerpo. Las moléculas que quedaron fueron puntuadas no solo por el ajuste geométrico, sino también por la estimación de la fuerza de unión usando un método que aproxima las energías implicadas cuando un compuesto se adhiere a NS5 en condiciones acuosas similares a las celulares. Este proceso redujo el campo a un puñado de flavonoides destacados, con un candidato, etiquetado PSCdb01560, que se distinguió por su energía de unión predicha particularmente fuerte.
Observar las moléculas moverse en un microscopio virtual
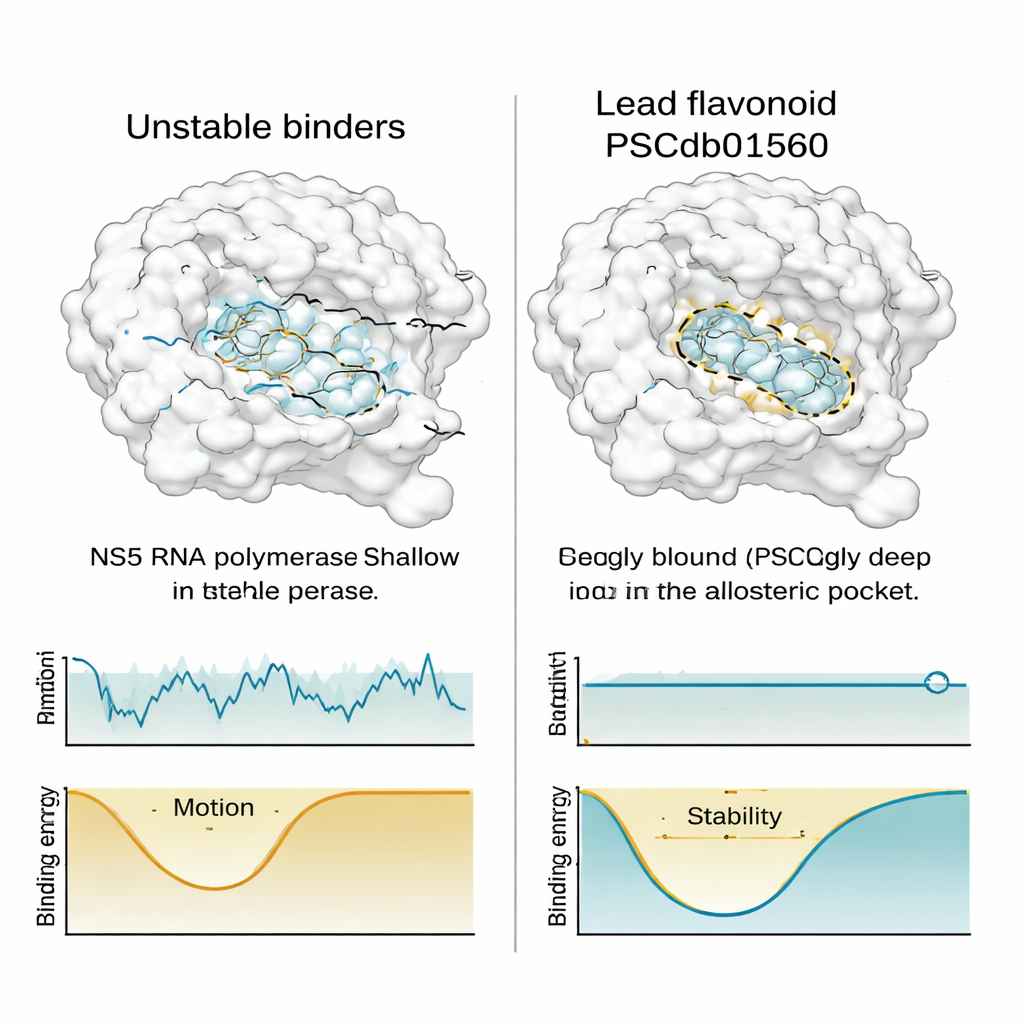
Encajar bien en una instantánea estática no basta; un fármaco útil también debe mantenerse en su sitio cuando todo vibra en la vida real. Para probar esto, el equipo realizó simulaciones de dinámica molecular largas y detalladas—películas computacionales equivalentes a medio microsegundo—para NS5 emparejada con los mejores flavonoides y con un inhibidor de referencia conocido. Registraron cuánto se bamboleaban la proteína y cada compuesto, cuán compacto permanecía el complejo, cuánto se exponía al agua circundante y con qué frecuencia se formaban y rompían contactos químicos clave. PSCdb01560 mostró un comportamiento notablemente estable: permaneció profundamente asentado en el bolsillo N, se movió muy poco en comparación con las moléculas rivales y pareció estabilizar la forma global de NS5 en lugar de alterarla.
En contraste, otros dos flavonoides que inicialmente parecían prometedores comenzaron a desplazarse dentro del bolsillo o se hicieron más expuestos al solvente con el paso del tiempo—señales de una unión más débil y menos fiable. Cuando los investigadores mapearon el "paisaje de energía libre" de cada complejo—una forma de visualizar qué conformaciones son termodinámicamente favorecidas—encontraron que PSCdb01560 ocupaba un valle energético profundo y bien definido, mientras que los compuestos menos estables saltaban entre varias cuencas más someras. Al comparar las instantáneas de menor energía con las posiciones iniciales obtenidas por acoplamiento, la posición de PSCdb01560 apenas cambió, subrayando su lealtad conformacional.
Números que sugieren potencia a nivel de fármaco
Finalmente, el equipo utilizó un marco de cálculo energético para estimar cuán fuertemente se uniría cada flavonoide después de tener en cuenta todo el movimiento simulado. PSCdb01560 alcanzó una energía libre de unión más favorable que el compuesto de referencia establecido, impulsada por una combinación de complementación de forma ajustada, interacciones eléctricas atractivas y contactos hidrofóbicos dentro del bolsillo. Este patrón—afinidad calculada fuerte, posicionamiento estable en el tiempo, flexibilidad interna limitada y participación de residuos cruciales de NS5 compartidos entre cepas del dengue—marca a PSCdb01560 como un punto de partida particularmente convincente para el diseño de fármacos.
Qué podría significar esto para futuros tratamientos contra el dengue
Estos resultados aún no entregan una píldora contra el dengue, pero reducen significativamente la búsqueda. El trabajo identifica un andamiaje flavonoide de origen vegetal que, en el ordenador, supera a varios competidores e incluso a un inhibidor de referencia conocido en estabilidad y fuerza de unión predicha. Los siguientes pasos son experimentales: comprobar si PSCdb01560 realmente bloquea NS5 en probetas, si detiene la replicación del dengue en células infectadas y si resulta seguro en modelos animales. Si esos desafíos se superan, los químicos podrían afinar este flavonoide hasta convertirlo en un antiviral clínicamente útil. Por ahora, el estudio ofrece un mensaje esperanzador: la propia biblioteca química de la naturaleza aún guarda herramientas prometedoras para desarmar una de las amenazas transmitidas por mosquitos de más rápido crecimiento en el mundo.
Cita: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Palabras clave: virus del dengue, polimerasa NS5, inhibidor flavonoide, descubrimiento de fármacos antivirales, acoplamiento molecular