Clear Sky Science · es
El cadmio induce ferroptosis en espermatocitos de ratón activando la vía ROS–TCA
Por qué un metal común importa para la salud masculina
El cadmio es un metal blando empleado en baterías, pigmentos y otros productos industriales. Puede acumularse en el suelo, el agua y los alimentos, entrando silenciosamente en nuestro organismo con el tiempo. Numerosos estudios han relacionado la exposición al cadmio con recuentos de esperma más bajos y una peor calidad seminal en hombres, pero la forma exacta en que daña las células que producen esperma ha sido poco clara. Este estudio se centra en ese problema y revela cómo el cadmio empuja a los espermatocitos de ratón hacia una vía específica de muerte celular vinculada al hierro y a un sistema energético mitocondrial estresado, las centrales eléctricas de la célula.
De la contaminación a los espermatozoides vulnerables
El cadmio es un conocido perturbador ambiental del sistema reproductor masculino. Los hombres expuestos en el trabajo o que viven en regiones contaminadas a menudo presentan menor número de espermatozoides, movilidad reducida, formas anormales e incluso daños en el ADN de los espermatozoides. Estudios en animales reproducen estos hallazgos, mostrando testículos encogidos, barreras protectoras permeables, niveles bajos de testosterona y pérdida generalizada de células germinales. Los autores observaron previamente que el cadmio podía desencadenar una forma inusual de muerte celular dependiente del hierro llamada ferroptosis en el tejido testicular. En el trabajo actual se centraron en los espermatocitos de ratón —células en proceso de convertirse en espermatozoides— para ver exactamente cómo los daña el cadmio y si esa vía vinculada al hierro está implicada.
Sobrecarga de hierro y un tipo especial de muerte celular
Para investigar, el equipo cultivó una línea celular de espermatocitos de ratón en placas y expuso las células al cadmio, con y sin fármacos conocidos por bloquear la ferroptosis. El cadmio redujo la supervivencia celular a la mitad aproximadamente y ralentizó la división celular. Dentro de las células, los niveles de hierro libre y de un marcador de daño lipídico llamado malondialdehído aumentaron drásticamente, mientras que una enzima protectora clave, GPX4, disminuyó. Otras proteínas implicadas en el almacenamiento y la exportación de hierro aumentaron, señalando un manejo del hierro muy alterado. Cuando los investigadores añadieron inhibidores de la ferroptosis —un quelante de hierro y una molécula protectora de lípidos— muchas de estas alteraciones nocivas se atenuaron y la supervivencia celular mejoró. En conjunto, estos cambios coinciden con la firma de la ferroptosis, lo que indica que el cadmio no mata las células de forma vaga, sino que las empuja hacia este programa de muerte específico, mediado por hierro y lípidos.
Mitocondrias bajo asedio
La historia se profundizó cuando los científicos dirigieron su atención a las mitocondrias, los centros energéticos que también generan especies reactivas de oxígeno (ROS) como subproductos. Bajo el microscopio, las células sanas mostraban mitocondrias largas y filamentosas, pero las células expuestas al cadmio exhibieron mitocondrias cortas y fragmentadas, signo de daño estructural. Las mediciones confirmaron que las ROS mitocondriales se dispararon, mientras que el potencial eléctrico a través de la membrana mitocondrial —un indicador clave de función— se redujo. Las células respondieron aumentando sus sistemas de defensa interna, incluidas proteínas reguladas por el sensor de estrés Nrf2, pero estas defensas no fueron suficientes. De forma importante, los fármacos que bloquean la ferroptosis redujeron las ROS mitocondriales y restauraron parcialmente la salud mitocondrial, vinculando las centrales dañadas directamente con la vía de muerte dependiente del hierro.
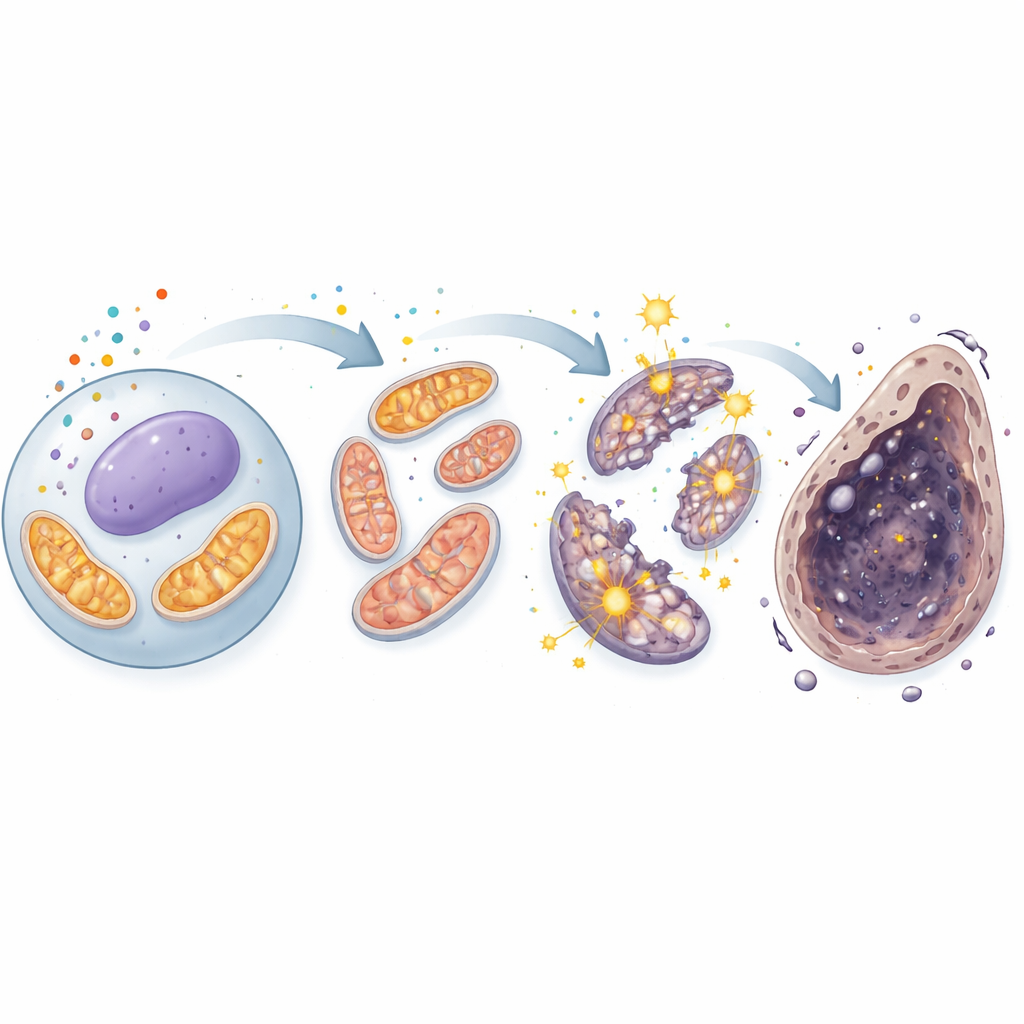
Un círculo vicioso en la central energética de la célula
Usando una combinación de perfilado de la actividad génica y mediciones de metabolitos, los investigadores observaron que el cadmio hizo más que simplemente dañar las mitocondrias: pareció secuestrar su circuito energético central, el ciclo de los ácidos tricarboxílicos (TCA). Los niveles de dos intermediarios centrales del TCA, alfa‑cetoglutarato y succinato, aumentaron significativamente, y se incrementó la actividad de la piruvato carboxilasa, una enzima que aporta nuevo combustible al ciclo. Esto sugiere que el ciclo TCA se volvió paradójicamente hiperactivo en las células dañadas, forzando más electrones a través de la cadena respiratoria y filtrando más ROS en el proceso. Esas ROS adicionales retroalimentaron la química del hierro y el daño a las membranas, reforzando la ferroptosis. De nuevo, los inhibidores de la ferroptosis atenuaron estas distorsiones metabólicas, subrayando el vínculo estrecho entre el cadmio, la sobrecarga mitocondrial y la muerte celular dependiente del hierro.
Qué significa esto para la fertilidad y la investigación futura
En términos sencillos, el estudio muestra que el cadmio ataca a las células formadoras de esperma dañando directamente sus mitocondrias y provocando que su ciclo energético entre en una peligrosa sobreactividad. Esta combinación inunda las células con moléculas reactivas de oxígeno y altera el equilibrio del hierro, empujándolas hacia la ferroptosis. Dado que los espermatocitos son esenciales para producir esperma sano, su pérdida ayuda a explicar por qué la exposición al cadmio se asocia tan fuertemente con una fertilidad masculina reducida. Aunque estos experimentos se realizaron en células de ratón en cultivo, proporcionan un mapa mecanístico claro que futuros estudios en animales y humanos pueden probar. El trabajo también señala estrategias protectoras potenciales: fármacos o nutrientes que calmen el estrés mitocondrial, ajusten finamente el ciclo TCA o prevengan el daño de membranas mediado por hierro podrían ayudar a proteger el sistema reproductor masculino frente a metales ambientales como el cadmio.
Cita: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Palabras clave: toxicidad por cadmio, fertilidad masculina, estrés mitocondrial, ferroptosis, especies reactivas de oxígeno