Clear Sky Science · es
Método práctico de mezcla dentro de la jeringa para una entrega uniforme de partículas durante procedimientos de embolización
Mantener las pequeñas perlas terapéuticas en el blanco
Muchos tratamientos mínimamente invasivos contra el cáncer y de los vasos sanguíneos dependen de microesferas que se inyectan mediante una jeringa para ocluir intencionadamente vasos pequeños. Para que estos procedimientos funcionen como se espera, los médicos necesitan que esas microesferas fluyan hacia el organismo en un chorro suave y uniforme. En la práctica, las microesferas tienden a hundirse o flotar dentro de la jeringa, de modo que los pacientes pueden recibir sobre todo líquido al principio y una ráfaga súbita de esferas al final. Este estudio presenta una solución compacta, alimentada por baterías, para agitar suavemente la jeringa desde el exterior, manteniendo las microesferas bien distribuidas y ayudando a los médicos a administrar tratamientos más previsibles y seguros.
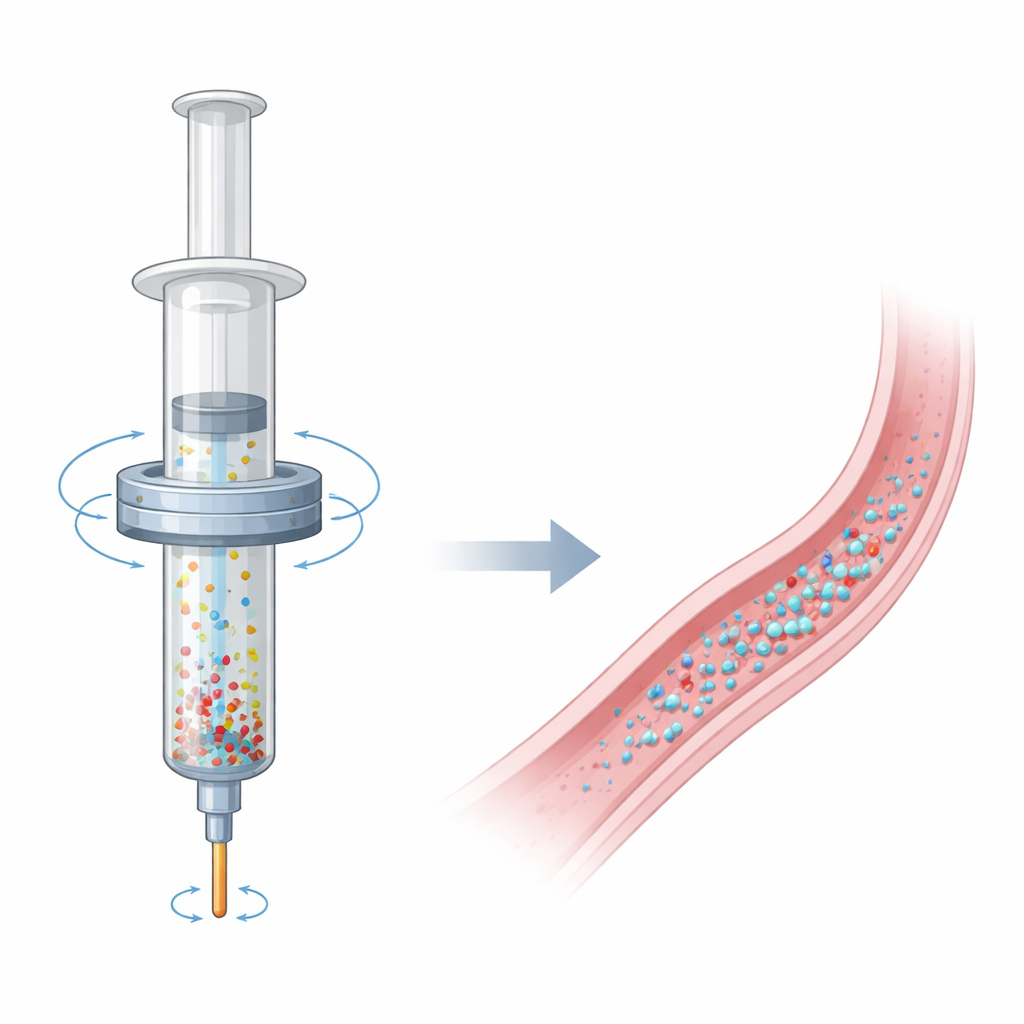
Por qué el flujo desigual de microesferas es un problema oculto
En los procedimientos de embolización, las partículas diminutas se mezclan con un medio de contraste y solución salina para que los médicos puedan observar su desplazamiento bajo rayos X mientras bloquean el flujo sanguíneo hacia un tumor o un vaso anómalo. Incluso cuando la mezcla está bien homogeneizada al inicio, las partículas se separan lentamente del líquido en menos de unos minutos, sedimentando hacia el fondo de la jeringa o flotando hacia la parte superior según su densidad. Dado que estas microesferas son invisibles a los rayos X, el médico solo ve el tinte de contraste, no la verdadera concentración de partículas. Eso hace que la inyección pueda parecer normal en la pantalla mientras que la dosis real de microesferas administrada a lo largo del tiempo es muy desigual: mayoritariamente líquido al principio, seguido de agregados de esferas o incluso un gran bolo al final.
Un anillo simple que convierte la jeringa en un agitador
Los investigadores reutilizaron la carcasa exterior fija de un motor paso a paso común —el mismo tipo de pieza que se usa en impresoras 3D y robots— para crear un campo magnético rotatorio alrededor de una jeringa de plástico estándar. Al retirar las piezas móviles internas del motor, dejaron un «estator» en forma de anillo con una abertura central lo bastante ancha para el cilindro de una jeringa. Dentro de la jeringa colocaron un pequeño agitador magnético con forma de varilla o de impulsor que gira cuando se expone al campo magnético variable generado por el estator. Alimentado por un controlador compacto y pilas AA, el estator hace girar el varillaje magnético y cambiar su sentido de giro a velocidades programadas, agitando suavemente el fluido y las partículas sin piezas móviles exteriores a la jeringa.
Evaluación de la uniformidad de las microesferas
Para comprobar si esta mezcla dentro de la jeringa mejora realmente la entrega, el equipo empleó grandes microesferas de hidrogel usadas clínicamente suspendidas en una mezcla de agua y contraste. Filmaron las partículas mientras fluían por un canal de observación personalizado conectado a la jeringa, usando un microscopio para contar las esferas cuadro a cuadro a medida que salían durante inyecciones a distintas velocidades. Cuando la jeringa permanecía inmóvil tras una agitación inicial, esperar más tiempo antes de inyectar provocaba que más partículas sedimentaran. Eso produjo un flujo muy desigual: salida modesta de microesferas al inicio, un largo período de casi solo líquido y luego una oleada de esferas densamente empaquetadas al final. Medido matemáticamente, la no uniformidad aumentaba con el retraso, y era especialmente grave a velocidades de inyección lentas, donde las partículas tenían tiempo de sedimentar durante el procedimiento.
Cómo cambia el panorama el agitado continuo
Cuando el agitador magnético se activó dentro de la jeringa, girando durante un período de espera de dos minutos y durante la inyección, la entrega de microesferas se volvió mucho más uniforme. En la condición de peor caso —inyección lenta tras un largo retraso—, el sistema de mezcla redujo las variaciones en la concentración de microesferas aproximadamente cuatro veces a velocidades de inyección habituales y al menos dos veces incluso en la velocidad más lenta. El agitador de varilla rindió algo mejor que el de impulsor, por lo que se convirtió en el diseño preferido. El equipo también exploró distintas velocidades de giro y la frecuencia de los cambios de sentido. Velocidades moderadas (alrededor de diez vueltas por segundo) con reversiones frecuentes cada cuarto de segundo produjeron el flujo más uniforme; giros muy lentos o muy rápidos, o girar siempre en la misma dirección, tendían a empujar las esferas lejos de la salida o a mezclarlas solo en una parte de la jeringa. Ráfagas cortas y de alta velocidad separadas por pausas podían re‑suspender rápidamente todo el contenido con una perturbación mínima en la inyección.
Del montaje de laboratorio al uso en el mundo real
Más allá de los experimentos principales, los autores mostraron que el mismo enfoque puede evitar que las partículas sedimenten rápidamente en líquidos finos y similares al agua y puede re‑suspenderlas parcialmente en fluidos de contraste espesos y almibarados. Discuten cómo factores como el tamaño de las partículas, la densidad y la viscosidad del fluido condicionarán la mejor receta de mezcla en distintas aplicaciones, y señalan consideraciones prácticas como la generación de calor, el ángulo de la jeringa y el pequeño volumen ocupado por el agitador. Es importante que el sistema funcione con piezas de motores comerciales y jeringas estándar, sin necesidad de cuerpos de jeringa personalizados ni mecanismos mecánicos complejos, lo que facilita su integración en flujos de trabajo clínicos o de investigación.
Qué significa esto para pacientes y profesionales
Para el público general, el resultado clave es que este dispositivo convierte una jeringa normal en un inyector autoagitado capaz de entregar las microesferas terapéuticas de forma mucho más uniforme a lo largo del tiempo. En lugar de un flujo impredecible de unas pocas microesferas seguido por una avalancha repentina, el paciente tiene más probabilidades de recibir un chorro constante y controlado. Eso debería ayudar a los médicos a alcanzar sus objetivos con mayor fiabilidad, reducir el riesgo de oclusiones en tejido sano y hacer la dosificación más consistente entre casos. Aunque hacen falta más estudios para ajustar los parámetros de mezcla según distintos tipos de microesferas y fluidos, el trabajo demuestra que un simple anillo de agitación magnética podría resolver de forma silenciosa un problema antiguo y en gran parte invisible en los tratamientos guiados por imagen.
Cita: Ng, D.KH., Drangova, M. & Holdsworth, D.W. Practical in-syringe mixing method for uniform particle delivery during embolization procedures. Sci Rep 16, 9245 (2026). https://doi.org/10.1038/s41598-026-38823-x
Palabras clave: embolización, microesferas, mezcla en jeringa, agitación magnética, radiología intervencionista