Clear Sky Science · es
Determinantes a nivel de residuos de la estabilidad térmica de la endolisina extremófila Ts2631
Por qué importan los virus amantes del calor para los antibióticos del futuro
A medida que aumenta la resistencia a los antibióticos, los científicos buscan con urgencia nuevas formas de eliminar bacterias peligrosas. Un enfoque prometedor toma prestadas armas de virus que infectan bacterias, llamados bacteriófagos. Estos virus producen enzimas, conocidas como endolisinas, que perforan la pared celular bacteriana. El estudio que se discute aquí se centra en una endolisina extraordinariamente resistente al calor, Ts2631, procedente de un virus que vive en manantiales termales islandeses. Al identificar qué bloques constructivos individuales de esta proteína la hacen tan estable a temperaturas cercanas al punto de ebullición, los investigadores esperan diseñar enzimas antibacterianas más robustas y duraderas para la medicina y la biotecnología. 
Una herramienta viral forjada en manantiales hirvientes
Ts2631 procede de un bacteriófago que infecta la bacteria termófila Thermus scotoductus, que prospera en aguas que alcanzan ampliamente más de 60 °C. La enzima Ts2631 corta un enlace específico en el peptidoglucano, la malla resistente que rodea las células bacterianas. Lo que distingue a Ts2631 es su termestabilidad extrema: permanece plegada hasta aproximadamente 100–105 °C, según la solución. Esto está muy por encima de las temperaturas a las que la mayoría de las proteínas se deshacen. Los autores compararon Ts2631 con su pariente mejor estudiado procedente de un virus de temperatura moderada, la lisozima T7, para averiguar qué trucos estructurales ha utilizado la naturaleza para mantener intacta a Ts2631 en condiciones tan extremas.
Bucle más cortos y una mezcla diferente de bloques constructivos
Las proteínas son cadenas de 20 tipos de aminoácidos, plegadas en formas intrincadas. Cuando los investigadores superpusieron las estructuras 3D de Ts2631 y la lisozima T7, encontraron que la arquitectura general es muy similar: ambas tienen un núcleo compacto de hélices y hebras. La diferencia clave radica en las regiones de bucle flexibles que conectan estos elementos. En Ts2631, esos bucles son más cortos y muestran menor flexibilidad, mientras que la lisozima T7 tiene bucles más largos y más laxos. Ts2631 también contiene mayor proporción de ciertos aminoácidos a menudo vinculados a la resistencia al calor: la rígida prolina; residuos aromáticos como tirosina y triptófano; y el arginino cargado positivamente. Al mismo tiempo, presenta menos residuos de serina, ácido aspártico y ácido glutámico, que pueden hacer que las proteínas sean más vulnerables a altas temperaturas. Este patrón se mantiene no solo frente a la lisozima T7 sino también cuando se compara Ts2631 con cientos de miles de proteínas virales y muchos millones de proteínas bacterianas.
Intercambiar aminoácidos individuales para probar su importancia
Para pasar de correlaciones a causa y efecto, el equipo sustituyó sistemáticamente 55 aminoácidos individuales en Ts2631 y midió cómo cada mutación afectaba la temperatura de fusión (Tm) y la capacidad de la enzima para degradar las paredes celulares bacterianas. Algunos cambios alrededor del sitio activo que contiene zinc fueron especialmente dañinos. Cuando alteraron tres residuos que coordinan el zinc (H30, H131 y C139), la Tm de la proteína cayó hasta alrededor de 20 °C y se perdió la actividad. Dos tirosinas conservadas (Y60 y Y69) también contribuyeron a la estabilidad. Sorprendentemente, eliminar un puente disulfuro—un tipo de enlace covalente entre las cisteínas C80 y C90—en realidad elevó la temperatura de fusión, aunque destruyó la actividad. Esto muestra que ser muy estable en tubo de ensayo no siempre significa que una proteína funcionará mejor en condiciones reales. 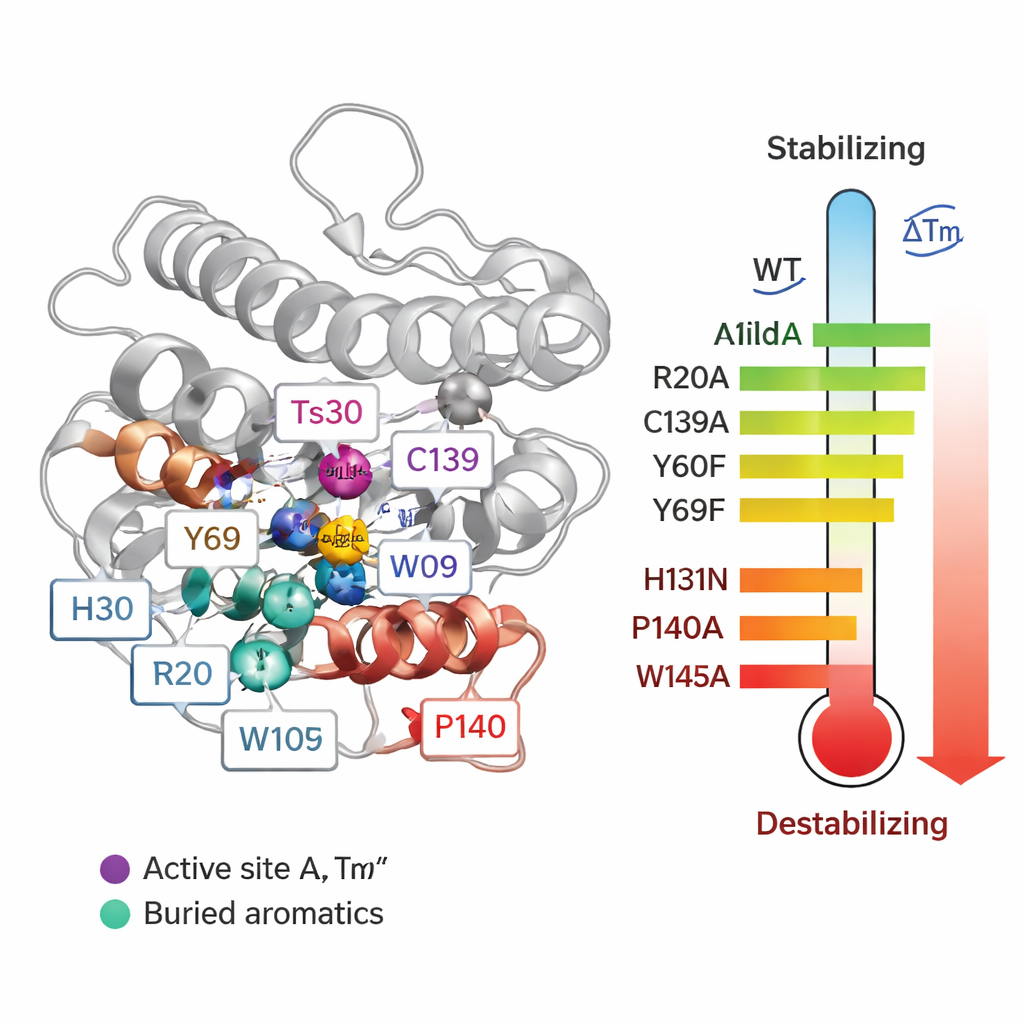
Anclas aromáticas ocultas y un agarre clave en la pared bacteriana
Los resultados más llamativos provinieron de mutar residuos de prolina y triptófano. Cambiar una sola prolina (P140), situada junto a la cisteína de unión al zinc C139, redujo la Tm en más de 21 °C y debilitó la actividad tras el calentamiento, porque la mutación alteró una geometría de enlace especial necesaria para la correcta unión del metal. Varios triptófanos profundamente enterrados (W102, W109 y especialmente W145) también resultaron críticos: sustituirlos por alanina provocó caídas de la Tm de 14–24 °C y volvió a la enzima mucho más sensible al calor en las pruebas de actividad. Estos residuos aromáticos actúan como anclas internas que bloquean el núcleo de la proteína en su lugar. Entre los argininos, la mayoría tuvo poco efecto en la estabilidad, pero R20 resultó esencial para agarrar el peptidoglucano. Cuando R20 fue reemplazado, la enzima se unió mal a la pared celular bacteriana y perdió actividad al calentarse, lo que revela que algunos residuos contribuyen más a la función que a la mera robustez térmica.
De enzimas de manantiales termales a antibacterianos más resistentes
En conjunto, el estudio muestra que la extraordinaria resistencia al calor de Ts2631 descansa en un puñado de aminoácidos bien situados más que en un reforzamiento uniforme de toda la proteína. Los residuos que unen el zinc, una prolina conservada cerca del sitio activo y cadenas laterales aromáticas enterradas forman un núcleo estabilizador, mientras que algunas características clásicas estabilizadoras, como los puentes disulfuro o los puentes salinos, importan menos aquí de lo esperado. Para el campo en general, este trabajo sugiere que las endolisinas mesófilas (de temperatura moderada) podrían hacerse más duraderas mediante el intercambio selectivo de posiciones por triptófano o prolina sin sacrificar la actividad antibacteriana. En otras palabras, al aprender cómo la naturaleza construye enzimas que resisten temperaturas cercanas a la ebullición, los científicos obtienen un plano práctico para diseñar antibióticos basados en proteínas más fiables y de mayor vida útil.
Cita: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Palabras clave: endolisina termosestable, enzimas de bacteriófagos, termestabilidad de proteínas, resistencia a antibióticos, ingeniería de proteínas