Clear Sky Science · es
Estudio sobre biomarcadores de la transformación inducida por homocisteína de las células del músculo liso vascular en células espumosas
Por qué las arterias obstruidas comienzan con pequeños cambios celulares
La aterosclerosis —el lento taponamiento y endurecimiento de las arterias— es una causa principal de infartos y accidentes cerebrovasculares. Normalmente escuchamos sobre el colesterol y la dieta, pero menos sobre cómo las células individuales de la pared vascular cambian a medida que progresa la enfermedad. Este estudio examina de cerca uno de esos desencadenantes, una molécula sanguínea llamada homocisteína, y muestra cómo puede empujar a las células musculares arteriales, normalmente bien comportadas, a acumular grasa y convertirse en las llamadas células espumosas, los ladrillos de las placas peligrosas.
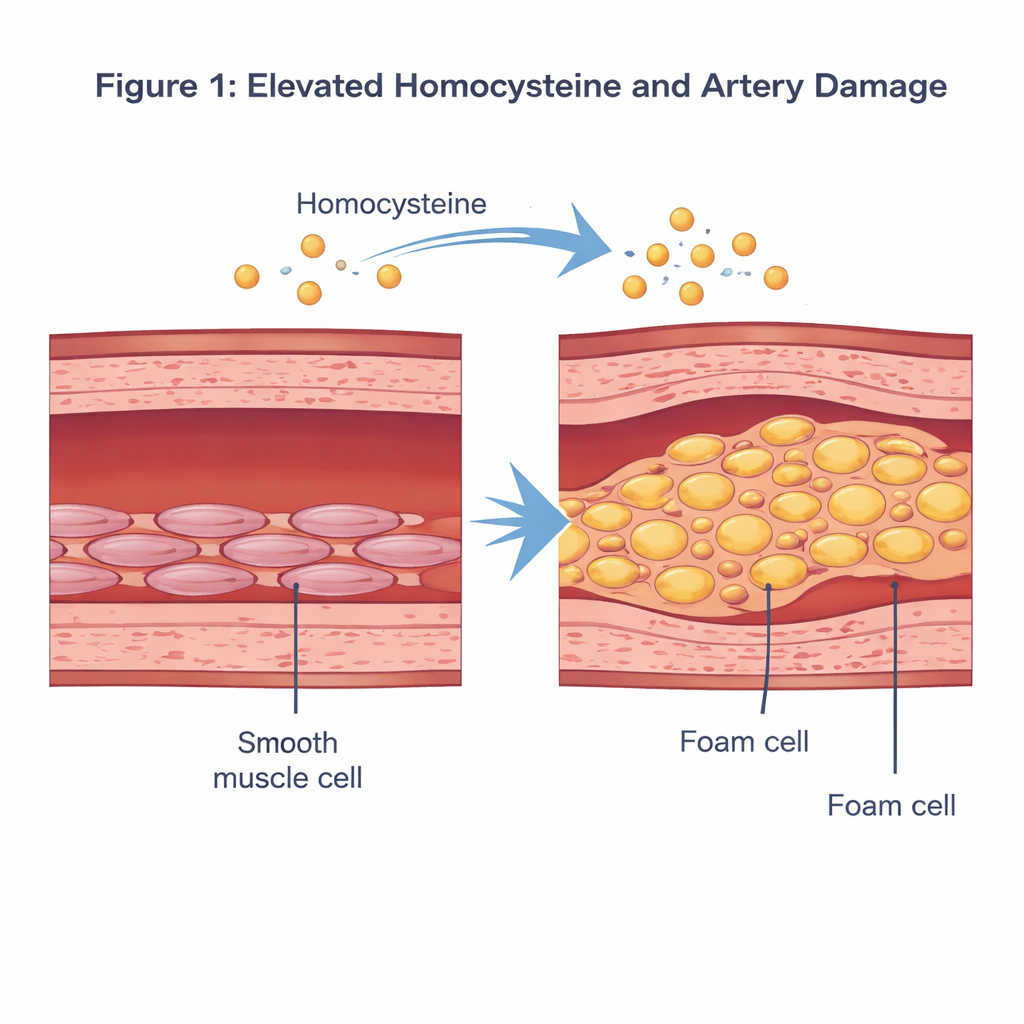
Un aminoácido problemático en el torrente sanguíneo
La homocisteína es un aminoácido que contiene azufre y se produce cuando nuestro organismo procesa el nutriente dietético metionina. En condiciones normales, su nivel en sangre es bajo. Cuando supera aproximadamente los 15 micromoles por litro —una condición llamada hiperhomocisteinemia— los estudios epidemiológicos la han vinculado a un mayor riesgo de enfermedad cardiovascular. Investigaciones previas sugerían que el exceso de homocisteína puede dañar el revestimiento interno de las arterias, provocar inflamación y alterar el comportamiento de las células del músculo liso vascular, que se sitúan en la capa media de la pared vascular y ayudan a regular la presión arterial mediante contracción y relajación.
Cómo las células musculares arteriales se convierten en células espumosas llenas de grasa
Los investigadores se centraron en cómo la homocisteína remodela estas células del músculo liso. En placas de laboratorio, expusieron células humanas del músculo liso vascular a una dosis de homocisteína diseñada para imitar un estado similar al de la enfermedad y las compararon con células no tratadas. Mediante tinciones estándar y pruebas bioquímicas, observaron que las células tratadas con homocisteína se llenaban de gotas de grasa teñidas de rojo, y sus niveles de colesterol y triglicéridos aumentaban drásticamente. Al mismo tiempo, los marcadores proteicos de su identidad “contráctil” habitual disminuyeron, mientras que aumentaron los marcadores de un estado más sintético y formador de placas. En conjunto, estos cambios muestran que la homocisteína puede alejar a las células del músculo liso de su papel normal y conducirlas hacia un fenotipo similar a células espumosas, cargado de lípidos, que contribuye directamente a la formación de placas.
Buscando huellas moleculares dentro de las células
Para entender qué proteínas cambian durante esta transformación, el equipo recurrió a la proteómica moderna, una tecnología que puede medir miles de proteínas a la vez. Compararon los niveles de proteínas en células tratadas con homocisteína frente a controles y cuantificaron de forma fiable casi 4.800 proteínas. De ellas, 54 destacaron por alterarse significativamente: 13 aumentaron y 41 disminuyeron. Muchas de las proteínas cambiantes están implicadas en el manejo de lípidos, la supervivencia celular, el estrés oxidativo y la remodelación estructural de las células. Los autores usaron luego herramientas bioinformáticas para agrupar estas proteínas en vías funcionales y mapear cómo interactúan entre sí, destacando redes vinculadas al metabolismo del colesterol y a las respuestas al estrés en la pared vascular.
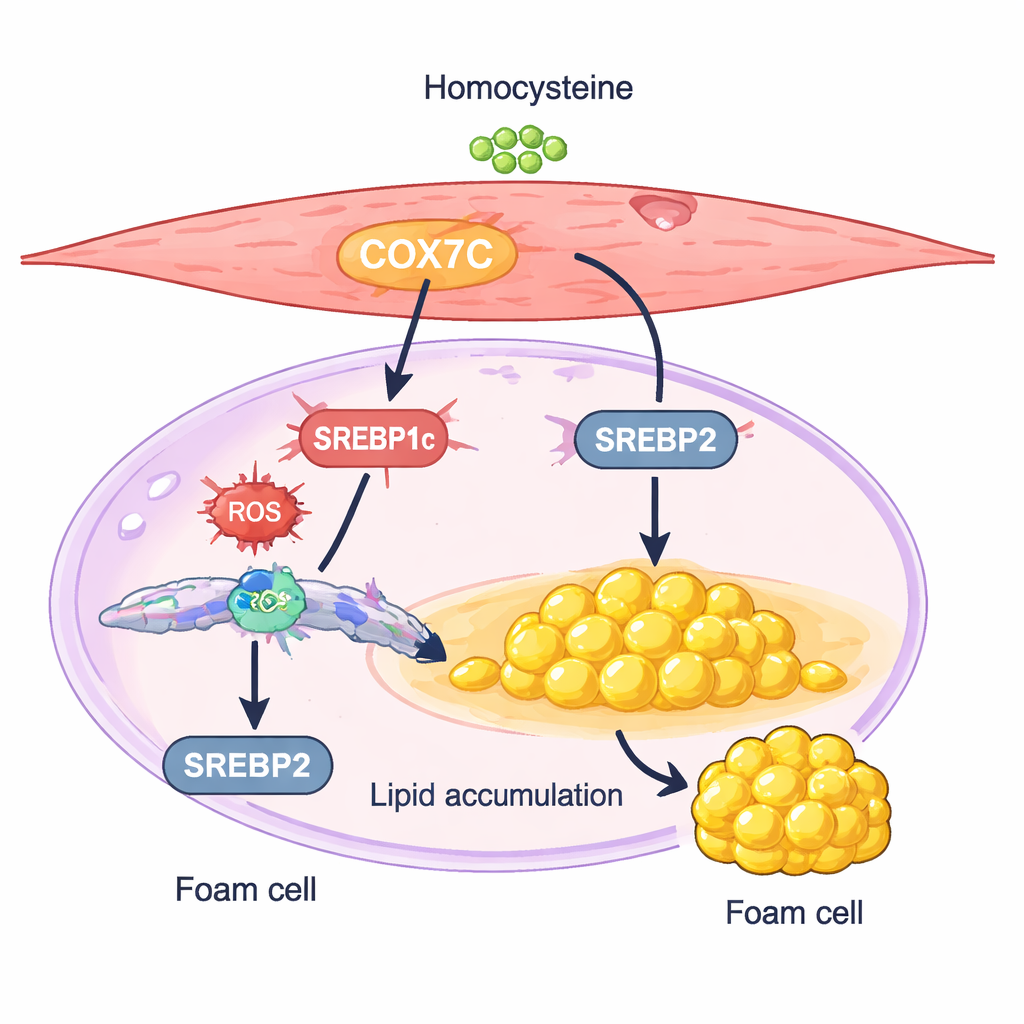
Un interruptor mitocondrial que empuja a las células a almacenar grasa
Una proteína llamada COX7C emergió como una sospechosa particularmente interesante. COX7C es un componente de las centrales energéticas de la célula, las mitocondrias, donde ayuda a gestionar la producción de energía. En las células del músculo liso tratadas con homocisteína, los niveles de COX7C fueron más altos que en los controles. Los investigadores demostraron que aumentar aún más COX7C hacía que las células acumularan más grasa y expresaran niveles superiores de dos reguladores maestros de la producción de lípidos, SREBP1c y SREBP2. Silenciar COX7C produjo el efecto contrario: atenuó la actividad de SREBP, redujo la acumulación de colesterol y triglicéridos y mitigó los cambios similares a células espumosas. Estos resultados apoyan un modelo en el que la homocisteína eleva COX7C en las mitocondrias, incrementa las señales de estrés celular y, a su vez, activa la síntesis lipídica dirigida por SREBP, empujando a las células del músculo liso hacia un estado acaparador de lípidos.
Qué significa esto para la salud cardiovascular y futuras terapias
Este trabajo aún no demuestra lo que ocurre en las arterias humanas y se realizó en cultivos celulares más que en pacientes. Aun así, ofrece una mirada detallada sobre cómo la homocisteína elevada puede ayudar a convertir células musculares arteriales beneficiosas en células espumosas dañinas, e identifica a COX7C y proteínas relacionadas como posibles biomarcadores o dianas farmacológicas. Para el lector general, el mensaje clave es que, más allá del colesterol “bueno” y “malo”, pequeños cambios en la química sanguínea —como el exceso de homocisteína— pueden reprogramar la pared vascular desde dentro. Al identificar jugadores moleculares como COX7C y la vía SREBP, este estudio sienta las bases para estrategias futuras destinadas a impedir la formación de placas, evitando que las células arteriales se conviertan en pequeños depósitos de grasa.
Cita: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Palabras clave: aterosclerosis, homocisteína, células espumosas, células del músculo liso vascular, COX7C