Clear Sky Science · es
La inhibición de puntos de control inmunitarios aumenta la respuesta de linfocitos T específicas frente a antígenos en el cáncer de cabeza y cuello
Volver las defensas del cuerpo contra el cáncer de cabeza y cuello
Los cánceres de cabeza y cuello siguen siendo difíciles de tratar, y aun las nuevas inmunoterapias potentes solo benefician a una fracción de los pacientes. Este estudio explora una idea prometedora: enseñar a las células inmunitarias a reconocer mejor señales específicas del cáncer y luego liberar a esas células de los “frenos” moleculares para que puedan atacar los tumores con mayor eficacia. Para las personas que viven con, o están en riesgo de, cáncer de cabeza y cuello, este trabajo apunta hacia futuras vacunas y combinaciones de fármacos que podrían hacer que los tratamientos actuales sean más potentes y duraderos.
Por qué la inmunoterapia actual ayuda a tan pocos
La inmunoterapia moderna contra el cáncer suele dirigirse a proteínas llamadas puntos de control inmunitarios, que actúan como frenos en los linfocitos T, las células blancas capaces de destruir tumores. En el carcinoma de células escamosas de cabeza y cuello (HNSCC), ya se usan fármacos que bloquean el punto de control PD-1—como nivolumab o pembrolizumab—. Sin embargo, solo alrededor del 20 % de los pacientes se beneficia y muchos cánceres acaban progresando. Los autores se propusieron entender, en un entorno de laboratorio controlado, cómo afecta el bloqueo de PD-1 y puntos de control relacionados a los linfocitos T que han sido primados para reconocer marcadores tumorales específicos, y si combinar varios fármacos que bloquean puntos de control aporta algo más que el bloqueo de PD-1 por sí solo.
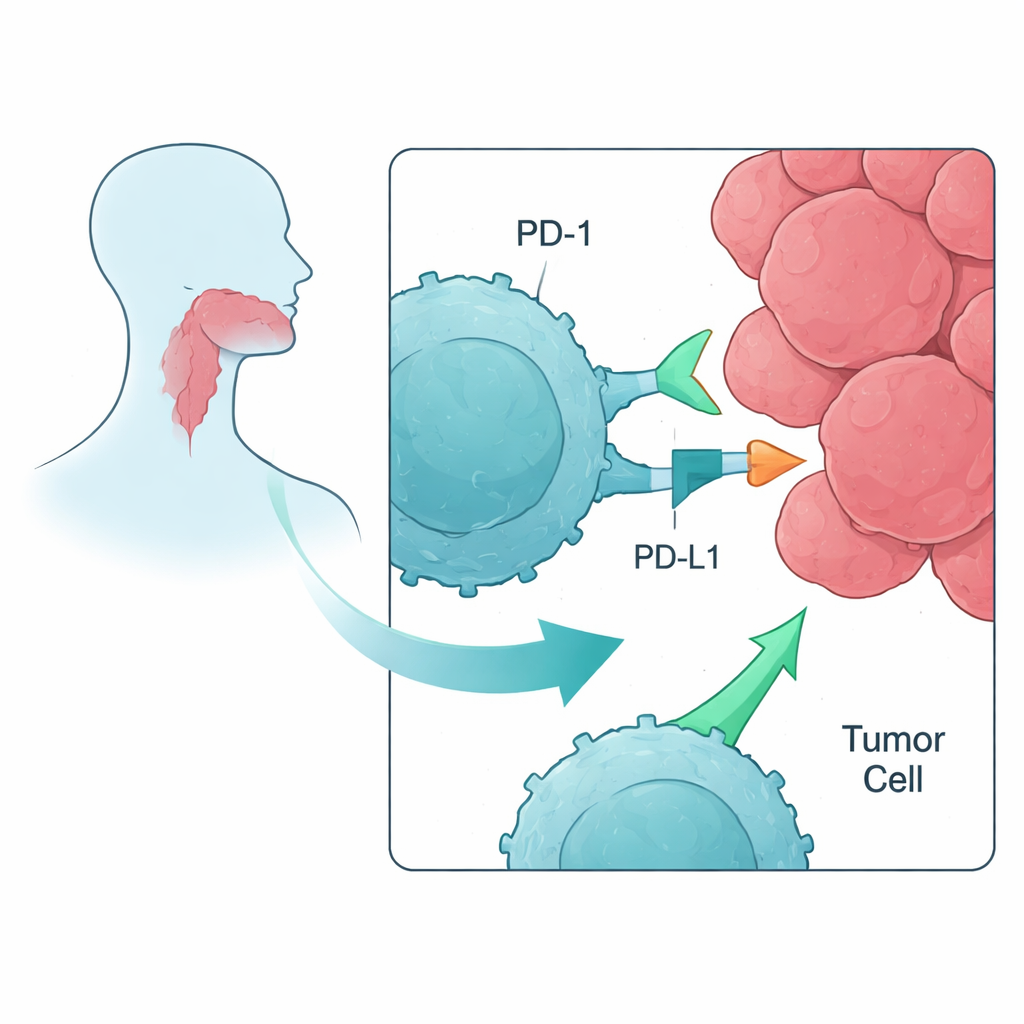
Entrenar a las células inmunitarias para ver los objetivos del cáncer
Los investigadores comenzaron con células sanguíneas de voluntarios sanos en lugar de pacientes, para modelar cómo podría responder un sistema inmunitario menos dañado en las primeras etapas de la enfermedad. Aislaron células mononucleares de sangre periférica, que incluyen linfocitos T, y las expusieron a fragmentos cortos de proteínas—péptidos—tomados de antígenos asociados a tumores que se encuentran comúnmente en cánceres de cabeza y cuello. Tres de esos objetivos resultaron especialmente buenos para activar linfocitos T: MAGE, NY-ESO-1 y PRAME. Durante aproximadamente una semana en cultivos mixtos de linfocitos y péptidos, estos péptidos actuaron como mini-vacunas, expandiendo linfocitos T raros que podían reconocer específicamente cada marcador relacionado con el cáncer.
Soltar los frenos en linfocitos T entrenados
A continuación, el equipo evaluó cómo se comportaban estos linfocitos T entrenados cuando se enfrentaban a células reales de cáncer de cabeza y cuello en presencia o ausencia de anticuerpos que bloquean puntos de control. Emplearon un ensayo estándar de laboratorio (ELISPOT) para medir la liberación de interferón gamma y granzima B—señales de que los linfocitos T están activados y son capaces de matar. En múltiples donantes, la adición del anticuerpo anti-PD-1 aumentó de manera consistente la respuesta de los linfocitos T específicos frente a la línea celular tumoral, incrementando frecuentemente la actividad entre un 60 % y 100 % o más en comparación con la estimulación solo con péptidos. En contraste, el bloqueo de otros puntos de control, como LAG-3 o TIM-3, ya fuese solo o en combinación con el bloqueo de PD-1, aportó poco o ningún beneficio adicional en este sistema.
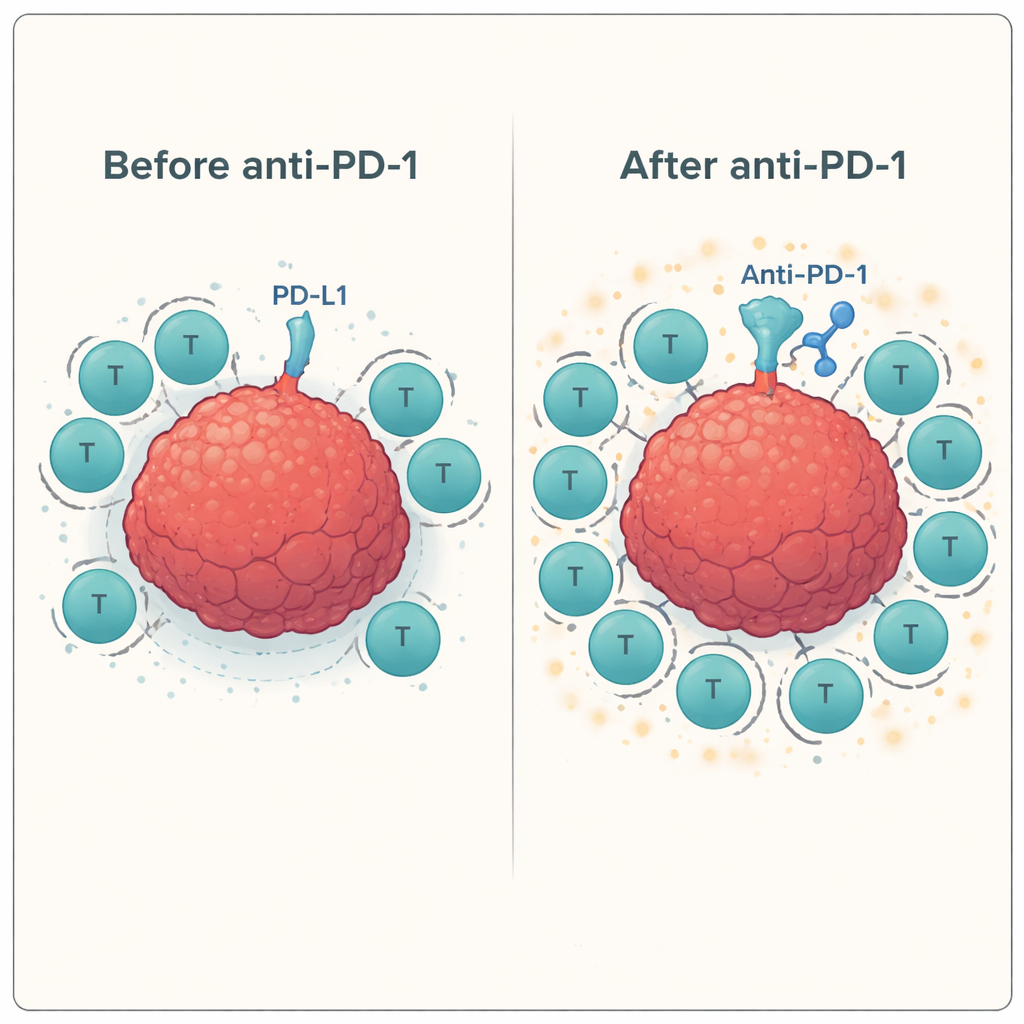
Mapear el paisaje inmunitario en detalle
Para entender por qué algunas combinaciones funcionaron y otras no, los investigadores utilizaron citometría de flujo, una técnica que cuenta y caracteriza células individuales. Mostraron que tanto los linfocitos T como las células tumorales expresan PD-1 y sus ligandos PD-L1 y PD-L2 a niveles significativos, creando múltiples puntos de contacto donde el freno PD-1 puede activarse—y por tanto ser bloqueado por fármacos. También estaban presentes marcadores asociados a LAG-3 y TIM-3, pero la línea celular tumoral expresaba solo un subconjunto de sus moléculas compañeras, lo que podría ayudar a explicar el impacto limitado de dirigirse a esos puntos de control. Además, observaron una tendencia hacia un aumento de las “señales de avance” (moléculas coestimuladoras como CD137 y GITR) en los linfocitos T tras la estimulación con péptidos y el bloqueo de PD-1, lo que sugiere que una vez que se libera el freno principal, el acelerador puede actuar con más fuerza.
Qué podría significar esto para futuros pacientes
Dado que estos experimentos se realizaron fuera del cuerpo, no pueden imitar completamente el complejo ambiente tumoral ni los sistemas inmunitarios a menudo debilitados de pacientes que han recibido quimioterapia y radioterapia. Aun así, los hallazgos ofrecen un mensaje claro y directo: cuando los linfocitos T primero se enseñan a reconocer banderas específicas del cáncer (mediante una vacuna de péptidos) y luego se les quita el freno de PD-1, se vuelven mucho mejores en atacar células tumorales de cabeza y cuello. Añadir más fármacos que bloqueen puntos de control además de PD-1 no ayudó en este contexto. Los autores concluyen que una estrategia focalizada—vacunar a los pacientes con péptidos asociados a tumores como MAGE, NY-ESO-1 o PRAME, combinada con el bloqueo de PD-1—merece ser probada en ensayos clínicos como forma de convertir el sistema inmunitario de más pacientes en un combatiente eficaz contra el cáncer.
Cita: Schuler, P.J., Oliveri, F., Puntigam, L. et al. Immune checkpoint inhibition increases antigen-specific T cell response in head and neck cancer. Sci Rep 16, 5583 (2026). https://doi.org/10.1038/s41598-026-38740-z
Palabras clave: cáncer de cabeza y cuello, terapia de puntos de control inmunitario, bloqueo de PD-1, vacunas contra el cáncer, antígenos tumorales